plaquetas - Platelet
| As plaquetas | |
|---|---|
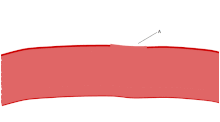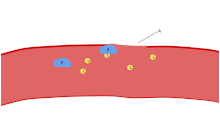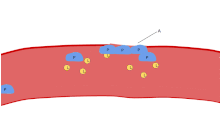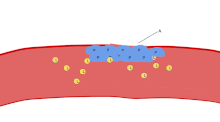
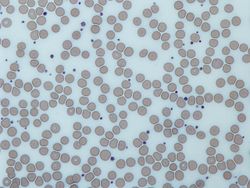 Imagem a partir de um microscópio de luz (500 ×) a partir de um coradas com Giemsa periférica esfregaço de sangue que mostra plaquetas (pontos azuis) rodeadas por células vermelhas do sangue (estruturas circulares rosa)
| |
| detalhes | |
| Precursor | megacariócitos |
| Função | A formação de coágulos sanguíneos; prevenção de sangramento |
| identificadores | |
| latino | trombócitos |
| Malha | D001792 |
| FMA | 62851 |
|
termos anatômicos de microanatomia [ Edit on wikidata ]
| |
As plaquetas , também chamadas de trombócitos (a partir de θρόμβος grego, "coágulo" e κύτος, "célula"), são um componente do sangue , cuja função (juntamente com os factores de coagulação ) consiste em fazer reagir a hemorragia da lesão do vaso sanguíneo por aglomeração, iniciando-se assim uma coágulo de sangue . As plaquetas não têm núcleo celular : elas são fragmentos de citoplasma que são derivados a partir dos megacariócitos da medula óssea, Que, em seguida, entram na circulação. As plaquetas circulantes n activadas são discóide biconvexa (lente em forma de) estruturas, 2-3? M de diâmetro maior. As plaquetas activadas têm projecções de membrana de células que cobrem a sua superfície. As plaquetas são encontrados apenas em mamíferos, enquanto que em outros vertebrados (por exemplo, pássaros, anfíbios) trombócitos circular como intactas as células mononucleares .
Em uma coradas esfregaço de sangue , plaquetas aparecem como manchas de cor púrpura escura, cerca de 20% do diâmetro das células vermelhas do sangue. A mancha é usada para examinar as plaquetas de tamanho, forma, número qualitativa, e aglomeração. Um adulto saudável tem, tipicamente, 10 a 20 vezes mais glóbulos vermelhos do que as plaquetas. Uma das principais funções das plaquetas é contribuir para a hemostasia : o processo de parar o sangramento no local da interrupção endotélio . Eles se reúnem no local ea menos que a interrupção é fisicamente muito grande, eles tapar o buraco. Primeiro, plaquetas anexar a substâncias fora do endotélio interrompido: adesão . Em segundo lugar, eles mudam de forma, ligar receptores e mensageiros químicos secretar: activação . Em terceiro lugar, eles se conectam entre si através de pontes de receptores: agregação . A formação deste tampão de plaquetas (hemostase primária) está associada com a activação da cascata de coagulação , com a resultante de fibrina deposição e ligando (hemostasia secundária). Estes processos podem sobrepor-se: o espectro é a partir de um tampão de plaquetas predominantemente, ou "coágulo branco" para um predominantemente de fibrina, ou "coágulo vermelho" ou a mistura mais típica. Alguns acrescentar a subsequente retracção e de inibição de plaquetas como quarta e quinta etapas para a conclusão do processo e ainda outros se adicionar um sexto passo, a reparação de feridas . As plaquetas também participam em ambos inata e respostas imunes adaptativas intravasculares. A membrana da célula das plaquetas tem receptores para colagénio. Seguindo a ruptura da parede do vaso sanguíneo, as plaquetas são expostas e que aderem ao colagénio no tecido conjuntivo circundante.
Concentração de plaquetas de baixa é chamada trombocitopenia , e é devido a qualquer diminuição da produção ou destruição aumentada . Concentração de plaquetas elevada é chamado de trombocitose , e é ou congénita , reactivo (a citoquinas), ou devido a produção desregulada : uma das neoplasias mieloproliferativas ou de certos outros neoplasmas mieldes. Um distúrbio da função das plaquetas é uma trombocitopatia .
Plaquetas normais podem responder a uma anomalia na parede do vaso , em vez de hemorragia, resultando em inadequado de plaquetas de adesão / activação e trombose : a formação de um coágulo dentro de um vaso intacto. Este tipo de trombose surge por mecanismos diferentes dos de um coágulo de normais: ou seja, estendendo-se a fibrina de trombose venosa ; estendendo-se uma placa arterial instável ou rompido, causando trombose arterial ; e trombose da microcirculação. Um trombo arterial pode obstruir parcialmente o fluxo de sangue, causando a jusante isquemia , ou pode obstruir completamente, fazendo com que a jusante morte do tecido .
Medição
Concentração de plaquetas é medida, quer manualmente, utilizando um hemocitómetro , ou colocando o sangue num analisador de plaquetas automatizado usando impedância eléctrica , tal como um contador de Coulter . O intervalo normal (99% da população analisados) para plaquetas em indivíduos saudáveis caucasianos é 150.000 a 450.000 por milímetro cúbico (um milímetro 3 é igual a um microlitro). ou 150-450 x 10 9 por litro. A escala normal foi confirmado para ser o mesmo nas populações idosas e espanhol.
O número de plaquetas varia entre individuals.The gama fisiológica normal é de 200000-500.000 por microlitro de sangue. Uma vez que contêm receptores para trombopoietina (a protea que facilita a maturação de megacariócitos e libertação de plaquetas), um maior número de plaquetas liga-se mais da proteína. Por conseguinte, existe a estimulação para a produção de mais trombopoietina no fígado e rins. Esta é a base para a produção de mais trombopoietina e, como resultado, mais plaquetas no sangue durante o processo de coagulação do sangue.
Forma
Numa primeira aproximação, a forma de plaquetas pode ser considerado similar ao esferóides achatados, com um semiaxis proporção de 2 para 8. Esta aproximação é muitas vezes utilizado para modelar as propriedades hidrodinâmicas e ópticas de uma população de plaquetas, assim como para restaurar os parâmetros geométricos de plaquetas individuais medidos por citometria de fluxo. modelos biofísicos mais precisas da morfologia da superfície das plaquetas, que modelo de sua forma a partir de primeiros princípios, torná-lo possível obter uma geometria de plaquetas mais realista em um estado calmo e ativada
Estrutura
Estruturalmente, o de plaquetas pode ser dividida em quatro zonas, a partir periférico para mais íntimo:
- zona periférica - é rica em glicoproteínas necessárias para a adesão de plaquetas, activação e agregação. Por exemplo, a GPIb / IX / X; GPVI; GPIIb / IIIa.
- Sol-gel zona - é rica em microtúbulos e microfilamentos, permitindo que as plaquetas para manter a sua forma discóide.
- Zona organela - é rico em granulados de plaquetas. Alfa grânulos contêm mediadores de coagulação tais como o factor V, o factor VIII, fibrinogénio, fibronectina, factor de crescimento derivado de plaquetas, e agentes quimiotácticos. Grânulos delta, ou corpos densos , conter ADP, cálcio, a serotonina, que são mediadores de activação de plaquetas.
- Zona membranoso - contém as membranas derivadas a partir do retículo endoplasmático liso megacariocítica organizados em um sistema tubular denso que é responsável pela tromboxano A2 síntese. Este sistema tubular densa está ligado à membrana plaquetária superfície para auxiliar a libertação de tromboxano A2.
Desenvolvimento
- Megacariócitos e à produção de plaquetas é regulada por trombopoietina , uma hormona produzida nos rins e fígado.
- Cada megacariocítica produz entre 1.000 e 3.000 plaquetas durante a sua vida útil.
- Uma média de 10 11 plaquetas são produzidos diariamente em um adulto saudável.
- Reservar plaquetas são armazenadas no baço, e são libertadas quando necessário por contracção do baço induzida pelo sistema nervoso simpático.
- A vida média de plaquetas circulantes é de 8 a 9 dias. A esperança de vida de plaquetas individuais é controlada por regulação da via apoptótica interna, que tem uma Bcl-x L temporizador.
- Plaquetas velhas são destruídas por fagocitose no baço e no fígado.
hemostasia
Uma visão geral resumindo a dinâmica de plaquetas, o complexo processo de conversão de plaquetas inativos em um tampão de plaquetas, é essencial EL 2 . Para complicar qualquer descrição verbal é o facto de, pelo menos, 193 301 proteínas e interacções estão envolvidos na dinâmica de plaquetas. A separação de dinâmica de plaquetas em três fases é útil a este respeito, mas é artificial: na verdade, cada fase é iniciada em rápida sucessão, e cada continua até que o gatilho para essa fase não está presente, então não há sobreposição.
Adesão
Formação de trombos em um endotélio intacto é impedida por óxido nítrico , prostaciclina , e CD39 .
As células endoteliais estão associadas ao colagénio subendotelial pelo factor de von Willebrand (vWF), que estas células produzem. VWF também é armazenada nos corpos de Weibel-Palade de células endoteliais e segregado constitutivamente para a corrente sanguínea. As plaquetas de vWF armazenar nos seus grânulos alfa.
Quando a camada endotelial é interrompido, colagénio e o vWF âncora plaquetas ao subendotélio. Plaquetas GP1b-IX-V receptor se liga com VWF; e receptor GPVI e integrina ligam α2β1 com colagénio.
Ativação

Inibição
O intactas endoteliais que revestem inibe a activação das plaquetas através da produção de óxido nítrico , endothelial- ADPase , e PGI 2 (prostaciclina). Endotelial-ADPase degrada o activador de plaquetas ADP .
Plaquetas descansam manter o cálcio activo efluxo através de uma AMP cíclico activadas bomba de cálcio. A concentração de cálcio intracelular determina estado de activação das plaquetas, assim como é o segundo mensageiro que as unidades de plaquetas mudança conformacional e desgranulação (ver abaixo). Endoteliais da prostaciclina liga-se a prostanóides receptores na superfície das plaquetas em repouso. Este evento estimula a acoplado Gs proteína para aumentar a adenilato-ciclase actividade e aumenta a produção de cAMP, promovendo ainda mais o efluxo de ccio e reduzindo a disponibilidade de cálcio intracelular por activação de plaquetas.
ADP sobre os outros se liga mão para receptores purinérgicos na superfície das plaquetas. Uma vez que o receptor purinérgico trombocítica P2Y12 é acoplado a Gi proteínas, ADP reduz a actividade da adenilato ciclase das plaquetas e produção de cAMP, conduzindo à acumulação de cálcio dentro das plaquetas por inactivação do AMPc bomba de efluxo de cálcio. Os outros-receptor de ADP P2Y1 casais a Gq que activa a fosfolipase C-beta 2 ( PLCB2 ), resultando em inositol 1,4,5-trisfosfato (IP3) geração e a libertação intracelular de cálcio mais. Isto induz a activação de plaquetas em conjunto. Endotelial ADPásica degrada ADP e impede que isso aconteça. Clopidogrel e medicamentos antiplaquetas relacionados também trabalhar como receptor purinérgico P2Y12 antagonistas .
Gatilho (indução)
Activação de plaquetas começa segundos após adesão ocorre. Ela é desencadeada quando colagénio dos subendotélio liga-se com os seus receptores ( GPVI de receptores de integrina e α2β1) sobre a plaquetas. GPVI está associada com a cadeia gama do receptor Fc e conduz através da activação de uma cascata de quinase tirosina, finalmente, para a activação de PLC-gama2 ( PLCG2 ) e mais libertação de cálcio.
O factor tecidular liga-se também ao factor VII no sangue, o que inicia a extrínseca de coagulação em cascata para aumentar trombina produção. A trombina é um activador de plaquetas poderoso, agindo através de Gq e G12. Estes são receptores acoplados à proteína G e em que se centram mediada por cálcio vias de sinalização dentro da plaqueta, superando o efluxo basal de cálcio. Famílias de três proteínas G (Gq, Gi, G12) operam em conjunto para a activação completa. A trombina também promove fibrina reforço secundário do tampão plaquetário. A activação de plaquetas em degranulates volta e liberta Factor V e fibrinogénio , potenciar a cascata de coagulação. Assim, na realidade, o processo de entupimento de plaquetas e coagulação estão a ocorrer simultaneamente em vez de sequencialmente, com cada induzir o outro para formar o trombo final de fibrina reticulado.
Componentes (consequências)
activação da GPIIb / IIIa
O colagénio mediada por GPVI sinalização aumenta a produção de plaquetas de tromboxano A2 (TXA2) e diminui a produção de prostaciclina . Isto ocorre através da alteração do fluxo metabólico de plaquetas do eicosanóide via de síntese, que envolve as enzimas fosfolipase A2 , a ciclo-oxigenase 1 , e tromboxano-A sintase . As plaquetas secretam tromboxano A2, que actua sobre próprios do plaquetas receptores de tromboxano na superfície das plaquetas (daqui a chamada "fora-de" mecanismo), e os de outras plaquetas. Estes receptores desencadear de sinalização intraplaquetário, que converte a GPIIb / IIIa receptores na sua forma activa para iniciar a agregação .
secreção granule
As plaquetas contêm grânulos densos , grânulos lambda e grânulos alfa . As plaquetas activadas segregam os conteúdos destes grânulos através dos seus sistemas canaliculares para o exterior. Simplesmente, ligado e plaquetas activadas desgranulam a libertação das plaquetas quimiotáticos agentes para atrair mais as plaquetas para o local da lesão endotelial. Características granulares:
- alfa grânulos alfa (grânulos) - contendo P-selectina , do factor 4 das plaquetas , factor de crescimento transformante-p1 , factor de crescimento derivado de plaquetas , fibronectina , B-tromboglobulina , vWF , de fibrinogénio e factores de coagulação V e XIII .
- δ grânulos (delta ou grânulos densos) - contendo o ADP ou o ATP , cálcio , e serotonina .
- y grânulos (grânulos de gama) - semelhantes para os lisossomas e conter várias enzimas hidrolíticas.
- X grânulos (grânulos lambda) - conteúdo envolvidos na reabsorção durante as fases posteriores de reparação vaso.
mudança morfologia
Tal como mostrado por citometria de fluxo e microscopia electrónica, o sinal mais sensível de activação, quando exposto às plaquetas utilizando ADP, são alterações morfológicas. Hiperpolarização mitocondrial é um evento chave em iniciar mudanças na morfologia. Aumento da concentração de cálcio intraplaquetário, estimulando a interacção entre o microtúbulo / actina complexo filamento. As mudanças contínuas na forma do unactivated ao plaquetas totalmente ativado é melhor visto em microscopia eletrônica de varredura. Três etapas ao longo deste caminho são nomeados início dendrítica , propagação início e propagação . A superfície das plaquetas não activadas parece muito semelhante à da superfície do cérebro, com uma aparência enrugada a partir de numerosas dobras superficiais para aumentar a área de superfície; dendrítica cedo , um polvo com vários braços e pernas; disseminação precoce , um ovo de fritura não cozido numa panela, o "gema" sendo o corpo central; ea propagação , um ovo frito cozido com um corpo central mais denso.
Estas alterações são todos provocada pela interacção do microtúbulo / actina complexo com a membrana celular das plaquetas e do sistema canalicular aberta (OCS), que é uma extensão e a invaginação da membrana que. Este complexo é executado apenas sob estas membranas e é o motor química que literalmente puxa o OCS invaginada para fora do interior da plaqueta, como o giro calças bolsos de dentro para fora, criando os dendritos. Este processo é semelhante ao mecanismo de contracção em uma célula muscular . Os OCS inteiras torna-se, assim, indistinguível da membrana de plaquetas inicial medida que se forma o "ovo frito". Este aumento dramático na área de superfície acontece com nenhum alongamento, nem a adição de fosfolipídios na membrana das plaquetas.
interacções de factores de plaquetas-coagulação: facilitação coagulação
A activação das plaquetas provoca a sua superfície de membrana para se tornar carregado negativamente. Uma das vias de sinalização voltas sobre scramblase , que se move com carga negativa fosfolidos a partir do interior para a superfície da membrana de plaquetas exterior. Estes fosfolípidos em seguida, ligar os TENase e protrombinase complexos, dois dos locais de interacção entre as plaquetas e a cascata de coagulação. Os iões de cálcio são essenciais para a ligação destes factores de coagulação.
Além de interagir com o vWF e fibrina, plaquetas interagir com trombina, os factores X, VA, VII, XI, IX, e protrombina a formação completa através da cascata de coagulação. Seis estudos sugeridos plaquetas expressar fator tecidual : O estudo mostra definitivas eles não o fazem. As plaquetas a partir de ratos foram conclusivamente demonstrado que a proteína do factor tecidular expresso e também provou-se que as plaquetas de rato transportam tanto o factor de tecido pré-ARNm e ARNm maduro.
Agregação
A agregação inicia minutos depois da activação, e ocorre como um resultado de ligar a GPIIb / IIIa do receptor, permitindo que estes receptores ligam-se a com vWF ou fibrinogénio . Há cerca de 60 000 destes receptores por plaqueta. Quando qualquer um ou mais de, pelo menos, nove receptores da superfície das plaquetas diferentes estão ligados durante a activação, as vias de sinalização intraplaquetário causar receptores GPIIb / IIIa existentes para alteração da forma - para enrolado linear - e, assim, tornar-se capaz de se ligar.
Uma vez que o fibrinogénio é uma proteína do tipo vareta, com nódulos em qualquer uma das extremidades capazes de se ligar a GPIIb / IIIa, plaquetas activadas com exposto da GPIIb / IIIa se pode ligar fibrinogénio ao agregado. GPIIb / IIIa pode também ainda âncora as plaquetas para subendotelial vWF para a estabilização estrutural adicional.
Classicamente, pensava-se que este foi o único mecanismo envolvido na agregação, mas três novos mecanismos têm sido identificados, que pode iniciar a agregação, dependendo da velocidade de fluxo sanguíneo (isto é, gama de cisalhamento).
reparação ferida
O coágulo de sangue é apenas uma solução temporária a hemorragia parada; reparação de tecidos é necessária. Pequenas interrupções no endotélio são tratados por mecanismos fisiológicos; grandes interrupções por parte do cirurgião de trauma. A fibrina é dissolvido lentamente pela enzima fibrinolítica, plasmina, e as plaquetas são clarificados por fagocitose .
Função imune
As plaquetas têm papel central na imunidade inata, iniciando e participando em vários processos inflamatórios, patógenos directamente ligação e mesmo destruindo-as. Este suporte de dados clínicos que mostram que muitas pessoas com infecções bacterianas ou virais graves têm trombocitopenia, reduzindo assim a sua contribuição para a inflamação. Também agregados de plaquetas-leucócitos (PLAs) encontrada em circulação são típicos em sepsia ou doença inflamatória do intestino , mostrando a conexão entre os trombócitos e células imunitárias sensu stricto .
Immunothrombosis
Como hemostasia é uma função básica de trombócitos em mamíferos, ele também tem seus usos na possível confinamento infecção. No caso de lesão, plaquetas, em conjunto com a cascata da coagulação, formar a primeira linha de defesa através da formação de um coágulo de sangue. Assim, a hemostasia e a defesa do hospedeiro foram entrelaçados em evolução. Por exemplo, no límulo ( fóssil vivo estimados em mais de 400 milhões de anos), o único tipo de células de sangue, o amebócito , facilita tanto a função hemostática e o encapsulamento e a fagocitose de agentes patogénicos através de exocitose de grulos intracelulares que contêm bactericidas moléculas de defesa. A coagulação do sangue suporta a função imune, aprisionando as bactérias patogénicas dentro.
Embora a trombose, a coagulação do sangue em vasos sanguíneos intactos, é geralmente vista como uma resposta imunitária patológica, que conduz à obturação do lúmen do vaso sanguíneo e a subsequente danos no tecido hipóxico, em alguns casos, trombose dirigida, chamado immunothrombosis, pode controlar localmente a propagação do infecção. A trombose é dirigida em concordância de plaquetas, neutrófilos e monócitos . O processo é iniciado quer por células imunitárias sensu stricto através da activação dos seus receptores de reconhecimento de padrões (PRRs), ou de plaquetas por ligação-bacteriana. As plaquetas podem ligar-se a bactérias, quer directamente através PRRs trombocítica e proteínas de superfície bacterianas, ou por meio de proteínas do plasma que se ligam tanto a plaquetas e bactérias. Os monócitos respondem a bacterianas padrões associados de agentes patogénicos moleculares (PAMP), ou padrões moleculares associados a danos (amortece) através da activação da via extrínseca da coagulação. Os neutrófilos facilitar a coagulação do sangue por NETosis . Por sua vez, as plaquetas facilitar NETosis neutrófilos. NET se ligar ao factor de tecido, ligando os centros de coagulação para o local da infecção. Eles também activar a via de coagulação intrínseca, fornecendo a sua superfície carregada negativamente para o factor XII. Outras secreções de neutrófilos, tais como as enzimas proteolíticas, que clivam inibidores da coagulação, também reforçar o processo.
Em caso de desequilíbrio em todo o regulamento de immunothrombosis, este processo pode rapidamente tornar-se aberrante. Defeitos reguladoras em immunothrombosis são suspeitos de ser importante factor na causa da trombose patológica em muitas formas, tais como coagulação intravascular disseminada (DIC) ou trombose venosa profunda . DIC em sépsis é um exemplo de ambos processo de coagulação desregulada bem como a resposta inflamatória sistémica indevida resultando na multiplicidade de microtrombos de composição semelhante à que em immunothrombosis fisiológico - fibrina, plaquetas, neutrilos e redes.
Inflamação
As plaquetas são rapidamente deslocado para locais de lesão ou infecção, e potencialmente modular processos inflamatórios através da interacção com leucócitos e através da secreção de citoquinas , quimioquinas e outros mediadores inflamatórios. As plaquetas também secretam o factor de crescimento derivado de plaquetas (PDGF).
As plaquetas modular neutrófilos através da formação de agregados de plaquetas-leucócitos (PLAs). Estes formação induzir a produção regulada positivamente de αmβ2 ( Mac-1 ) integrina em neutrófilos. Interacção com PLAs também induzem a desgranulação e aumento da fagocitose dos neutrófilos. As plaquetas também são a maior fonte de solúvel de CD40L que induz a produção de espécies reactivas de oxigénio (ROS) e expressão supra-regular de moléculas de adesão, tais como a E-selectina, ICAM-1 e VCAM-1, em neutrófilos, activa macrófagos e activa a resposta citotóxica in Os linfócitos T e B.
Recentemente, o dogma de que as plaquetas de mamífero que faltam núcleo é incapaz de locomoção autónomos foi quebrado. Na verdade, as plaquetas são catadores ativos, escalar paredes dos vasos sanguíneos e reorganizando o trombo. Eles são capazes de reconhecer e aderir a muitas superfícies, incluindo bactérias. Eles são ainda capaz de envolver totalmente los no seu sistema canalicular aberta (OCP), levando a denominação proposta do processo ser "covercytosis", em vez de fagocitose, como OCS é meramente uma invaginação da membrana plasmática externa. Estes feixes-bactérias de plaquetas são, então, usado como uma plataforma de interacção para os neutrófilos, que destroem as bactérias usando o NETosis e fagocitose.
As plaquetas também participam em doenças inflamatórias crónicas, tais como artrite reumatóide ou sinovite. As plaquetas são activadas por receptor de colagénio glicoproteína IV (GPVI). Microvesículas plaquetas pró-inflamatórias desencadear secreção de citoquinas constante da vizinha do tipo fibroblasto sinoviócitos , mais proeminentemente IL-6 e IL-8 . Dano inflamatório para circundante matriz extracelular revela continuamente mais colagénio, mantendo a produção microvesículas.
Imunidade adaptativa
As plaquetas activadas são capazes de participar na imunidade adaptativa, que interage com os anticorpos . Eles são capazes de especificamente se ligam a IgG através de Fc? RIIA , receptor para o fragmento constante (Fc) de IgG. Quando activado e ligado a IgG opsonizado bactérias, as plaquetas subsequentemente libertar espécies reactivas de oxigénio (ROS), os péptidos antimicrobianos defensinas, kinocidins, e proteases, matando as bactérias directamente. As plaquetas também pró-inflamatória secretam e mediadores pró-coagulantes, tais como polifosfatos inorgânicos ou factor de plaquetas 4 (PF4), inato de ligação e as respostas imunitárias adaptativas.
Sinais e sintomas de distúrbios
Hemorragia espontânea e excessiva pode ocorrer por causa de doenças plaquetárias. Esta hemorragia pode ser causada por números insuficientes de plaquetas, plaquetas disfuncionais, ou números muito excessivas de plaquetas: mais de 1,0 milhões / microlitro. (Os números excessivos criar uma deficiência relativa de factor de von Willebrand devido a sequestro.)
Pode-se obter uma pista sobre se o sangramento é devido a um distúrbio plaquetária ou um distúrbio fator de coagulação pelas características e localização do sangramento. Todas as seguintes sugerem sangramento de plaquetas, coagulação não sangramento: a hemorragia a partir de uma pele cortada, tais como uma máquina de barbear entalhe é rápido e excessivo, mas pode ser controlada por pressão; hemorragia espontânea na pele que provoca uma mancha púrpura nomeado pelo seu tamanho: petéquias , púrpura , equimoses ; sangramento para dentro das membranas mucosas que causam sangramento das gengivas, sangramento do nariz, e hemorragia gastrointestinal; menorragia; e sangramento intra e intracraniana.
Um número excessivo de plaquetas e / ou plaquetas normais respondem às paredes dos vasos anormais, pode resultar em trombose venosa e a trombose arterial . Os sintomas dependem do local da trombose.
Testes de função
Tempo de hemorragia
Desenvolvido por Duke em 1910 e que leva seu nome, é medido o tempo para estancar a hemorragia de uma ferida padronizada no lóbulo da orelha que é apagados a cada 30 segundos. Normal foi de menos de 3 minutos. técnicas mais modernos são agora usados. Um tempo de hemorragia normais reflete números de plaquetas suficientes e função mais microvascular normal.
Multipanel agregometria eléctrodo múltipla
No Multiplate analisador, o sangue total anticoagulado é misturado com solução salina e um agonista de plaquetas numa cuvete de uso único com dois pares de eléctrodos. O aumento na impedcia entre os eltrodos como plaquetas agregam para eles, é medida e visualizada como uma curva.
PFA-100
O PFA-100 (função plaquetária Ensaio-100) é um sistema para análise da função das plaquetas em sangue total citrado, que é aspirado através de um cartucho descartável, que contém uma abertura, dentro de uma membrana revestida quer com colagénio e adrenalina ou colagénio e ADP. Estes agonistas de induzir a adesão de plaquetas, activação e agregação, que conduz a uma rápida oclusão da abertura e a cessação do fluxo de sangue chamado de tempo de fecho (CT). Uma elevada CT com IPE e colagénio podem indicar defeitos intrínsecos, tais como a doença de von Willebrand , uremia , ou inibidores de plaquetas em circulação. O seguimento teste envolvendo o colagénio e ADP é utilizado para indicar se o CT anormal com colagénio e EPI foi causada pelos efeitos da acetil ácido sulfossalicílico (aspirina) ou medicamentos contendo inibidores.
Disorders
Adaptado de:
Os três grandes categorias de distúrbios de plaquetas são "não é suficiente"; "disfuncional"; e "muitos".
trombocitopenia
- Trombocitopenias imunitário (ITP) - anteriormente conhecidos como púrpura trombocitopénica imune e púrpura trombocitopénica idiopática
- esplenomegalia
- trombocitopenia familial
- Quimioterapia
- babesiose
- Dengue
- Onyalai
- Púrpura trombocitopénica trombótica
- síndrome HELLP
- Síndrome hemolítico-urêmica
- Induzida por drogas púrpura trombocitopénica (cinco fármacos conhecidos - o mais problemático é a trombocitopenia induzida pela heparina (HIT)
- gravidez associada
- alloimmune Neonatal associado
- Anemia aplástica
- transfusão de associados
- pseudoplaquetopenia
- púrpura trombocitopênica idiopática
- A síndrome de Gilbert
alteração da função plaquetária
- congênito
- Distúrbios de aderência
- Desordens de activação
- Distúrbios da quantidade de grânulos ou liberação
- síndrome Hermansky-Pudlak
- síndrome de plaquetas cinza
- defeito receptor de ADP
- actividade ciclooxigenase diminuiu
- defeitos pool de armazenamento, adquiridas ou congênitas
- Distúrbios de agregação
- Adquirido
- Distúrbios de aderência
- hemoglobinúria paroxística nocturna
- Asma
- Tríade de Samter (aspirina-exacerbada doença respiratória / DREA)
- Câncer
- Malária
- actividade ciclooxigenase diminuiu
- Distúrbios de aderência
Trombocitose e trombocitemia
- reativo
- A infecção crônica
- Inflamação crônica
- Malignidade
- Hipoesplenismo (pós-esplenectomia)
- Falta de ferro
- perda aguda de sangue
- Neoplasias mieloproliferativas - plaquetas são ambos elevados e activada
- Associado a outras neoplasias mielóides
- congênito
drogas que afetam
drogas anti-inflamatórias
Alguns fármacos utilizados para tratar a inflamação tem o efeito secundário indesejado de suprimir a função normal das plaquetas. Estas são as drogas não esteróides anti-inflamatórias (NSAIDs). Aspirina irreversivelmente destrói a função plaquetária por inibição da ciclo-oxigenase -1 (COX1), e, portanto, a hemostase normal. As plaquetas resultantes são incapazes de produzir novas ciclooxigenase porque eles não têm DNA. Função plaquetária normal não retornará até o uso de aspirina cessou e suficiente das plaquetas afetados foram substituídos por novos, o que pode levar mais de uma semana. Ibuprofeno , outro AINE , não têm um tal efeito de longa duração, com a função das plaquetas geralmente voltar dentro de 24 horas, e tomando ibuprofeno antes impede aspirina os efeitos irreversíveis da aspirina.
As drogas que suprimem a função plaquetária
Estes fármacos são utilizados para prevenir a formação de trombos.
agentes orais
Drogas que estimulam a produção de plaquetas
agentes intravenosos
- abciximab ,
- eptifibatide
- tirofiban
- Outros oprelvecina , romiplostim , eltrombopag , argatroban
A terapia com plaquetas
Transfusão
indicações
A transfusão de plaquetas é mais frequentemente usado para corrigir as contagens anormalmente baixas de plaquetas, para prevenir a ocorrência de hemorragias espontâneas (tipicamente a contagem inferior a 10 x 10 9 / L) ou em antecipação a procedimentos médicos que envolvem necessariamente alguma hemorragia. Por exemplo, em pacientes submetidos a cirurgia , um nível abaixo de 50 x 10 9 / L está associada a hemorragia cirúrgica anormal, e anestésicos regionais procedimentos tais como epidurais são evitados para níveis abaixo de 80 x 10 9 / L. As plaquetas também pode ser utilizado quando a contagem de plaquetas é normal, mas as plaquetas são disfuncionais, por exemplo, quando um indivíduo está a tomar aspirina ou clopidogrel . Finalmente, as plaquetas podem ser transfundido como parte de um protocolo de transfusão maciço , em que os três principais componentes do sangue (glóbulos vermelhos, plasma e plaquetas) são transfundidas para tratar hemorragia grave. A transfusão de plaquetas é contra-indicada em trombótica púrpura trombocitopénica (TTP), à medida que alimenta a coagulopatia .
Coleção
As plaquetas são ou isolado a partir de unidades recolhidos de sangue total e reunidos para fazer uma dose terapêutica, ou recolhidas por aférese plaquetária : sangue é tomada a partir do dador, passados através de um dispositivo que remove as plaquetas, e o restante é devolvido ao dador numa circuito fechado. O padrão da indústria é de plaquetas a ser testado para as bactérias antes da transfusão para evitar reacções séptico, que pode ser fatal. Recentemente, os padrões da indústria AABB para Bancos de Sangue e Transfusão de Serviços (5.1.5.1) tem permitido para o uso de tecnologia de redução de patógenos como uma alternativa para rastreios bacterianas em plaquetas.
Agrupados plaquetas de sangue total, às vezes chamados “aleatórios” plaquetas, são separados por um dos dois métodos. Nos EUA, uma unidade de sangue total é colocado em uma grande centrífuga em que é referido como uma “rotação suave.” Nessas configurações, as plaquetas permanecem suspensas no plasma. O plasma rico em plaquetas (PRP) é removida das células vermelhas e, em seguida centrifugou-se a fixação de um mais rápido para colheita das plaquetas do plasma. Em outras regiões do mundo, a unidade de sangue total é centrifugada utilizando as definições que causa que as plaquetas se tornam suspensas no “ buffy coat ” camada, que inclui as plaquetas e as células brancas do sangue. O “buffy coat” é isolado num saco estéril, suspenso numa pequena quantidade de células vermelhas do sangue e do plasma, em seguida, centrifugou-se novamente para separar as plaquetas e plasma das células vermelhas e brancas do sangue. Independentemente do método de preparação inicial, múltiplas doações podem ser combinados em um recipiente utilizando um dispositivo de ligação estéril para a fabricação de um único produto com a dose terapêutica desejada.
Aférese plaquetas são recolhidas utilizando um dispositivo mecânico que extrai o sangue do doador e centrifuga o sangue foi recolhido de forma a separar as plaquetas e outros componentes a serem recolhidos. O sangue restante é devolvido ao dador. A vantagem deste método é que uma única doação fornece, pelo menos, uma dose terapêutica, em oposição com as múltiplas doações de plaquetas de sangue total. Isto significa que um destinatário não está exposta ao maior número de doadores diferentes e possui menos risco de doença transmitida por transfusão e outras complicações. Às vezes uma pessoa, como um câncer paciente que requer transfusões de rotina de plaquetas receberá doações repetidas de um doador específico para minimizar ainda mais o risco. Redução de agentes patogénicos de plaquetas utilizando, por exemplo, a riboflavina e tratamentos de luz UV também pode ser realizada para reduzir a carga infecciosa de agentes patogénicos contidos nos produtos de sangue doado, reduzindo assim o risco de transmissão de doenças transmitidas transfusão. Um outro processo de tratamento fotoquímico utilizando amotosaleno e luz UVA tem sido desenvolvido para a inactivação de vírus, bactérias, parasitas, e leucócitos que podem contaminar os componentes sanguíneos destinados a transfusão. Além disso, as plaquetas por aférese tendem a conter menos células vermelhas do sangue contaminantes, porque o método de recolha é mais eficiente do que a centrifugação “rotação suave” em isolar o componente sanguíneo desejado.
Armazenamento
As plaquetas coletadas por qualquer método têm uma vida útil muito curta, geralmente de cinco dias. Isso resulta em problemas freqüentes com pouca oferta, como testando as doações muitas vezes requer até um dia inteiro. Como não existem soluções conservantes eficazes para plaquetas, eles perdem a potência de forma rápida e são melhores quando fresco.
As plaquetas são armazenadas sob agitação constante a 20-24 ° C (68-75,2 ° F). As unidades não pode ser refrigerado, pois isso faz com que as plaquetas a forma mudança e função perder. Armazenamento à temperatura ambiente fornece um ambiente em que todas as bactérias que são introduzidas ao componente do sangue durante o processo de recolha pode proliferar e subsequentemente causa bacteriémia no paciente. Regulamentos estão em vigor nos Estados Unidos que exigem produtos a serem testados para a presença de contaminação bacteriana antes da transfusão.
Entrega aos destinatários
As plaquetas não necessitam de pertencer ao mesmo grupo sanguíneo ABO como o destinatário ou ser cruzada com garantir compatibilidade imunológica entre dador e receptor, a menos que eles contêm uma quantidade significativa de células vermelhas do sangue (RBC). A presença de RBCs confere uma cor laranja-avermelhada ao produto, e é geralmente associada com plaquetas de sangue total. Um esforço é feito às vezes às plaquetas específicos do tipo de problema, mas isso não é crítica, pois é com hemácias.
Antes de emitir plaquetas ao destinatário, eles podem ser irradiados para evitar enxerto transfusão-associado versus hospedeiro ou podem ser lavadas para remover o plasma se indicado.
A mudança na contagem de plaquetas do receptor após a transfusão é denominado o "incremento" e é calculado subtraindo-se a pré-transfusão de plaquetas a partir do pós-transfusão de plaquetas. Muitos fatores afetam o incremento incluindo o tamanho do destinatário, órgão, o número de plaquetas transfundidas, e características clínicas que podem causar destruição prematura das plaquetas transfundidas. Quando os destinatários não conseguem demonstrar um aumento pós-transfusão adequada, isto é denominado de plaquetas transfusão refractariedade .
As plaquetas, quer derivadas de aférese ou aleatório-doador, pode ser processado através de uma redução do volume de processo. Neste processo, as plaquetas são centrifugados numa centrífuga e o excesso de plasma é removido, deixando 10 a 100 ml de concentrado de plaquetas. Tais plaquetas reduzida de volume são normalmente transfundido apenas para pacientes pediátricos e neonatais, quando um grande volume de plasma poderia sobrecarregar pequeno sistema circulatório da criança. O volume de plasma mais baixa também reduz a probabilidade de uma reacção adversa à transfusão de proteínas plasmáticas. Volume reduzido plaquetas têm uma vida útil de apenas quatro horas.
terapia ferida
As plaquetas libertar factor de crescimento derivado de plaquetas (PDGF), um potente quimiotáctica agente; e TGF beta , que estimula a deposição de matriz extracelular ; factor de crescimento de fibroblastos , insulina-like growth factor 1 , derivado de plaquetas do factor de crescimento epidérmico , e factor de crescimento endotelial vascular . A aplicação local desses factores num aumento das concentrações através de Plasma Rico em Plaquetas (PRP) é usado como um adjuvante na cicatrização de feridas.
Outros animais
Em vez de ter plaquetas, vertebrados não-mamíferos têm trombócitos nucleadas, que se assemelham linfócitos B na morfologia. Eles agregam em resposta a trombina, mas não para ADP, serotonina, nem adrenalina, como plaquetas fazer.
História
- George Gulliver em 1841 desenhou imagens de plaquetas usando o microscópio de lente twin (composto) inventado em 1830 por Joseph Jackson Lister . Isso melhorou resolução microscópio suficiente para torná-lo possível ver plaquetas, pela primeira vez.
- William Addison em 1842 desenhou um coágulo de plaquetas-fibrina.
- Lionel Beale em 1864 foi o primeiro a publicar um desenho mostrando plaquetas.
- Max Schultze em 1865 descreveu o que ele chamou de "esférulas", que ele observou eram muito menores do que as células vermelhas do sangue, ocasionalmente agregadas, e às vezes eram encontrados em colecções de material de fibrina.
- Giulio Bizzozero em 1882 estudaram o sangue de anfíbios microscopicamente in vivo . Ele nomeou esférulas de Schultze (It.) Piastrine : pequenas placas.
- William Osler observado plaquetas e, em palestras publicados, em 1886, os chamou um terceiro corpúsculo e um sangue de placa ; e os descreveu como "um disco protoplasmic incolor".
- James Wright analisou sangue esfregaços usando a mancha nomeado para ele, e usado o termo placas em sua publicação 1906, mas mudou de plaquetas em sua publicação 1910 que se tornou o termo universalmente aceito.
O termo thrombocyte (célula coágulo) entrou em uso no início de 1900 e é por vezes utilizado como sinônimo de plaquetas; mas não em geral na literatura científica, exceto como uma palavra raiz para outros termos relacionados com as plaquetas (por exemplo trombocitopenia ou seja baixa de plaquetas). O termo trombócitos é adequado para células mononucleares encontradas no sangue de vertebrados não-mamíferos: eles são o equivalente funcional das plaquetas, mas circula como células intactas, em vez de fragmentos citoplasmáticos de megacariócitos de medula óssea.
Nalguns contextos, a palavra trombo é utilizado alternadamente com o termo coágulo , independentemente da sua composição (branco, vermelho, ou misturado). Noutros contextos, é usado para contrastar um normal a partir de um coágulo anormal: trombo decorre da hemostase fisiológica, trombose resulta de uma quantidade excessiva patológico e de coágulo. Num terceiro contexto, é utilizado para contrastar o resultado do processo: trombo é o resultado, trombose é o processo.
Referências
links externos
-
Vídeo resumindo a dinâmica de plaquetas (
 página irá reproduzir áudio quando carregado)
página irá reproduzir áudio quando carregado)






