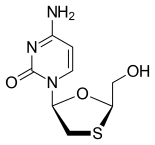
Lamivudina - Lamivudine
 | |
| Dados clínicos | |
|---|---|
| Nomes comerciais | Epivir, Epivir-HBV, Zeffix, outros |
| Outros nomes | (-) - L-2 ′, 3′-didesoxi-3′-tiacitidina |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a696011 |
| Dados de licença | |
Categoria de gravidez |
|
| Vias de administração |
Pela boca |
| Código ATC | |
| Status legal | |
| Status legal | |
| Dados farmacocinéticos | |
| Biodisponibilidade | 86% |
| Ligação proteica | Menos de 36% |
| Meia-vida de eliminação | 5 a 7 horas |
| Excreção | Rim (cerca de 70%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| Ligante PDB | |
| Painel CompTox ( EPA ) | |
| ECHA InfoCard |
100.132.250 |
| Dados químicos e físicos | |
| Fórmula | C 8 H 11 N 3 O 3 S |
| Massa molar | 229,25 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
|
| |
A lamivudina , comumente chamada de 3TC , é um medicamento anti - retroviral usado para prevenir e tratar o HIV / AIDS . Também é usado para tratar a hepatite B crônica quando outras opções não são possíveis. É eficaz contra o HIV-1 e HIV-2 . É normalmente usado em combinação com outros antirretrovirais, como zidovudina e abacavir . A lamivudina pode ser incluída como parte da prevenção pós-exposição em pessoas que foram potencialmente expostas ao HIV. A lamivudina é administrada por via oral na forma de líquido ou comprimido.
Os efeitos colaterais comuns incluem náusea, diarreia, dores de cabeça, cansaço e tosse. Os efeitos colaterais graves incluem doença hepática , acidose láctica e agravamento da hepatite B entre os já infectados. É seguro para pessoas com mais de três meses de idade e pode ser usado durante a gravidez . O medicamento pode ser tomado com ou sem alimentos. A lamivudina é um inibidor da transcriptase reversa de nucleosídeos e atua bloqueando a transcriptase reversa do HIV e a polimerase do vírus da hepatite B.
A lamivudina foi patenteada em 1995 e aprovada para uso nos Estados Unidos em 1995. Está na Lista de Medicamentos Essenciais da Organização Mundial de Saúde . Ele está disponível como um medicamento genérico .
Usos médicos
A lamivudina (Epivir) é indicada em combinação com outros medicamentos antirretrovirais para o tratamento da infecção pelo HIV-1. A lamivudina (Epivir HBV) é indicada para o tratamento da infecção crônica pelo vírus da hepatite B associada a evidências de replicação viral da hepatite B e inflamação ativa do fígado.
A lamivudina tem sido usada para o tratamento da hepatite B crônica em uma dose mais baixa do que para o tratamento do HIV / AIDS . Ele melhora a soroconversão de hepatite B positiva para antígeno e também melhora o estadiamento histológico do fígado. O uso prolongado de lamivudina leva ao surgimento de um mutante do vírus da hepatite B resistente (YMDD). Apesar disso, a lamivudina ainda é amplamente utilizada por ser bem tolerada.
Resistência
No HIV, o alto nível de resistência está associado à mutação M184V / I no gene da transcriptase reversa, conforme relatado pelo grupo de Raymond Schinazi na Emory University . A GlaxoSmithKline afirmou que a mutação M184V reduz a "aptidão viral", devido à descoberta de que o tratamento continuado com lamivudina faz com que a carga viral do HIV se recupere, mas em um nível muito mais baixo, e que a retirada da lamivudina resulta em um rebote de carga viral mais alto com rápida perda de a mutação M184V; GSK, portanto, argumentou que pode haver benefício em continuar o tratamento com lamivudina, mesmo na presença de alto nível de resistência, porque o vírus resistente é "menos apto". O estudo COLATE sugeriu que não há benefício em continuar o tratamento com lamivudina em pacientes com resistência à lamivudina. Uma explicação melhor para os dados é que a lamivudina continua a ter um efeito antiviral parcial, mesmo na presença da mutação M184V.
Na hepatite B, a resistência à lamivudina foi descrita pela primeira vez no locus YMDD ( tirosina - metionina - aspartato - aspartato ) do gene da transcriptase reversa do HBV. O gene da transcriptase reversa do HBV tem 344 aminoácidos de comprimento e ocupa os códons 349 a 692 no genoma viral. As mutações de resistência mais comumente encontradas são M204V / I / S. A mudança na sequência de aminoácidos de YMDD para YIDD resulta em uma redução de 3,2 vezes na taxa de erro da transcriptase reversa, o que se correlaciona com uma desvantagem de crescimento significativa do vírus. Outras mutações de resistência são L80V / I, V173L e L180M.
Efeitos colaterais
- Os efeitos colaterais menores podem incluir náuseas , fadiga , dores de cabeça , diarreia , tosse e congestão nasal .
- Não prescrever lamivudina / zidovudina, abacavir / lamivudina ou abacavir / lamivudina / zidovudina a pacientes em tratamento com emtricitabina .
- O uso prolongado de lamivudina pode desencadear um mutante do vírus da hepatite B resistente (YMDD).
- Mulheres infectadas com HIV ou VHB que tomam lamivudina são alertadas para interromper a amamentação, pois isso coloca o bebê em risco de transmissão do HIV e efeitos colaterais da medicação.
- Pacientes que estão infectados com HIV e HCV e estão tomando interferon e lamivudina podem sofrer danos ao fígado.
- A droga pode desencadear uma resposta inflamatória a infecções oportunistas (por exemplo, complexo Mycobacterium avium [MAC], M. tuberculosis , citomegalovírus [CMV], Pneumocystis jirovecii [anteriormente P. carinii).
- Foram relatadas doenças autoimunes e os sintomas podem ocorrer muitos meses após o início da terapia anti- retroviral.
- Utilizar com cuidado para pacientes com função renal comprometida e não prescrever este tratamento para pacientes com função hepática comprometida .
Mecanismo de ação
A lamivudina é um análogo da citidina . Pode inibir ambos os tipos (1 e 2) de VIH transcriptase reversa e também a transcriptase reversa de vírus da hepatite B . É fosforilado em metabólitos ativos que competem pela incorporação no DNA viral. Eles inibem a enzima transcriptase reversa do HIV competitivamente e atuam como um terminador da cadeia da síntese de DNA. A falta de um grupo 3'-OH no análogo de nucleosídeo incorporado evita a formação da ligação fosfodiéster 5 'a 3' essencial para o alongamento da cadeia de DNA e, portanto, o crescimento do DNA viral é interrompido.
A lamivudina é administrada por via oral e é rapidamente absorvida com uma biodisponibilidade de mais de 80%. Algumas pesquisas sugerem que a lamivudina pode atravessar a barreira hematoencefálica . A lamivudina é freqüentemente administrada em combinação com a zidovudina , com a qual é altamente sinérgica. O tratamento com lamivudina demonstrou restaurar a sensibilidade à zidovudina do HIV previamente resistente. A lamivudina não mostrou evidência de carcinogenicidade ou mutagenicidade em estudos in vivo em camundongos e ratos em doses de 10 a 58 vezes as usadas em humanos.
Tem meia-vida de 5–7 horas em adultos e 2 horas em crianças infectadas pelo HIV.
História
O BCH-189 racêmico (a forma menos é conhecida como lamivudina) foi inventado por Bernard Belleau enquanto trabalhava na Universidade McGill e Paul Nguyen-Ba nos laboratórios IAF BioChem International, Inc. sediados em Montreal em 1988 e o enantiômero negativo isolado em 1989 As amostras foram enviadas primeiro para Yung-Chi Cheng, da Universidade de Yale, para estudo de sua toxicidade. Quando usado em combinação com o AZT, ele descobriu que a forma negativa da lamivudina reduzia os efeitos colaterais e aumentava a eficiência do medicamento na inibição da transcriptase reversa. A combinação de lamivudina e AZT aumentou a eficiência na inibição de uma enzima que o HIV usa para reproduzir seu material genético. Como resultado, a lamivudina foi identificada como um agente menos tóxico para o DNA da mitocôndria do que outras drogas retrovirais .
A lamivudina foi aprovada pela Food and Drug Administration (FDA) em 17 de novembro de 1995 para uso com zidovudina (AZT) e novamente em 2002 como medicamento administrado uma vez ao dia. Ele está na Lista de Medicamentos Essenciais da Organização Mundial da Saúde , os medicamentos mais seguros e eficazes necessários em um sistema de saúde .
Formulações
- Comprimidos Epivir (GlaxoSmithKline; EUA e Reino Unido) para o tratamento do HIV
- Comprimidos de Epivir-HBV (GlaxoSmithKline; apenas nos EUA) para o tratamento da hepatite B
- Comprimidos Zeffix (GlaxoSmithKline; apenas no Reino Unido) para o tratamento da hepatite B
- Comprimidos 3TC (GlaxoSmithKline; África do Sul) para o tratamento do HIV
- A lamivudina está disponível em combinações de dose fixa com outros medicamentos para HIV, como:
- Lamivudina / zidovudina (com zidovudina )
- Abacavir / lamivudina (com abacavir )
- Abacavir / lamivudina / zidovudina (com zidovudina e abacavir)
Referências
links externos
- "Lamivudina" . Portal de informações sobre medicamentos . Biblioteca Nacional de Medicina dos EUA.
