níquel -Nickel
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Níquel | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aparência | brilhante, metálico e prateado com um tom dourado | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atômico padrão A r °(Ni) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Níquel na tabela periódica | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número atômico ( Z ) | 28 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo | grupo 10 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Período | período 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloquear | bloco d | |||||||||||||||||||||||||||||||||||||||||||||||||||
| configuração eletrônica | [ Ar ] 3d 8 4s 2 ou [Ar] 3d 9 4s 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elétrons por camada | 2, 8, 16, 2 ou 2, 8, 17, 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase em STP | sólido | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 1728 K (1455 °C, 2651 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 3003 K (2730 °C, 4946 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidade (perto de rt ) | 8,908 g/ cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| quando líquido (em mp ) | 7,81 g/ cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusão | 17,48 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor da vaporização | 379 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade térmica molar | 26,07 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||
Pressão de vapor
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidação | −2, −1, 0, +1, +2 , +3, +4 (um óxido levemente básico ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Eletro-negatividade | Escala de Pauling: 1,91 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| energias de ionização | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico | empírico: 124h | |||||||||||||||||||||||||||||||||||||||||||||||||||
| raio covalente | 124±16h | |||||||||||||||||||||||||||||||||||||||||||||||||||
| raio de Van der Waals | 163h | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Linhas espectrais de níquel | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Outras propriedades | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ocorrência natural | primordial | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Estrutura de cristal | Cúbico de Face (FCC) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som haste fina | 4900 m/s (à temperatura ambiente ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansão térmica | 13,4 µm/(m⋅K) (a 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 90,9 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | 69,3 nΩ⋅m (a 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenação magnética | ferromagnético | |||||||||||||||||||||||||||||||||||||||||||||||||||
| módulo de Young | 200 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| módulo de cisalhamento | 76 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| módulo de massa | 180 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| razão de Poisson | 0,31 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| dureza de Mohs | 4.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Vickers | 638 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 667–1600 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Número CAS | 7440-02-0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| História | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Descoberta e primeiro isolamento | Axel Fredrik Cronstedt (1751) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| isótopos de níquel | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
O níquel é um elemento químico com símbolo Ni e número atômico 28. É um metal lustroso branco-prateado com um leve tom dourado. O níquel é um metal de transição duro e dúctil . O níquel puro é quimicamente reativo, mas peças grandes demoram a reagir com o ar em condições padrão porque uma camada de passivação de óxido de níquel se forma na superfície, o que evita mais corrosão. Mesmo assim, o níquel nativo puro é encontrado na crosta terrestre apenas em pequenas quantidades, geralmente em rochas ultramáficas e no interior de meteoritos maiores de níquel-ferro que não foram expostos ao oxigênio quando estavam fora da atmosfera terrestre.
O níquel meteórico é encontrado em combinação com o ferro , um reflexo da origem desses elementos como os principais produtos finais da nucleossíntese da supernova . Acredita-se que uma mistura de ferro-níquel componha os núcleos externo e interno da Terra .
O uso de níquel (como liga natural de níquel-ferro meteórico ) remonta a 3500 aC. O níquel foi isolado e classificado pela primeira vez como um elemento em 1751 por Axel Fredrik Cronstedt , que inicialmente confundiu o minério com um mineral de cobre , nas minas de cobalto de Los, Hälsingland, Suécia . O nome do elemento vem de um sprite travesso da mitologia mineira alemã, Nickel (semelhante ao Old Nick ), que personificava o fato de que os minérios de cobre-níquel resistiam ao refinamento em cobre. Uma fonte economicamente importante de níquel é o minério de ferro limonita , que geralmente contém 1 a 2% de níquel. Outros minerais importantes de minério de níquel incluem pentlandita e uma mistura de silicatos naturais ricos em Ni, conhecida como garnierita . Os principais locais de produção incluem a região de Sudbury , Canadá (que se acredita ser de origem meteórica ), Nova Caledônia no Pacífico e Norilsk , Rússia .
O níquel é um dos quatro elementos (os outros são ferro , cobalto e gadolínio ) que são ferromagnéticos em temperatura ambiente. Os ímãs permanentes de Alnico baseados parcialmente em níquel são de resistência intermediária entre os ímãs permanentes à base de ferro e os ímãs de terras raras . O metal é usado principalmente em ligas e revestimentos resistentes à corrosão. Cerca de 68% da produção mundial é utilizada em aço inoxidável . Outros 10% são usados para ligas à base de níquel e cobre, 9% para revestimento, 7% para ligas de aço, 3% em fundições e 4% em outras aplicações, como em baterias recarregáveis, inclusive em veículos elétricos ( EVs). O níquel é amplamente utilizado em moedas , embora os objetos banhados a níquel às vezes provoquem alergia ao níquel . Como composto, o níquel tem vários usos de nicho na fabricação de produtos químicos, como catalisador para hidrogenação , cátodos para baterias recarregáveis, pigmentos e tratamentos de superfícies metálicas. O níquel é um nutriente essencial para alguns microorganismos e plantas que possuem enzimas com níquel como sítio ativo .
Propriedades
Propriedades atômicas e físicas

O níquel é um metal branco prateado com um leve tom dourado que requer alto polimento. É um dos quatro elementos que são ferromagnéticos à temperatura ambiente ou próximo dela; os outros são ferro, cobalto e gadolínio . Sua temperatura Curie é de 355 °C (671 °F), o que significa que o níquel a granel não é magnético acima dessa temperatura. A célula unitária do níquel é um cubo de face centrada com o parâmetro de rede de 0,352 nm, dando um raio atômico de 0,124 nm. Esta estrutura cristalina é estável a pressões de pelo menos 70 GPa. O níquel é duro, maleável e dúctil , e tem uma condutividade elétrica e térmica relativamente alta para metais de transição. A alta resistência à compressão de 34 GPa, prevista para cristais ideais, nunca é obtida no material a granel real devido à formação e movimento de discordâncias . No entanto, foi alcançado em nanopartículas de Ni .
Disputa de configuração eletrônica
O níquel tem duas configurações eletrônicas atômicas , [Ar] 3d 8 4s 2 e [Ar] 3d 9 4s 1 , que são muito próximas em energia; [Ar] denota a estrutura completa do núcleo de argônio . Há algum desacordo sobre qual configuração tem a menor energia. Livros de química citam a configuração eletrônica do níquel como [Ar] 4s 2 3d 8 , também escrito [Ar] 3d 8 4s 2 . Essa configuração está de acordo com a regra de ordenação de energia de Madelung , que prevê que 4s seja preenchido antes de 3d. É apoiado pelo fato experimental de que o estado de energia mais baixo do átomo de níquel é um nível de energia 3d 8 4s 2 , especificamente o nível 3d 8 ( 3 F) 4s 2 3 F, J = 4.
No entanto, cada uma dessas duas configurações se divide em vários níveis de energia devido à estrutura fina , e os dois conjuntos de níveis de energia se sobrepõem. A energia média dos estados com [Ar] 3d 9 4s 1 é na verdade menor do que a energia média dos estados com [Ar] 3d 8 4s 2 . Portanto, a literatura de pesquisa em cálculos atômicos cita a configuração do estado fundamental como [Ar] 3d 9 4s 1 .
isótopos
Os isótopos de níquel variam em peso atômico de 48 u (48
Ni ) a 78 u (78
Ni ).
O níquel natural é composto por cinco isótopos estáveis ,58
Ni ,60
Ni ,61
Ni ,62
Ni e64
Ni , dos quais58
Ni é o mais abundante (68,077% de abundância natural ).
O níquel-62 tem a maior energia de ligação por núcleo de qualquer nuclídeo : 8,7946 MeV/nucleon. Sua energia de ligação é maior que ambas56
Fé e58
Fe , nuclídeos mais abundantes frequentemente citados incorretamente como tendo a maior energia de ligação. Embora isso pareça prever o níquel como o elemento pesado mais abundante no universo, a alta taxa de fotodesintegração do níquel no interior das estrelas faz com que o ferro seja de longe o mais abundante.
O níquel-60 é o produto filho do extinto radionuclídeo 60
Fe (meia-vida de 2,6 milhões de anos). Devido à longa meia-vida de60
Fe , sua persistência em materiais do Sistema Solar pode gerar variações observáveis na composição isotópica de60
Ni . Portanto, a abundância de60
Ni em material extraterrestre pode dar uma visão sobre a origem do Sistema Solar e sua história inicial.
Pelo menos 26 radioisótopos de níquel foram caracterizados; os mais estáveis são59
Ni com meia-vida de 76.000 anos,63
Ni (100 anos) e56
Ni (6 dias). Todos os outros radioisótopos têm meias-vidas inferiores a 60 horas e a maioria destes tem meias-vidas inferiores a 30 segundos. Este elemento também possui um meta-estado .
O níquel-56 radioativo é produzido pelo processo de queima de silício e posteriormente liberado em grandes quantidades em supernovas do tipo Ia . A forma da curva de luz dessas supernovas em tempos intermediários a tardios corresponde ao decaimento via captura de elétrons de56
Ni para cobalto -56 e, finalmente, para ferro-56. O níquel-59 é um radionuclídeo cosmogênico de vida longa ; meia-vida 76.000 anos.59
Ni encontrou muitas aplicações em geologia de isótopos .59
Ni tem sido usado para datar a idade terrestre de meteoritos e para determinar a abundância de poeira extraterrestre no gelo e sedimentos . A meia-vida do níquel-78 foi recentemente medida em 110 milissegundos e acredita-se que seja um isótopo importante na nucleossíntese de supernovas de elementos mais pesados que o ferro. 48 Ni, descoberto em 1999, é o isótopo de elemento pesado mais rico em prótons conhecido. Com 28 prótons e 20 nêutrons , o 48 Ni é " duplamente mágico ", assim como o 78 Ni com 28 prótons e 50 nêutrons. Ambos são, portanto, excepcionalmente estáveis para núcleos com um desequilíbrio próton-nêutron tão grande .
O níquel-63 é um contaminante encontrado na estrutura de suporte de reatores nucleares. É produzido através da captura de nêutrons pelo níquel-62. Pequenas quantidades também foram encontradas perto de locais de teste de armas nucleares no Pacífico Sul.
Ocorrência

Na Terra, o níquel ocorre mais frequentemente em combinação com enxofre e ferro na pentlandita , com enxofre na milerita , com arsênico no mineral níquel e com arsênico e enxofre na galena de níquel . O níquel é comumente encontrado em meteoritos de ferro como as ligas kamacite e taenita . O níquel em meteoritos foi detectado pela primeira vez em 1799 por Joseph-Louis Proust , um químico francês que trabalhava na Espanha. Proust analisou amostras do meteorito de Campo del Cielo (Argentina), obtido em 1783 por Miguel Rubín de Celis, descobrindo nelas a presença de níquel (cerca de 10%) junto com ferro.
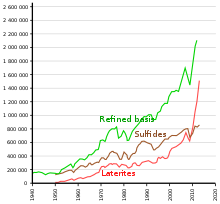
A maior parte do níquel é extraída de dois tipos de depósitos de minério . A primeira é a laterita , onde as principais misturas minerais de minério são limonita niquelífera , (Fe,Ni)O(OH) e garnierita (uma mistura de vários níquel hidratado e silicatos ricos em níquel). O segundo são os depósitos magmáticos de sulfetos , onde o principal minério é a pentlandita : (Ni,Fe) 9 S 8 .
A Indonésia e a Austrália têm as maiores reservas estimadas, com 43,6% do total mundial.
Os recursos terrestres identificados em todo o mundo com uma média de 1% de níquel ou mais compreendem pelo menos 130 milhões de toneladas de níquel (cerca do dobro das reservas conhecidas). Cerca de 60% está em lateritas e 40% em depósitos de sulfeto.
Em evidências geofísicas , acredita-se que a maior parte do níquel na Terra esteja nos núcleos externo e interno da Terra . A kamacita e a taenita são ligas naturais de ferro e níquel. Para kamacite, a liga geralmente está na proporção de 90:10 a 95:5, embora impurezas (como cobalto ou carbono ) possam estar presentes. Taenite é de 20% a 65% de níquel. Kamacite e taenite também são encontrados em meteoritos de ferro níquel .
Compostos
O estado de oxidação mais comum do níquel é +2, mas os compostos de Ni 0 , Ni + e Ni 3+ são bem conhecidos, e os estados de oxidação exóticos Ni 2− e Ni − foram produzidos e estudados.
Níquel(0)
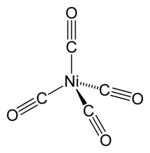
O níquel tetracarbonilo (Ni(CO) 4 ), descoberto por Ludwig Mond , é um líquido volátil e altamente tóxico à temperatura ambiente. Ao aquecer, o complexo se decompõe em níquel e monóxido de carbono:
- Ni(CO) 4 ⇌ Ni + 4 CO
Este comportamento é explorado no processo Mond de purificação do níquel, conforme descrito acima. O bis(ciclooctadieno)níquel(0) complexo relacionado de níquel(0) é um catalisador útil na química de organoníquel porque os ligantes ciclooctadieno (ou bacalhau ) são facilmente deslocados.
Níquel(I)
Complexos de níquel(I) são incomuns, mas um exemplo é o complexo tetraédrico NiBr(PPh 3 ) 3 . Muitos complexos de níquel(I) têm ligação Ni-Ni, como o vermelho escuro diamagnético K 4 [Ni 2 (CN) 6 ] preparado pela redução de K 2 [Ni 2 (CN) 6 ] com amálgama de sódio . Este composto é oxidado em água, liberando H 2 .
Acredita-se que o estado de oxidação do níquel(I) seja importante para as enzimas contendo níquel, como a [NiFe]-hidrogenase , que catalisa a redução reversível de prótons a H 2 .
Níquel(II)

O níquel(II) forma compostos com todos os ânions comuns, incluindo sulfeto , sulfato , carbonato, hidróxido, carboxilatos e haletos. O sulfato de níquel (II) é produzido em grandes quantidades pela dissolução de níquel metálico ou óxidos em ácido sulfúrico , formando um hexa- e hepta-hidrato útil para galvanoplastia de níquel. Sais comuns de níquel, como cloreto, nitrato e sulfato, dissolvem-se em água para dar soluções verdes do metal aquo complexo [Ni(H 2 O) 6 ] 2+ .
Os quatro haletos formam compostos de níquel, que são sólidos com moléculas com centros octaédricos de Ni. O cloreto de níquel (II) é o mais comum e seu comportamento é ilustrativo dos outros haletos. O cloreto de níquel (II) é feito pela dissolução de níquel ou seu óxido em ácido clorídrico . Geralmente é encontrado como o hexa-hidrato verde, cuja fórmula é normalmente escrita NiCl 2 ·6H 2 O . Quando dissolvido em água, este sal forma o metal aquo complexo [Ni(H 2 O) 6 ] 2+ . A desidratação de NiCl 2 ·6H 2 O dá NiCl 2 amarelo anidro .
Alguns complexos de níquel(II) tetracoordenado, por exemplo, cloreto de bis(trifenilfosfina)níquel , existem tanto em geometrias planares tetraédricas quanto quadradas. Os complexos tetraédricos são paramagnéticos ; os complexos planos quadrados são diamagnéticos . Por possuírem propriedades de equilíbrio magnético e formação de complexos octaédricos, contrastam com os complexos divalentes dos metais mais pesados do grupo 10, paládio(II) e platina(II), que formam apenas geometria quadrado-planar.
Nickelocene é conhecido; tem uma contagem de elétrons de 20 e é instável à temperatura ambiente, tornando-o relativamente instável.
Níquel (III) e (IV)
Muitos compostos de Ni(III) são conhecidos. Os primeiros desses compostos são [Ni( PR 3 ) 2 X 2 ] , onde X = Cl , Br , I e R = etil , propil , butil . Além disso, o Ni(III) forma sais simples com íons fluoreto ou óxido . O Ni(III) pode ser estabilizado por ligantes σ-doadores, como tióis e organofosfinas .
Ni(III) ocorre no hidróxido de óxido de níquel , que é usado como cátodo em muitas baterias recarregáveis , incluindo níquel-cádmio , níquel-ferro , níquel-hidreto e níquel-hidreto metálico , e usado por alguns fabricantes em baterias de íons de lítio .
Ni(IV) ocorre no óxido misto BaNiO 3 . O Ni(IV) continua sendo um estado de oxidação raro e poucos compostos são conhecidos.
História
Como os minérios de níquel são facilmente confundidos com minérios de prata e cobre, a compreensão desse metal e seu uso é relativamente recente. Mas o uso não intencional de níquel é antigo e pode ser rastreado até 3500 aC. Descobriu-se que bronzes do que hoje é a Síria contêm até 2% de níquel. Alguns manuscritos chineses antigos sugerem que o "cobre branco" ( cuproníquel , conhecido como baitong ) foi usado lá em 1700-1400 aC. Este cobre branco Paktong foi exportado para a Grã-Bretanha já no século 17, mas o teor de níquel desta liga não foi descoberto até 1822. Moedas de liga de níquel-cobre foram cunhadas pelos reis bactrianos Agátocles, Eutidemo II e Pantaleão no século II . aC, possivelmente do cuproníquel chinês.
Na Alemanha medieval, um mineral amarelo metálico foi encontrado nas Erzgebirge (montanhas de minério) que se assemelhava ao minério de cobre. Mas quando os mineiros não conseguiram obter cobre dele, eles culparam um espírito travesso da mitologia alemã, Nickel (semelhante ao Velho Nick ), por assediar o cobre. Eles chamaram esse minério de Kupfernickel do alemão Kupfer 'cobre'. Este minério é agora conhecido como mineral niquelina (anteriormente niccolita ), um arsenieto de níquel . Em 1751, o barão Axel Fredrik Cronstedt tentou extrair cobre de kupfernickel em uma mina de cobalto na vila de Los, na Suécia , e em vez disso produziu um metal branco que chamou de níquel em homenagem ao espírito que deu nome ao mineral. No alemão moderno, Kupfernickel ou Kupfer-Nickel designa a liga de cuproníquel .
Originalmente, a única fonte de níquel era o raro Kupfernickel. A partir de 1824, o níquel foi obtido como subproduto da produção de azul de cobalto . A primeira fundição em grande escala de níquel começou na Noruega em 1848 a partir de pirrotita rica em níquel . A introdução do níquel na produção de aço em 1889 aumentou a demanda por níquel; os depósitos de níquel da Nova Caledônia , descobertos em 1865, forneceram a maior parte do suprimento mundial entre 1875 e 1915. A descoberta dos grandes depósitos na Bacia de Sudbury , Canadá em 1883, em Norilsk -Talnakh, Rússia em 1920, e no Merensky Reef , na África do Sul em 1924, possibilitou a produção de níquel em grande escala.
Cunhagem

Além das moedas bactrianas acima mencionadas, o níquel não era um componente das moedas até meados do século XIX.
Canadá
Moedas de cinco centavos com 99,9% de níquel foram cunhadas no Canadá (o maior produtor mundial de níquel na época) durante os anos sem guerra, de 1922 a 1981; o conteúdo de metal tornava essas moedas magnéticas. Durante os anos de guerra de 1942 a 1945, a maior parte ou todo o níquel foi removido das moedas canadenses e americanas para salvá-lo na fabricação de armaduras. O Canadá usou 99,9% de níquel de 1968 em suas moedas de maior valor até 2000.
Suíça
Moedas de níquel quase puro foram usadas pela primeira vez em 1881 na Suíça.
Reino Unido
Moedas de níquel forjadas em Birmingham em c. 1833 para negociação na Malásia.
Estados Unidos
Nos Estados Unidos, o termo "níquel" ou "nick" originalmente aplicado ao centavo Flying Eagle de cobre-níquel , que substituiu o cobre por 12% de níquel 1857–58, depois o centavo Indian Head da mesma liga de 1859 a 1864. Ainda mais tarde, em 1865, o termo designou o níquel de três centavos , com níquel aumentado para 25%. Em 1866, o escudo de níquel de cinco centavos (25% de níquel, 75% de cobre) apropriou-se da designação, que tem sido usada desde então para as peças subsequentes de 5 centavos. Esta proporção de liga não é ferromagnética .
A moeda de níquel dos EUA contém 0,04 onças (1,1 g) de níquel, que no preço de abril de 2007 valia 6,5 centavos, junto com 3,75 gramas de cobre no valor de cerca de 3 centavos, com um valor total de metal de mais de 9 centavos. Como o valor nominal de um níquel é de 5 centavos, isso o tornou um alvo atraente para a fusão de pessoas que desejam vender os metais com lucro. A Casa da Moeda dos Estados Unidos , antecipando essa prática, implementou novas regras provisórias em 14 de dezembro de 2006, sujeitas a comentários públicos por 30 dias, que criminalizavam a fusão e exportação de centavos e níquel. Os infratores podem ser punidos com multa de até US$ 10.000 e/ou no máximo cinco anos de prisão. Em 19 de setembro de 2013, o valor de fusão de um níquel dos EUA (incluindo cobre e níquel) é de US$ 0,045 (90% do valor de face).
Uso atual
No século 21, o alto preço do níquel levou a algumas substituições do metal em moedas ao redor do mundo. Moedas ainda feitas com ligas de níquel incluem moedas de um e dois euros , 5 ¢, 10 ¢, 25 ¢, 50 ¢ e moedas de US $ 1 , e moedas de 20p, 50p, £ 1 e £ 2 do Reino Unido . A partir de 2012, a liga de níquel usada para moedas de 5p e 10p do Reino Unido foi substituída por aço niquelado. Isso gerou uma controvérsia pública sobre os problemas das pessoas com alergia ao níquel .
produção mundial
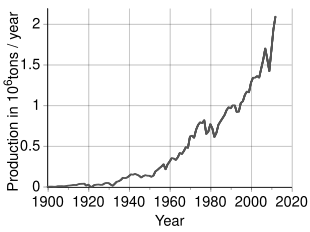
Estima-se que 3,3 milhões de toneladas (t) de níquel por ano são extraídas em todo o mundo; Indonésia (1.600.000 t), Filipinas (330.000 t), Rússia (220.000 t), Nova Caledônia ( França ) (190.000 t), Austrália (160.000 t) e Canadá (130.000 t) são os maiores produtores em 2022. Os maiores depósitos de níquel na Europa não-russa estão na Finlândia e na Grécia . Fontes terrestres identificadas com pelo menos 1% de níquel contêm pelo menos 130 milhões de toneladas de níquel. Cerca de 60% está em lateritas e 40% está em depósitos de sulfeto. Além disso, extensas fontes de níquel são encontradas nas profundezas do Oceano Pacífico , especialmente em uma área chamada Clarion Clipperton Zone na forma de nódulos polimetálicos salpicando o fundo do mar a 3,5–6 km abaixo do nível do mar . Esses nódulos são compostos de numerosos metais de terras raras e são estimados em 1,7% de níquel. Com os avanços da ciência e da engenharia , a regulamentação está sendo estabelecida pela Autoridade Internacional dos Fundos Marinhos para garantir que esses nódulos sejam coletados de maneira ambientalmente responsável, respeitando os Objetivos de Desenvolvimento Sustentável das Nações Unidas .
O único lugar nos Estados Unidos onde o níquel foi extraído com lucro é Riddle, Oregon , com vários quilômetros quadrados de depósitos superficiais de garnierita contendo níquel . A mina foi fechada em 1987. O projeto da mina Eagle é uma nova mina de níquel na Península Superior de Michigan . A construção foi concluída em 2013 e as operações começaram no terceiro trimestre de 2014. No primeiro ano completo de operação, a Eagle Mine produziu 18.000 t.
Produção
O níquel é obtido por meio da metalurgia extrativa : é extraído do minério por processos convencionais de torrefação e redução que produzem metal com pureza superior a 75%. Em muitas aplicações de aço inoxidável , níquel 75% puro pode ser usado sem purificação adicional, dependendo das impurezas.
Tradicionalmente, a maioria dos minérios de sulfeto são processados usando técnicas pirometalúrgicas para produzir um fosco para posterior refino. Avanços recentes em técnicas hidrometalúrgicas resultam em produtos de níquel metálico significativamente mais puros. A maioria dos depósitos de sulfeto tem sido tradicionalmente processada por concentração através de um processo de flotação seguido de extração pirometalúrgica. Nos processos hidrometalúrgicos, os minérios de sulfeto de níquel são concentrados com flotação (flotação diferencial se a relação Ni/Fe for muito baixa) e depois fundidos. O fosco de níquel é posteriormente processado com o processo Sherritt-Gordon . Primeiro, o cobre é removido pela adição de sulfeto de hidrogênio , deixando um concentrado de cobalto e níquel. Em seguida, a extração por solvente é usada para separar o cobalto e o níquel, com o teor final de níquel superior a 86%.

Eletrorrefinação
Um segundo processo de refino comum é a lixiviação do fosco de metal em uma solução de sal de níquel, seguida da extração eletrolítica do níquel da solução, depositando-o em um cátodo como níquel eletrolítico.
Processo Mond

O metal mais puro é obtido do óxido de níquel pelo processo Mond , que dá uma pureza superior a 99,99%. O processo foi patenteado por Ludwig Mond e está em uso industrial desde antes do início do século XX. Neste processo, o níquel reage com monóxido de carbono na presença de um catalisador de enxofre a cerca de 40–80 °C para formar níquel carbonil . Em uma reação semelhante com o ferro, o ferro pentacarbonil pode se formar, embora essa reação seja lenta. Se necessário, o níquel pode ser separado por destilação. Dicobalto octacarbonila também é formado na destilação de níquel como um subproduto, mas se decompõe em tetracobalto dodecacarbonila na temperatura de reação para dar um sólido não volátil.
O níquel é obtido a partir de carbonila de níquel por um de dois processos. Pode ser passado por uma grande câmara a altas temperaturas em que dezenas de milhares de esferas de níquel (pellets) são constantemente agitadas. A carbonila se decompõe e deposita níquel puro nas esferas. No processo alternativo, a carbonila de níquel é decomposta em uma câmara menor a 230 °C para criar um pó fino de níquel. O subproduto monóxido de carbono é recirculado e reutilizado. O produto de níquel altamente puro é conhecido como "níquel carbonílico".
Valor de mercado
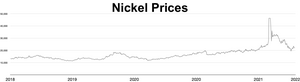
O preço de mercado do níquel aumentou ao longo de 2006 e nos primeiros meses de 2007; em 5 de abril de 2007, o metal era negociado a US $ 52.300/ tonelada ou US$ 1,47/oz. O preço depois caiu drasticamente; em setembro de 2017, o metal estava sendo negociado a $ 11.000/t, ou $ 0,31/oz. Durante a invasão russa da Ucrânia em 2022 , as preocupações com as sanções às exportações russas de níquel desencadearam um pequeno aperto , fazendo com que o preço do níquel quadruplicasse em apenas dois dias, chegando a US$ 100.000 por tonelada. A London Metal Exchange cancelou contratos no valor de US$ 3,9 bilhões e suspendeu o comércio de níquel por mais de uma semana. O analista Andy Home argumentou que tais choques de preços são exacerbados pelos requisitos de pureza impostos pelos mercados de metais: apenas o metal Grau I (99,8% puro) pode ser usado como commodity nas bolsas, mas a maior parte da oferta mundial é de ferro-níquel ligas ou purezas de grau inferior.
Formulários
Atualmente, o uso global de níquel é de 68% em aço inoxidável, 10% em ligas não ferrosas , 9% em galvanoplastia , 7% em ligas de aço, 3% em fundições e 4% em outros (incluindo baterias).
O níquel é usado em muitos produtos industriais e de consumo reconhecíveis, incluindo aço inoxidável , ímãs de alnico , cunhagem, baterias recarregáveis (por exemplo, níquel-ferro ), cordas de guitarra elétrica, cápsulas de microfone, revestimento de encanamentos e ligas especiais como permalloy , elinvar , e invar . É usado para chapeamento e como uma tonalidade verde em vidro. O níquel é predominantemente uma liga de metal, e seu uso principal é em aços de níquel e ferros fundidos de níquel, nos quais normalmente aumenta a resistência à tração, tenacidade e limite elástico. É amplamente utilizado em muitas outras ligas, incluindo latão e bronze de níquel e ligas com cobre, cromo, alumínio, chumbo, cobalto, prata e ouro ( Inconel , Incoloy , Monel , Nimonic ).

Como o níquel é resistente à corrosão, ele foi ocasionalmente usado como substituto da prata decorativa. O níquel também foi usado ocasionalmente em alguns países depois de 1859 como um metal de cunhagem barato (veja acima), mas nos últimos anos do século 20, foi substituído por ligas de aço inoxidável (ou seja, ferro) mais baratas, exceto nos Estados Unidos e Canadá.
O níquel é um excelente agente de liga para certos metais preciosos e é usado no ensaio de fogo como um coletor de elementos do grupo da platina (PGE). Como tal, o níquel pode coletar totalmente todos os seis PGEs dos minérios e pode coletar parcialmente o ouro. As minas de níquel de alto rendimento também podem fazer recuperação de PGE (principalmente platina e paládio ); exemplos são Norilsk, Rússia e a Bacia de Sudbury, Canadá.
Espuma de níquel ou malha de níquel é usada em eletrodos de difusão de gás para células de combustível alcalina .
O níquel e suas ligas são freqüentemente usados como catalisadores para reações de hidrogenação . O níquel de Raney , uma liga de níquel-alumínio finamente dividida, é uma forma comum, embora também sejam usados catalisadores relacionados, incluindo catalisadores do tipo Raney.
O níquel é naturalmente magnetostritivo: na presença de um campo magnético , o material sofre uma pequena alteração no comprimento. A magnetostricção do níquel é da ordem de 50 ppm e é negativa, indicando que ele se contrai.
O níquel é usado como aglutinante na indústria de carboneto de tungstênio cimentado ou metal duro e usado em proporções de 6% a 12% em peso. O níquel torna o carboneto de tungstênio magnético e adiciona resistência à corrosão às peças cimentadas, embora a dureza seja menor do que aquelas com aglutinante de cobalto.
63
Ni , com uma meia-vida de 100,1 anos, é útil em dispositivos de krytron como um emissor de partículas beta ( elétrons de alta velocidade ) para tornar a ionização pelo eletrodo de manutenção de vida mais confiável. Está sendo investigado como fonte de energia para baterias betavoltaicas .
Cerca de 27% de toda a produção de níquel é usada para engenharia, 10% para construção civil, 14% para produtos tubulares, 20% para produtos de metal, 14% para transporte, 11% para produtos eletrônicos e 5% para outros usos.
O níquel de Raney é amplamente usado para hidrogenação de óleos insaturados para fazer margarina , e margarina abaixo do padrão e restos de óleo podem conter níquel como contaminante . Forte et ai. descobriram que pacientes diabéticos tipo 2 têm 0,89 ng/mL de Ni no sangue em relação a 0,77 ng/mL em controles.
papel biológico
Não foi reconhecido até a década de 1970, mas o níquel é conhecido por desempenhar um papel importante na biologia de algumas plantas, bactérias , archaea e fungos . As enzimas de níquel, como a urease, são consideradas fatores de virulência em alguns organismos. A urease catalisa a hidrólise da uréia para formar amônia e carbamato . As hidrogenases de NiFe podem catalisar a oxidação de H 2 para formar prótons e elétrons; e também a reação inversa, a redução de prótons para formar o gás hidrogênio. Uma coenzima de níquel-tetrapirrol, cofator F430 , está presente na metil coenzima M redutase, que pode catalisar a formação de metano, ou a reação inversa, em archaea metanogênica (em estado de oxidação +1). Uma das enzimas do monóxido de carbono desidrogenase consiste em um agrupamento Fe -Ni- S . Outras enzimas contendo níquel incluem uma classe bacteriana rara de enzimas superóxido dismutase e glioxalase I em bactérias e vários parasitas tripanossomais eucarióticos (em outros organismos, incluindo leveduras e mamíferos, esta enzima contém Zn 2+ bivalente ).
O níquel dietético pode afetar a saúde humana através de infecções por bactérias dependentes de níquel, mas o níquel também pode ser um nutriente essencial para as bactérias que vivem no intestino grosso, funcionando como um prebiótico . O Instituto de Medicina dos EUA não confirmou que o níquel é um nutriente essencial para os seres humanos, portanto, nem uma Ingestão Dietética Recomendada (RDA) nem uma Ingestão Adequada foram estabelecidas. O nível de ingestão tolerável de níquel na dieta é de 1 mg/dia como sais de níquel solúveis. A ingestão dietética estimada é de 70 a 100 µg/dia; menos de 10% é absorvido. O que é absorvido é excretado na urina. Quantidades relativamente grandes de níquel – comparáveis à ingestão média estimada acima – se infiltram nos alimentos cozidos em aço inoxidável. Por exemplo, a quantidade de níquel lixiviada após 10 ciclos de cozimento em uma porção de molho de tomate é em média de 88 µg.
Suspeita-se que o níquel liberado pelas erupções vulcânicas das armadilhas siberianas ajude o crescimento de Methanosarcina , um gênero de archaea euryarchaeote que produziu metano no evento de extinção Permiano-Triássico , a maior extinção em massa conhecida .
Toxicidade
| Perigos | |
|---|---|
| Rotulagem GHS : | |
  
|
|
| Perigo | |
| H317 , H351 , H372 , H412 | |
| P201 , P202 , P260 , P264 , P270 , P272 , P273 , P280 , P302+P352 , P308 +P313 , P333+P313 , P363 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
A principal fonte de exposição ao níquel é o consumo oral, pois o níquel é essencial para as plantas. As concentrações típicas de níquel não excedem 20 ng/m 3 no ar, 100 mg/kg no solo, 10 mg/kg na vegetação, 10 μg/L na água doce e 1 μg/L na água do mar. As concentrações ambientais podem ser aumentadas pela poluição humana . Por exemplo, torneiras niqueladas podem contaminar a água e o solo; mineração e fundição podem despejar níquel em águas residuais ; panelas de liga de níquel-aço e pratos pigmentados com níquel podem liberar níquel nos alimentos. O ar pode ser poluído pelo refino do minério de níquel e pela queima de combustível fóssil . Os seres humanos podem absorver o níquel diretamente da fumaça do tabaco e do contato da pele com joias, xampus , detergentes e moedas . Uma forma menos comum de exposição crônica é através da hemodiálise , pois traços de íons de níquel podem ser absorvidos no plasma pela ação quelante da albumina .
A exposição diária média não é uma ameaça para a saúde humana. A maior parte do níquel absorvido pelos seres humanos é removido pelos rins e eliminado do corpo pela urina ou é eliminado pelo trato gastrointestinal sem ser absorvido. O níquel não é um veneno cumulativo, mas doses maiores ou exposição crônica por inalação podem ser tóxicos, até mesmo cancerígenos , e constituir um risco ocupacional .
Os compostos de níquel são classificados como cancerígenos humanos com base no aumento dos riscos de câncer respiratório observados em estudos epidemiológicos de trabalhadores de refinarias de minério sulfídico. Isso é corroborado pelos resultados positivos dos bioensaios de NTP com subsulfeto de Ni e óxido de Ni em ratos e camundongos. Os dados humanos e animais indicam consistentemente uma falta de carcinogenicidade por via oral de exposição e limitam a carcinogenicidade de compostos de níquel a tumores respiratórios após inalação. O níquel metálico é classificado como um carcinógeno suspeito; há consistência entre a ausência de riscos aumentados de câncer respiratório em trabalhadores predominantemente expostos ao níquel metálico e a ausência de tumores respiratórios em um estudo de carcinogenicidade por inalação de ratos ao longo da vida com pó de níquel metálico. Nos estudos de inalação de roedores com vários compostos de níquel e níquel metálico, foram observadas inflamações pulmonares aumentadas com e sem hiperplasia ou fibrose dos gânglios linfáticos brônquicos. Em estudos com ratos, a ingestão oral de sais de níquel solúveis em água pode desencadear mortalidade perinatal em animais prenhes. Não está claro se esses efeitos são relevantes para os seres humanos, pois estudos epidemiológicos de trabalhadoras altamente expostas não mostraram efeitos adversos de toxicidade no desenvolvimento.
As pessoas podem ser expostas ao níquel no local de trabalho por inalação, ingestão e contato com a pele ou olhos. A Occupational Safety and Health Administration (OSHA) estabeleceu o limite legal ( limite de exposição permissível ) para o local de trabalho em 1 mg/m 3 por dia de trabalho de 8 horas, excluindo níquel carbonilado. O Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH) define o limite de exposição recomendado (REL) em 0,015 mg/m 3 por dia de trabalho de 8 horas. A 10 mg/m3 , o níquel é imediatamente perigoso para a vida e a saúde . O carbonilo de níquel [Ni(CO) 4 ] é um gás extremamente tóxico. A toxicidade dos carbonilos metálicos é uma função tanto da toxicidade do metal como da libertação de gás do monóxido de carbono dos grupos funcionais do carbonilo; o níquel carbonílico também é explosivo no ar.
Pessoas sensibilizadas podem apresentar alergia de contato com a pele ao níquel, conhecida como dermatite de contato . Pessoas altamente sensibilizadas também podem reagir a alimentos com alto teor de níquel. Pacientes com pompholyx também podem ser sensíveis ao níquel. O níquel é o principal alérgeno de contato confirmado em todo o mundo, em parte devido ao seu uso em joias para orelhas furadas . As alergias ao níquel que afetam as orelhas furadas geralmente são marcadas por coceira e vermelhidão na pele. Muitos brincos agora são feitos sem níquel ou com níquel de baixa liberação para resolver esse problema. A quantidade permitida em produtos que entram em contato com a pele humana agora é regulamentada pela União Européia . Em 2002, os pesquisadores descobriram que o níquel liberado pelas moedas de 1 e 2 euros excedia em muito esses padrões. Acredita-se que isso se deva a uma reação galvânica . O níquel foi eleito o Alérgeno do Ano em 2008 pela American Contact Dermatitis Society. Em agosto de 2015, a Academia Americana de Dermatologia adotou uma declaração de posição sobre a segurança do níquel: "Estimativas sugerem que a dermatite de contato, que inclui a sensibilização ao níquel, representa aproximadamente US$ 1,918 bilhão e afeta quase 72,29 milhões de pessoas".
Relatórios mostram que tanto a ativação induzida por níquel do fator induzível por hipóxia (HIF-1) quanto a regulação positiva de genes induzíveis por hipóxia são causadas pela depleção de ascorbato intracelular . A adição de ascorbato ao meio de cultura aumentou o nível intracelular de ascorbato e reverteu a estabilização induzida por metal da expressão gênica dependente de HIF-1 e HIF-1α.
Referências
links externos
- Níquel na Tabela Periódica de Vídeos (Universidade de Nottingham)
- CDC – Níquel – Tópico de Saúde e Segurança no Trabalho do NIOSH
- Uma avaliação de higiene ocupacional de exposições dérmicas ao níquel em indústrias de produção primária por GW Hughson. Relatório de Pesquisa do Instituto de Medicina Ocupacional TM/04/05
- Uma avaliação de higiene ocupacional das exposições dérmicas ao níquel na produção primária e nas indústrias de usuários primários. Fase 2 Relatório por GW Hughson. Relatório de Pesquisa do Instituto de Medicina Ocupacional TM/05/06
- "O metal que trouxe voos baratos" , BBC News