beta- Sitosterol - beta-Sitosterol

|
|
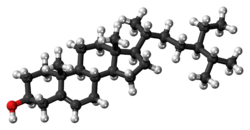
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Stigmast-5-en-3β-ol
|
|
|
Nome IUPAC preferido
(1 R , 3a S , 3b S , 7, S , 9- R , 9b S , 11- R ) -1 - [(2 R , 5 R ) -5-etil-6-methylheptan-2-il] -9a, 11a -dimetil-2,3,3a, 3b, 4,6,7,8,9,9a, 9b, 10,11,11a-tetradecahidro- 1H- ciclopenta [ a ] fenantreno-7-ol |
|
| Outros nomes
22,23-Dihidrostigmasterol, β-Sitosterina
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100,001,346 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 29 H 50 O | |
| Massa molar | 414,718 g · mol −1 |
| Ponto de fusão | 136 a 140 ° C (277 a 284 ° F; 409 a 413 K) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O β-sitosterol ( beta-sitosterol ) é um dos vários fitoesteróis (esteróis vegetais) com estruturas químicas semelhantes às do colesterol . É um pó ceroso branco com um odor característico e é um dos componentes do aditivo alimentar E499 . Os fitoesteróis são hidrofóbicos e solúveis em álcoois.
Ocorrências naturais e alimentos
O β-sitosterol é amplamente distribuído no reino vegetal e encontrado em óleos vegetais , nozes , abacates e alimentos preparados, como molhos para salada .
Pesquisa humana
O β-sitosterol está sendo estudado quanto ao seu potencial para reduzir a hiperplasia prostática benigna (BPH) e os níveis de colesterol no sangue .
Desordem genética
Embora os esteróis vegetais sejam geralmente benéficos, existe um distúrbio genético autossômico recessivo raro, a fitosterolemia, que causa absorção excessiva de fitoesteróis.
Precursor de boldenona de esteróide anabolizante
Por ser um esteróide, o β-sitosterol é um precursor do esteróide anabolizante boldenona . O undecilenato de boldenona é comumente usado na medicina veterinária para induzir o crescimento em bovinos, mas também é um dos esteróides anabolizantes mais usados no esporte. Isso levou à suspeita de que alguns atletas com teste positivo para undecilenato de boldenona não abusaram do hormônio em si, mas consumiram alimentos ricos em β-sitosterol.
Química
Engenheiro químico
O uso do sitosterol como intermediário químico foi por muitos anos limitado devido à falta de um ponto químico de ataque na cadeia lateral que permitisse sua remoção. Esforços extensos por parte de muitos laboratórios eventualmente levaram à descoberta de um micróbio de pseudomonas que efetuou essa transformação com eficiência. A fermentação digere toda a cadeia lateral alifática no carbono 17 para produzir uma mistura de produtos 17-ceto incluindo dehidroepiandrosterona .
Síntese
A síntese total de β-sitosterol não foi alcançada. No entanto, o β-sitosterol foi sintetizado a partir do estigmasterol 1 , que envolve uma hidrogenação específica da cadeia lateral do estigmasterol.
A primeira etapa na síntese forma tosilato de estigmasterol 2 a partir de estigmasterol 1 (pureza de 95%) usando p-TsCl, DMAP e piridina (90% de rendimento). O tosilato 2 sofre então solvólise à medida que é tratado com piridina e MeOH anidro para dar uma proporção de 5: 1 de éter metílico de i-estigmasterol 3 (rendimento de 74%) para éter metílico de estigmasterol 4 , que é subsequentemente removido por cromatografia. A etapa de hidrogenação de uma síntese proposta anteriormente envolveu o catalisador Pd / C e o solvente acetato de etila. No entanto, devido à isomerização durante a hidrólise, outros catalisadores, como PtO2, e solventes, como etanol, foram testados. Houve pouca mudança com o uso de um catalisador diferente. O etanol, no entanto, evitou a isomerização e a formação da impureza não identificada para dar o composto 5 . A última etapa da síntese é a desproteção da ligação dupla do anel β de 5 com p-TsOH, dioxano aquoso e calor (80 ° C) para produzir β-sitosterol 6 . O rendimento cumulativo para as duas etapas finais foi de 55% e o rendimento total da síntese foi de 37%.
Biossíntese
A regulação da biossíntese de ambos os esteróis e alguns lipídios específicos ocorre durante a biogênese da membrana. Por meio dos padrões de marcação com 13C, foi determinado que as vias do mevalonato e da desoxixilulose estão envolvidas na formação de β-sitosterol. O mecanismo preciso de formação do β-sitosterol varia de acordo com o organismo, mas geralmente é proveniente do cicloartenol .
A biossíntese do cicloartenol começa como uma molécula de difosfato de isopentenila (IPP) e duas moléculas de difosfato de dimetilalila (DMAPP) formam difosfato de farnesila (FPP). Duas moléculas de FPP são então unidas cauda com cauda para produzir esqualeno , um triterpeno . O esqualeno, por meio de uma reação de ciclização com 2,3-oxidosqualeno 6 como intermediário, forma o cicloartenol.
A dupla ligação do cicloartenol (composto 7 no diagrama) é metilada por SAM para dar um carbocátion que sofre uma mudança de hidreto e perde um próton para produzir um composto com uma cadeia lateral de metileno. Ambas as etapas são catalisadas pela esterol C-24 metiltransferase (Etapa E1 no diagrama). O composto 8 é então catalisado pela esterol C-4 desmetilase (E2) e perde um grupo metil para produzir ciclo eucalenol. Posteriormente a isso, o anel de ciclopropano é aberto com ciclo eucalenol cicloisomerase (E3) para formar 10 . O composto 10 perde um grupo metil e sofre uma isomerização alílica para formar gramisterol 11 . Esta etapa é catalisada por esterol C-14 desmetilase (E4), esterol Δ14-redutase (E5) e esterol Δ8-Δ7-isomerase (E6). O último grupo metil é removido pela esterol desmetilase (E7) para formar o episterol 12 . Episterol 12 é metilado por SAM para produzir um segundo carbocátion, que perde um próton para produzir 13 . Esta etapa é catalisada pela 24-metilenesterol C-metiltransferase (E8). O composto 13 agora sofre redução por NADPH e modificações no anel β para formar β-sitosterol.
Veja também
- Charantin , um β-sitosteril glucosídeo encontrado no melão amargo .


