Tautomer - Tautomer
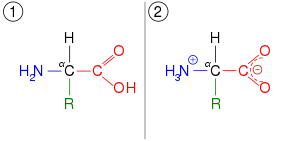
Os tautómeros ( / t ɔː t ə m ər / ) são os isómeros estruturais (isómeros constitucionais) de compostos químicos que prontamente interconvertem. Essa reação comumente resulta na realocação de um átomo de hidrogênio. O tautomerismo é, por exemplo, relevante para o comportamento dos aminoácidos e dos ácidos nucléicos, dois dos blocos de construção fundamentais da vida.
O conceito de tautomerização é denominado tautomerismo . O tautomerismo também é denominado desmotropismo. A reação química interconvertendo os dois é chamada de tautomerização .
Deve-se ter cuidado para não confundir tautômeros com representações de "estruturas contribuintes" em ressonância química . Tautômeros são espécies químicas distintas e podem ser identificados como tais por seus dados espectroscópicos diferentes , enquanto as estruturas de ressonância são meramente representações convenientes e não existem fisicamente.
Exemplos
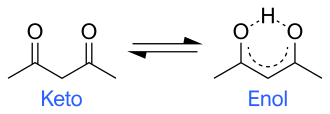
A tautomerização é difundida na química orgânica . É tipicamente associado a moléculas polares e íons contendo grupos funcionais que são pelo menos fracamente ácidos. Os tautômeros mais comuns existem em pares, o que significa que o hidrogênio está localizado em uma das duas posições e, ainda mais especificamente, a forma mais comum envolve um hidrogênio trocando de lugar com uma ligação dupla: H − X − Y = Z ⇌ X = Y− Z − H. Os pares tautoméricos comuns incluem:
- cetona - enol : H − O − C = C ⇌ O = C − C − H, ver tautomerismo ceto-enol
-
enamina - imina : H − N − C = C ⇌ N = C − C − H
- cianamida - carbodiimida
- guanidina - guanidina - guanidina: Com um carbono central rodeado por três nitrogênios , um grupo guanidina permite esta transformação em três orientações possíveis
-
amida - ácido imídico : H − N − C = O ⇌ N = C − O − H (por exemplo, o último é encontrado durante as reações de hidrólise de nitrila )
- lactam - lactim , uma forma cíclica de tautomerismo de ácido amida-imídico em 2-piridona e estruturas derivadas, como as nucleobases guanina , timina e citosina
- imina - imina, por exemplo, durante o fosfato de piridoxal catalisada enzimáticas reacções
- R 1 R 2 C (= NCHR 3 R 4 ) ⇌ (R 1 R 2 CHN =) CR 3 R 4
- nitro - aci -nitro (ácido nitrônico): RR'HC – N + (= O) (O - ) ⇌ RR'C = N + (O - ) (OH)
- nitroso - oxima : H − C − N = O ⇌ C = N − O − H
- ceteno - inol , que envolve uma ligação tripla: H − C = C = O ⇌ C≡C − O − H
-
aminoácido - carboxilato de amônio, que se aplica aos blocos de construção das proteínas. Isso desloca o próton para mais de dois átomos, produzindo um zwitterion em vez de deslocar uma ligação dupla: H 2 N − CH 2 −COOH ⇌ H 3 N+
−CH 2 −CO-
2 - fosfito - fosfonato : P (OR) 2 (OH) ⇌ HP (OR) 2 (= O) entre fósforo trivalente e pentavalente.
Prototropia
A prototropia é a forma mais comum de tautomerismo e se refere à realocação de um átomo de hidrogênio. O tautomerismo prototrópico pode ser considerado um subconjunto do comportamento ácido-básico . Tautômeros prototrópicos são conjuntos de estados de protonação isoméricos com a mesma fórmula empírica e carga total . As tautomerizações são catalisadas por:
- bases , envolvendo uma série de etapas: desprotonação, formação de um ânion deslocalizado (por exemplo, um enolato ) e protonação em uma posição diferente do ânion; e
- ácidos , envolvendo uma série de etapas: protonação, formação de um cátion deslocalizado e desprotonação em uma posição diferente adjacente ao cátion).

Duas outras subcategorias específicas de tautomerizações:
- O tautomerismo anular é um tipo de tautomerismo prototrópico em que um próton pode ocupar duas ou mais posições de um sistema heterocíclico , por exemplo, 1 H - e 3 H - imidazol ; 1 H -, 2 H - e 4 H - 1,2,4-triazol ; 1 H - e 2 H - isoindole .
- Os tautômeros de cadeia em anel ocorrem quando o movimento do próton é acompanhado por uma mudança de uma estrutura aberta para um anel, como a cadeia aberta e o hemiacetal cíclico (tipicamente piranose ou furanose ) de muitos açúcares. (Veja Carboidrato § Isomerismo de cadeia linear de anel .) O deslocamento tautomérico pode ser descrito como H − O ⋅ C = O ⇌ O − C − O − H, onde o "⋅" indica a ausência inicial de uma ligação.
Valence tautomerism
Tautomerismo de valência é um tipo de tautomerismo em que ligações simples e / ou duplas são rapidamente formadas e rompidas, sem migração de átomos ou grupos. É distinto do tautomerismo prototrópico e envolve processos com rápida reorganização dos elétrons de ligação.
Um par de tautômeros de valência com fórmula C 6 H 6 O são óxido de benzeno e oxepina .
Outros exemplos deste tipo de tautomerismo podem ser encontrados em bullvalene , e em formas abertas e fechadas de certos heterociclos , tais como azidas e tetrazoles orgânicos , ou münchnone mesoiônico e acilamino ceteno.
O tautomerismo de valência requer uma mudança na geometria molecular e não deve ser confundido com estruturas de ressonância canônica ou mesômeros.
Veja também
Referências
links externos
-
 Mídia relacionada ao tautomerismo no Wikimedia Commons
Mídia relacionada ao tautomerismo no Wikimedia Commons


