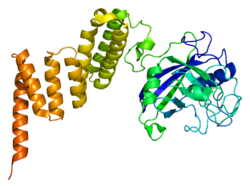Peptidilprolil isomerase D - Peptidylprolyl isomerase D
A peptidilprolil isomerase D (ciclofilina D) , também conhecida como PPID , é uma enzima que em humanos é codificada pelo gene PPID no cromossomo 4. Como membro da família da peptidil-prolil cis-trans isomerase (PPIase), esta proteína catalisa a Isomerização cis-trans de ligações peptídicas imídicas de prolina , o que permite facilitar o dobramento ou reparo de proteínas. Além disso, o PPID participa de muitos processos biológicos, incluindo metabolismo mitocondrial , apoptose , redox e inflamação , bem como em doenças e condições relacionadas, como lesão de reperfusão isquêmica , AIDS e câncer .
Estrutura
Como outras ciclofilinas, o PPID forma uma estrutura de barril β com um núcleo hidrofóbico. Este barril β é composto por oito fitas β anti-paralelas e coberto por duas hélices α na parte superior e inferior. Além disso, as voltas β e os laços nos fios contribuem para a flexibilidade do cano. O PPID, em particular, é composto por 370 resíduos e compartilha homologia estrutural com PPIF , FKBP4 e FKBP5 , incluindo um domínio semelhante a imunofilina N-terminal e um domínio de repetição de tetratricopeptídeo C-terminal (TPR) .
Função
A proteína codificada por este gene é um membro da família da peptidil-prolil cis-trans isomerase ( PPIase ). As PPIases catalisam a isomerização cis-trans das ligações peptídicas imídicas da prolina em oligopeptídeos e aceleram o dobramento das proteínas. Geralmente, as PPIases são encontradas em todas as eubactérias e eucariotos, bem como em algumas arquéias e, portanto, são altamente conservadas. A família PPIase é ainda dividida em três subfamílias estruturalmente distintas: ciclofilina (CyP), proteína de ligação a FK506 ( FKBP ) e parvulina (Pvn). Como uma ciclofilina, o PPID liga-se à ciclosporina A (CsA) e pode ser encontrado dentro da célula ou secretado pela célula. Em eucariotos, as ciclofilinas localizam-se de forma ubíqua em muitos tipos de células e tecidos. Além das atividades da PPIase e da chaperona proteica, as ciclofilinas também atuam no metabolismo mitocondrial, apoptose, resposta imunológica, inflamação e crescimento e proliferação celular. O PPID, em particular, ajuda a acompanhar a formação da proteína de choque térmico Hsp90 , bem como a localização nuclear dos receptores de glicocorticóide, estrogênio e progesterona. Juntamente com o PPIF, o PPID regula a apoptose mitocondrial. Em resposta a níveis elevados de espécies reativas de oxigênio (ROS) e de íons de cálcio, o PPID interage com Bax para promover a formação de poros mitocondriais, liberando assim fatores pró-apoptóticos, como citocromo C e AIF .
Significado clínico
Como uma ciclofilina, o PPID se liga à droga imunossupressora CsA para formar um complexo CsA-ciclofilina, que então tem como alvo a calcineurina para inibir a via de sinalização para a ativação das células T.
Em células miogênicas cardíacas, observou-se que as ciclofilinas são ativadas por choque térmico e hipóxia-reoxigenação, bem como complexas com proteínas de choque térmico. Assim, as ciclofilinas podem funcionar na cardioproteção durante a lesão de isquemia-reperfusão .
Atualmente, a expressão da ciclofilina está altamente correlacionada com a patogênese do câncer, mas os mecanismos específicos ainda precisam ser elucidados. Estudos demonstraram que o PPID protege os queratinócitos humanos da apoptose induzida por UVA, portanto, medicamentos e terapias que inibem o PPID, como CsA, podem inadvertidamente auxiliar no desenvolvimento do câncer de pele. Por outro lado, os tratamentos que promovem a atividade PPID podem melhorar os resultados do paciente quando combinados com terapias UVA contra o câncer.
Interações
Foi demonstrado que o PPID interage com:
Referências
Leitura adicional
- Berardini TZ, Bollman K., Sun H, Poethig RS (março de 2001). "Regulação da mudança de fase vegetativa em Arabidopsis thaliana pela ciclofilina 40". Ciência . 291 (5512): 2405–7. doi : 10.1126 / science.1057144 . PMID 11264535 . S2CID 31121128 .
- Kieffer LJ, Thalhammer T, Handschumacher RE (março de 1992). "Isolamento e caracterização de uma proteína relacionada à ciclofilina de 40 kDa". The Journal of Biological Chemistry . 267 (8): 5503–7. PMID 1544925 .
- Hoffmann K, Kakalis LT, Anderson KS, Armitage IM, Handschumacher RE (abril de 1995). "Expression of human cyclophilin-40 and the effect of the His141 -> Trp mutation on catysis and cyclosporin A binding". European Journal of Biochemistry / FEBS . 229 (1): 188–93. doi : 10.1111 / j.1432-1033.1995.tb20454.x . PMID 7744028 .
- Kieffer LJ, Seng TW, Li W, Osterman DG, Handschumacher RE, Bayney RM (junho de 1993). "Ciclofilina-40, uma proteína com homologia ao componente P59 do complexo do receptor de esteróide. Clonagem do cDNA e posterior caracterização". The Journal of Biological Chemistry . 268 (17): 12303–10. PMID 8509368 .
- Yokoi H, Shimizu Y, Anazawa H, Lefebvre CA, Korneluk RG, Ikeda JE (agosto de 1996). "A estrutura e a sequência de nucleotídeos completa do gene da ciclofilina 40 humana (PPID)". Genômica . 35 (3): 448–55. doi : 10.1006 / geno.1996.0384 . PMID 8812478 .
- Bonaldo MF, Lennon G, Soares MB (set 1996). "Normalização e subtração: duas abordagens para facilitar a descoberta do gene" . Genome Research . 6 (9): 791–806. doi : 10.1101 / gr.6.9.791 . PMID 8889548 .
- Silverstein AM, Galigniana MD, Chen MS, Owens-Grillo JK, Chinkers M, Pratt WB (junho de 1997). "A proteína fosfatase 5 é um componente principal do receptor de glucocorticóides. Complexos hsp90 com propriedades de uma imunofilina de ligação a FK506" . The Journal of Biological Chemistry . 272 (26): 16224–30. doi : 10.1074 / jbc.272.26.16224 . PMID 9195923 .
- Young JC, Obermann WM, Hartl FU (julho de 1998). "Ligação específica de proteínas de repetição de tetratricopeptídeo ao domínio C-terminal de 12 kDa de hsp90" . The Journal of Biological Chemistry . 273 (29): 18007–10. doi : 10.1074 / jbc.273.29.18007 . PMID 9660753 .
- Mark PJ, Ward BK, Kumar P, Lahooti H, Minchin RF, Ratajczak T (janeiro de 2001). "A ciclofilina humana 40 é uma proteína de choque térmico que exibe localização intracelular alterada após choque térmico" . Estresse celular e acompanhantes . 6 (1): 59–70. doi : 10.1379 / 1466-1268 (2001) 006 <0059: HCIAHS> 2.0.CO; 2 . PMC 434384 . PMID 11525244 .
- Ward BK, Allan RK, Mok D, Temple SE, Taylor P, Dornan J, Mark PJ, Shaw DJ, Kumar P, Walkinshaw MD, Ratajczak T (outubro de 2002). "Uma análise mutacional baseada na estrutura da ciclofilina 40 identifica resíduos-chave no domínio de repetição do tetratricopeptídeo central que medeia a ligação a Hsp90" . The Journal of Biological Chemistry . 277 (43): 40799–809. doi : 10.1074 / jbc.M207097200 . PMID 12145316 .
- McStay GP, Clarke SJ, Halestrap AP (outubro de 2002). "Papel dos grupos tiol críticos na superfície da matriz da translocase do nucleotídeo da adenina no mecanismo do poro de transição da permeabilidade mitocondrial" . The Biochemical Journal . 367 (Pt 2): 541–8. doi : 10.1042 / BJ20011672 . PMC 1222909 . PMID 12149099 .
- Gevaert K, Goethals M, Martens L, Van Damme J, Staes A, Thomas GR, Vandekerckhove J (maio de 2003). "Explorando proteomas e analisando o processamento de proteínas por identificação de espectrometria de massa de peptídeos N-terminais classificados". Nature Biotechnology . 21 (5): 566–9. doi : 10.1038 / nbt810 . PMID 12665801 . S2CID 23783563 .
- Schubert A, Grimm S (janeiro de 2004). "Ciclofilina D, um componente do poro de transição de permeabilidade, é um repressor de apoptose" . Cancer Research . 64 (1): 85–93. doi : 10.1158 / 0008-5472.CAN-03-0476 . PMID 14729611 .
- Machida K, Osada H (dezembro de 2003). "A interação molecular entre a ciclofilina D e a translocase do nucleotídeo da adenina na liberação do citocromo c: isso determina se a liberação do citocromo c depende da transição da permeabilidade ou não?". Anais da Academia de Ciências de Nova York . 1010 : 182–5. doi : 10.1196 / annals.1299.031 . PMID 15033717 . S2CID 1034903 .
- Carrello A, Allan RK, Morgan SL, Owen BA, Mok D, Ward BK, Minchin RF, Toft DO, Ratajczak T (2005). "Interaction of the Hsp90 cochaperone cyclophilin 40 with Hsc70" . Estresse celular e acompanhantes . 9 (2): 167–81. doi : 10.1379 / CSC-26R.1 . PMC 1065296 . PMID 15497503 .
- Barrios-Rodiles M, Brown KR, Ozdamar B, Bose R, Liu Z, Donovan RS, Shinjo F, Liu Y, Dembowy J, Taylor IW, Luga V, Przulj N, Robinson M, Suzuki H, Hayashizaki Y, Jurisica I, Wrana JL (março de 2005). "Mapeamento de alto rendimento de uma rede de sinalização dinâmica em células de mamíferos". Ciência . 307 (5715): 1621–5. doi : 10.1126 / science.1105776 . PMID 15761153 . S2CID 39457788 .
- Machida K, Ohta Y, Osada H (maio de 2006). "Supressão da apoptose pela ciclofilina D via estabilização da ligação mitocondrial hexokinase II em células cancerosas" . The Journal of Biological Chemistry . 281 (20): 14314–20. doi : 10.1074 / jbc.M513297200 . PMID 16551620 .
- Mok D, Allan RK, Carrello A, Wangoo K, Walkinshaw MD, Ratajczak T (maio de 2006). "A função chaperona da ciclofilina 40 mapeia uma fenda entre os domínios de repetição da prolil isomerase e tetratricopeptídeo" . FEBS Letters . 580 (11): 2761–8. doi : 10.1016 / j.febslet.2006.04.039 . PMID 16650407 . S2CID 26811748 .