Vacina pentavalente - Pentavalent vaccine
| Combinação de | |
|---|---|
| Vacina DTP | Vacina |
| Vacina contra hepatite B | Vacina |
| Vacina contra Haemophilus | Vacina |
| Dados clínicos | |
| Nomes comerciais | Quintavax, Pentavac, Pentacel, outros |
| Vias de administração |
Injeção intramuscular |
| Código ATC | |
| Identificadores | |
| Número CAS | |
Uma vacina pentavalente , também conhecida como vacina 5 em 1 , é uma vacina combinada com cinco vacinas individuais conjugadas em uma.
A vacina pentavalente freqüentemente se refere à vacina 5 em 1 que protege contra difteria , tétano , coqueluche , hepatite B e Haemophilus influenzae tipo B , que é geralmente usada em países de renda média e baixa , onde a vacina da poliomielite é administrada separadamente.
Outra vacina pentavalente é a vacina 5 em 1 que protege contra difteria, tétano, coqueluche, poliomielite e Haemophilus influenza tipo B , que foi usada no Reino Unido até 2017, após a qual uma vacina 6 em 1 foi disponibilizada contendo a proteção adicional contra a hepatite B.
Em 2013, as vacinas pentavalentes representavam 100% das vacinas contendo DTP adquiridas pela UNICEF , que fornece vacinas para uma grande proporção das crianças do mundo.
Segurança
Durante os estudos e testes, a vacina líquida conjugada DTPw - HepB - Hib demonstrou ter segurança positiva quando administrada como reforço a crianças pequenas que receberam um esquema de vacinação com outro reforço pentavalente que requer uma mudança na constituição e também foi considerado ser adequadamente imunogênica .
História
Em outubro de 2004, a Agência Europeia de Medicamentos concedeu aprovação de comercialização na UE para a vacina pentavalente Quintanrix, fabricada pela GlaxoSmithKline . A Quintanrix foi retirada voluntariamente pelo fabricante em 2008.
Em setembro de 2006, a primeira formulação de vacina pentavalente recebeu aprovação de pré-qualificação da Organização Mundial de Saúde .
Em 2012, o UNICEF e a Organização Mundial da Saúde emitiram e recomendaram uma declaração conjunta à Divisão de Imunização, Ministério da Saúde e Bem-Estar da Família, Governo da Índia e outras nações em desenvolvimento em documentos separados sobre o uso de vacinas pentavalentes para proteger contra cinco dos principais causas de morte evitável por vacina em crianças.
Em 2013, as vacinas pentavalentes representavam 100% das vacinas contendo DTP adquiridas pela UNICEF, que fornece vacinas para uma grande proporção das crianças do mundo.
Em 2014, o Sudão do Sul se tornou o último dos 73 países com apoio da GAVI a introduzir a vacina cinco em um.
Sociedade e cultura
Em maio de 2010, a Crucell NV anunciou um prêmio de US $ 110 milhões da UNICEF para fornecer sua vacina pediátrica pentavalente Quinvaxem para o mundo em desenvolvimento.
Em novembro de 2010, o consórcio público-privado GAVI anunciou que o custo da vacina pentavalente para países emergentes havia caído para menos de US $ 3,00 por dose.
Os países de alta renda tendem a usar formulações alternativas usando coqueluche acelular (Pa), que tem um perfil mais favorável de efeitos colaterais, em vez de componentes de coqueluche de células inteiras. Na Europa, as vacinas hexavalentes que também contêm a vacina inativada contra a poliomielite ( IPV ) são amplamente utilizadas. Nos EUA, as duas vacinas pentavalentes que receberam aprovação para comercialização contêm IPV em vez da vacina contra hepatite B (vacina DTaP-IPV / Hib ) ou vacina Hib (vacina DTaP-IPV-HepB ).
Todos os preços das vacinas pentavalentes caíram e a discriminação de preços quase desapareceu. Gráfico de GAVI; preços não UNICEF não mostrados
Índia
Em 2013, verificou-se que as vacinas Pentavac PFS estavam sendo fornecidas com dois conjuntos diferentes de embalagens: um conjunto com datas de fabricação e validade estava sendo fornecido para hospitais privados , enquanto o outro conjunto sem datas de fabricação e validade estava sendo distribuído para hospitais públicos . Posteriormente, foi esclarecido que as vacinas sem data foram fornecidas pela UNICEF e estavam em conformidade com a legislação indiana .
Sri Lanka
O Sri Lanka introduziu o Quinvaxem em janeiro de 2008. Em três meses, quatro notificações de mortes e 24 notificações de episódios hipotônicos-hiporresponsivos suspeitos solicitaram atenção regulatória e suspensão preventiva do lote inicial da vacina. Uma morte subsequente que ocorreu com o próximo lote em abril de 2009 levou as autoridades a suspender o uso da vacina pentavalente e retomar a vacinação contra DTwP e hepatite B. Após investigação de especialistas independentes nacionais e internacionais, a vacina foi reintroduzida em 2010.
Butão
O Butão introduziu o Easyfive-TT em setembro de 2009. A identificação de cinco casos com encefalopatia e / ou meningoencefalite logo após a vacinação pentavalente levou as autoridades a suspender a vacinação em 23 de outubro de 2009. Posteriormente, quatro casos graves adicionais relacionados à vacina administrada antes da suspensão foram identificados e investigado. Após uma revisão abrangente por especialistas nacionais e internacionais independentes, a vacina foi reintroduzida em 2011.
Vietnã
Entre dezembro de 2012 e março de 2013, nove mortes foram relatadas no Vietnã de crianças que haviam recebido recentemente injeções da vacina pentavalente Quinvaxem. Em 4 de maio de 2013, o Ministério da Saúde do Vietnã anunciou que o uso de Quinvaxem foi suspenso.
Após uma revisão dos casos conduzida por especialistas nacionais em conjunto com funcionários da OMS e UNICEF e um médico independente, nenhuma ligação com a vacinação pôde ser identificada. As fatalidades relatadas no Vietnã foram atribuídas a problemas de saúde coincidentes relacionados no tempo, mas não relacionados ao uso de Quinvaxem, ou casos para os quais as informações disponíveis não permitiam uma conclusão definitiva, mas não havia sinais clínicos consistentes com o uso da vacina. O relatório da OMS enfatizou que mais de 400 milhões de doses de Quinvaxem foram administradas e que nenhum evento adverso fatal foi associado ao Quinvaxem ou vacinas semelhantes.
Após relatórios adicionais da Índia , Sri Lanka e Butão sobre um pequeno número de eventos adversos sérios após a imunização com vacinas pentavalentes, a OMS solicitou a um painel global de especialistas independentes para revisar a segurança da vacina. Esta revisão ocorreu de 12 a 13 de junho de 2013 e concluiu que nenhuma reação incomum pode ser atribuída às vacinas pentavalentes. Em 20 de junho de 2013, o Ministério da Saúde anunciou que o Vietnã retomaria o uso de Quinvaxem.
Os eventos relatados nessas nações asiáticas causaram incerteza pública quanto ao uso de vacinas pentavalentes para se espalhar para outras nações em desenvolvimento. Em resposta a isso, e uma disseminação correspondente de informações imprecisas sobre a segurança das vacinas, a Academia Indiana de Pediatria divulgou uma declaração em apoio às vacinas pentavalentes.
Formulações
Versões comuns de vacinas pentavalentes incluem Quinvaxem, Pentavac PFS, Easyfive TT, ComBE Five, Shan5 e Pentabio.
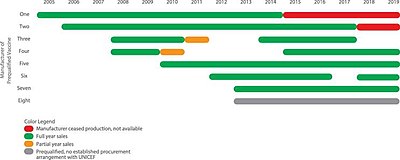
| Vacina | Fabricante | Data pré-qualificada pela OMS |
|---|---|---|
| Quinvaxem | Crucell | 26 de setembro de 2006 |
| Pentavac PFS | Instituto de Soro da Índia | 23 de junho de 2010 |
| Easyfive TT | Panacea Biotec | 2 de outubro de 2013 |
| ComBE Five | Biological E. Limited | 1 de setembro de 2011 |
| Shan5 | Shantha Biotechnics | 29 de abril de 2014 |
| Pentabio | Bio Farma | 19 de dezembro de 2014 |
Notas
Referências
Leitura adicional
- Dodoo AN, Renner L, van Grootheest AC, Labadie J, Antwi-Agyei KO, Hayibor S, et al. (2007). "Monitoramento de segurança de uma nova vacina pentavalente no programa ampliado de imunização em Gana". Segurança de medicamentos . 30 (4): 347–56. doi : 10.2165 / 00002018-200730040-00007 . PMID 17408311 . S2CID 37633844 .
- Verma R, Khanna P, Chawla S (julho de 2013). "Vacina DTP pentavalente: precisa ser incorporada ao programa de vacinação da Índia" . Vacinas e imunoterapêuticas humanas . 9 (7): 1497–9. doi : 10.4161 / hv.24382 . PMID 23571225 .
links externos
- Quinn B (6 de junho de 2011). “Empresas de medicamentos para baixar o preço das vacinas nos países em desenvolvimento” . The Guardian .
- Dhar A (11/10/2013). "A vacina pentavalente é limpa, definida para escala nacional" . O hindu .
- Sinha V (10 de junho de 2011). "Organização da Saúde, Fundação Gates Promover Maior Uso de Vacinas" . Voice of America . Arquivado do original em 5 de março de 2016.