Metilmalonil-CoA mutase - Methylmalonyl-CoA mutase
| metilmalonil-CoA mutase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| EC nº | 5.4.99.2 | ||||||||
| CAS no. | 9023-90-9 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
Metilmalonil-CoA mutase (MCM), mitocondrial , também conhecida como metilmalonil-CoA isomerase , é uma proteína que em humanos é codificada pelo gene MUT . Esta vitamina B 12 enzima dependente catalisa a isomerização de metilmalonil-CoA para succinil-CoA-redutase nos seres humanos. Mutações no gene MUT podem levar a vários tipos de acidúria metilmalônica .
MCM foi identificado pela primeira vez em fígado de rato e rim de ovelha em 1955. Em sua forma latente, tem 750 aminoácidos de comprimento. Após a entrada na mitocôndria, a sequência líder mitocondrial de 32 aminoácidos no terminal N da proteína é clivada, formando o monômero totalmente processado. Os monômeros então se associam em homodímeros e ligam AdoCbl (um para cada sítio ativo do monômero) para formar a forma de holoenzima ativa final .
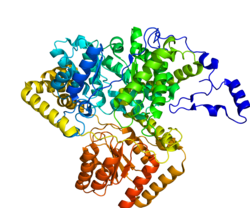
Estrutura
Gene
O gene MUT está localizado no cromossomo 6p12.3 e consiste em 13 exons , medindo mais de 35kb.
Proteína
A enzima madura é um homodímero com o domínio de ligação de CoA N-terminal e o domínio de ligação de cobalamina C-terminal.
Função
A metilmalonil-CoA mutase é expressa em altas concentrações no rim , em concentrações intermediárias no coração , ovários , cérebro , músculos e fígado e em baixas concentrações no baço . A enzima pode ser encontrada em todo o sistema nervoso central (SNC). MCM reside na mitocôndria, onde uma série de substâncias, incluindo os aminoácidos de cadeia ramificada isoleucina e valina , bem como metionina , treonina , timina e ácidos graxos de cadeia ímpar , são metabolizados via semialdeído de metilmalonato (MMlSA) ou propionil-CoA (Pr-CoA) a um composto comum - metilmalonil-CoA (MMl-CoA). MCM catalisa a isomerização reversível de l-metilmalonil-CoA em succinil-CoA, requerendo cobalamina (vitamina B12) na forma de adenosilcobalamina (AdoCbl) como cofator. Como uma etapa importante no catabolismo do propionato, essa reação é necessária para a degradação dos ácidos graxos de cadeia ímpar , os aminoácidos valina , isoleucina , metionina e treonina e colesterol , canalizando metabólitos da decomposição desses aminoácidos em ácido tricarboxílico ciclo .
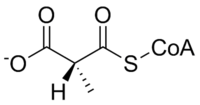
A mutase de metilmalonil-CoA catalisa a seguinte reação:
| L-metilmalonil-CoA | metilmalonil-CoA mutase | Succinil-CoA | |
|

|
||

|
|||
| metilmalonil-CoA mutase | |||
O substrato da metilmalonil-CoA mutase, metilmalonil-CoA , é principalmente derivado de propionil-CoA , uma substância formada a partir do catabolismo e da digestão de isoleucina , valina , treonina , metionina , timina , colesterol ou ácidos graxos de cadeia ímpar. O produto da enzima, succinil-CoA , é uma molécula chave do ciclo do ácido tricarboxílico .
Significado clínico
A deficiência dessa enzima é responsável por um distúrbio hereditário do metabolismo, deficiência da metilmalonil-CoA mutase , que é uma das causas da acidemia metilmalônica (também conhecida como acidúria metilmalônica ou MMA). O MMA é um erro inato hereditário autossômico recessivo do metabolismo, caracterizado por episódios recorrentes de vômitos, letargia, cetoacidose profunda , hiperamonemia e pancitopenia na infância e pode causar morte precoce. As complicações incluem cardiomiopatia , acidente vascular cerebral metabólico , pancreatite e insuficiência renal progressiva .
As mutações no gene MUT (codifica a metilmalonil-CoA mutase) ou MMAA (codifica uma proteína chaperona da metilmalonil-CoA mutase, proteína MMAA ) podem levar à acidemia da metilmalonil. Mutações em MUT podem ser categorizadas como MUT 0 (não demonstra atividade mesmo na presença de excesso de AdoCbl) ou MUT 1 (demonstra atividade muito baixa na presença de excesso de AdoCbl). Mais da metade das mutações de MUT são mutações sem sentido, enquanto as mutações sem sentido compreendem uma fração restante significativa (aproximadamente 14%)
Os métodos de tratamento comuns para MMA incluem um transplante de fígado ou um transplante de fígado e rim para combater a doença renal da acidemia metilmalônica. No entanto, os efeitos neurológicos prejudiciais podem continuar a atormentar os pacientes, mesmo após uma operação bem-sucedida. Pensa-se que isto se deve à presença generalizada de metilmalonil-CoA mutase em todo o sistema nervoso central. Devido à perda de funcionalidade da enzima, os níveis de substrato se acumulam no SNC. O substrato, L-metilmalonil-CoA hidrolisa para formar metilmalonato (ácido metilmalônico), um ácido dicarboxílico neurotóxico que, devido às fracas capacidades de transporte de ácido dicarboxílico da barreira hematoencefálica, é efetivamente preso dentro do SNC, levando à debilitação neurológica. Para combater esses efeitos, regimes anti-catabólicos perioperatórios e nenhuma interrupção da dieta são recomendados.
O modelo murino provou ser uma forma adequada e precisa de estudar os efeitos do MMA e os métodos de tratamento potenciais.
Mecanismo
O mecanismo de reação MCM começa com a clivagem homolítica da ligação C- Co (III) do AdoB12 , os átomos C e Co cada um adquire um dos elétrons que formaram a ligação do par de elétrons clivado. O íon Co, portanto, flutua entre seus estados de oxidação Co (III) e Co (II) [os dois estados são espectroscopicamente distinguíveis: Co (III) é vermelho e diamagnético (sem elétrons desemparelhados), enquanto Co (II) é amarelo e paramagnético (elétrons desemparelhados)]. Conseqüentemente, o papel da coenzima B-12 no processo catalítico é o de um gerador reversível de um radical livre . A ligação C-Co (III) é fraca, com uma energia de dissociação = 109 kJ / mol, e parece ser ainda mais enfraquecida por meio de interações estéricas com a enzima. A reação homolítica é incomum na biologia, assim como a presença de uma ligação metal-carbono.
Metilmalonil-CoA mutase é um membro da subfamília isomerase de enzimas dependentes de adenosilcobalaminas. Além disso, é classificado como classe I, pois é uma enzima 'DMB-off' / 'His-on'. Isso se refere à natureza do cofator AdoCbl no sítio ativo do metilmalonil CoA. AdoCbl é composto por um anel corrin contendo cobalto central , um ligante axial superior (ligante axial β) e um ligante axial inferior (ligante axial α). Na metilmalonil-CoA mutase, o ligante β-axial 5'-desoxi-5'-adenosina dissocia-se reversivelmente para dar o radical desoxiadenosil . O ligante α-axial 5,6-dimetilbenzimidazol (DMB) está envolvido na organização do sítio ativo para permitir que a histidina -610 se ligue com Co, em vez de DMB (a razão para a notação 'DMB-off' / 'His-on' ) A ligação do resíduo de histidina-610 aumenta a taxa de quebra da ligação do ligante β-axial homolítico - Co por um fator de 10 12 .

Outros resíduos importantes da metilmalonil-CoA mutase incluem Histidina-244, que atua como um ácido geral próximo ao substrato e protege as espécies radicais de reações colaterais envolvendo oxigênio, Glutamato -370, cuja ligação de hidrogênio com o grupo 2'-OH da ribose do ligando axial β força a interação entre as espécies de radicais do ligante axial β e o substrato, e tirosina -89 que estabiliza intermediários de radicais reativos e é responsável pela estereosseletividade da enzima.
A proteína de processamento, a proteína MMAA , desempenha o importante papel de auxiliar no carregamento e na troca de cofator. A proteína MMAA favorece a associação com a apoenzima MCM e permite a transferência do cofator AdoCbl para o sítio ativo da enzima. Além disso, se o AdoCbl ligado acumula dano oxidativo durante o funcionamento normal, a proteína MMAA promove a troca do cofator danificado por um novo AdoCbl por meio de uma via dependente de GTP .
Interações
Referências
Leitura adicional
- Ledley FD, Rosenblatt DS (1997). "Mutações na acidemia metilmalônica mut: correlações clínicas e enzimáticas". Mutação Humana . 9 (1): 1–6. doi : 10.1002 / (SICI) 1098-1004 (1997) 9: 1 <1 :: AID-HUMU1> 3.0.CO; 2-E . PMID 8990001 .
- Ludwig ML, Matthews RG (1997). "Perspectivas baseadas na estrutura em enzimas dependentes de B12". Revisão Anual de Bioquímica . 66 : 269–313. doi : 10.1146 / annurev.biochem.66.1.269 . PMID 9242908 .
- Lubrano R, Elli M, Rossi M, Travasso E, Raggi C, Barsotti P, Carducci C, Berloco P (agosto de 2007). “Transplante renal na acidemia metilmalônica: poderia ser a melhor opção? Relato de um caso aos 10 anos e revisão da literatura”. Nefrologia Pediátrica . 22 (8): 1209–14. doi : 10.1007 / s00467-007-0460-z . PMID 17401587 . S2CID 24610554 .
- Frenkel EP, Kitchens RL (dezembro de 1975). "Localização intracelular de propionil-CoA carboxilase hepática e metilmalonil-CoA mutase em humanos e ratos normais e com deficiência de vitamina B12". British Journal of Hematology . 31 (4): 501–13. doi : 10.1111 / j.1365-2141.1975.tb00885.x . PMID 24458 . S2CID 1232083 .
- Crane AM, Jansen R, Andrews ER, Ledley FD (fevereiro de 1992). "Clonagem e expressão de uma mutase metilmalonil coenzima A mutase com afinidade de cobalamina alterada que causa acidúria mutmetilmalônica" . The Journal of Clinical Investigation . 89 (2): 385–91. doi : 10.1172 / JCI115597 . PMC 442864 . PMID 1346616 .
- Crane AM, Martin LS, Valle D, Ledley FD (maio de 1992). "Fenótipo da doença em três pacientes com mutações idênticas na metilmalonil CoA mutase". Genética Humana . 89 (3): 259–64. doi : 10.1007 / BF00220536 . PMID 1351030 . S2CID 5624280 .
- Raff ML, Crane AM, Jansen R, Ledley FD, Rosenblatt DS (janeiro de 1991). "Caracterização genética de uma mutação no locus MUT discriminando heterogeneidade em mut0 e mut-acidúria metilmalônica por complementação interalélica" . The Journal of Clinical Investigation . 87 (1): 203–7. doi : 10.1172 / JCI114972 . PMC 295026 . PMID 1670635 .
- Jansen R, Ledley FD (novembro de 1990). "Mutações heterozigotas no locus mut em fibroblastos com acidemia metilmalônica mut0 identificada por clonagem de cDNA por reação em cadeia da polimerase" . American Journal of Human Genetics . 47 (5): 808–14. PMC 1683687 . PMID 1977311 .
- Nham SU, Wilkemeyer MF, Ledley FD (dezembro de 1990). "Estrutura do locus humano metilmalonil-CoA mutase (MUT)". Genômica . 8 (4): 710–6. doi : 10.1016 / 0888-7543 (90) 90259-W . PMID 1980486 .
- Ledley FD, Lumetta M, Nguyen PN, Kolhouse JF, Allen RH (maio de 1988). "Molecular cloning of L-methylmalonyl-CoA mutase: gene transfer and analysis of mut cell lines" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 85 (10): 3518–21. Bibcode : 1988PNAS ... 85.3518L . doi : 10.1073 / pnas.85.10.3518 . PMC 280243 . PMID 2453061 .
- Jansen R, Kalousek F, Fenton WA, Rosenberg LE, Ledley FD (fevereiro de 1989). "Clonagem de metilmalonil-CoA mutase de comprimento total de uma biblioteca de cDNA usando a reação em cadeia da polimerase". Genômica . 4 (2): 198–205. doi : 10.1016 / 0888-7543 (89) 90300-5 . PMID 2567699 .
- Fenton WA, Hack AM, Kraus JP, Rosenberg LE (março de 1987). "Estudos imunoquímicos de fibroblastos de pacientes com deficiência de apoenzima metilmalonil-CoA mutase: detecção de uma mutação que interfere com a importação mitocondrial" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 84 (5): 1421–4. Bibcode : 1987PNAS ... 84.1421F . doi : 10.1073 / pnas.84.5.1421 . PMC 304442 . PMID 2881300 .
- Zoghbi HY, O'Brien WE, Ledley FD (novembro de 1988). "Relações de ligação da mutase metilmalonil CoA humana aos loci HLA e D6S4 no cromossomo 6". Genômica . 3 (4): 396–8. doi : 10.1016 / 0888-7543 (88) 90135-8 . PMID 2907507 .
- Kolhouse JF, Utley C, Allen RH (abril de 1980). "Isolamento e caracterização da mutase metilmalonil-CoA da placenta humana" . The Journal of Biological Chemistry . 255 (7): 2708–12. doi : 10.1016 / S0021-9258 (19) 85795-2 . PMID 6102092 .
- Fenton WA, Hack AM, Willard HF, Gertler A, Rosenberg LE (abril de 1982). "Purificação e propriedades de metilmalonil coenzima A mutase de fígado humano". Arquivos de Bioquímica e Biofísica . 214 (2): 815–23. doi : 10.1016 / 0003-9861 (82) 90088-1 . PMID 6124211 .
- Qureshi AA, Crane AM, Matiaszuk NV, Rezvani I, Ledley FD, Rosenblatt DS (abril de 1994). "Clonagem e expressão de mutações demonstrando complementação intragênica na acidúria metilmalônica mut0" . The Journal of Clinical Investigation . 93 (4): 1812–9. doi : 10.1172 / JCI117166 . PMC 294249 . PMID 7909321 .
- Crane AM, Ledley FD (julho de 1994). "Clustering of mutations in methylmalonyl CoA mutase associated with mut-methylmalonic acidemia" . American Journal of Human Genetics . 55 (1): 42–50. PMC 1918235 . PMID 7912889 .
- Janata J, Kogekar N, Fenton WA (setembro de 1997). "Expressão e caracterização cinética de metilmalonil-CoA mutase de pacientes com o mut-fenótipo: evidência de complementação interalélica de ocorrência natural" . Human Molecular Genetics . 6 (9): 1457–64. doi : 10.1093 / hmg / 6.9.1457 . PMID 9285782 .
links externos
- GeneReviews / NIH / NCBI / UW entrada na Acidemia Metilmalônica
- Metilmalonil-CoA + Mutase nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)