Ácido malônico - Malonic acid
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Ácido malônico
|
|
|
Nome IUPAC preferido
Ácido propanodioico |
|
| Outros nomes
Ácido metanodicarboxílico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100,005,003 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 3 H 4 O 4 | |
| Massa molar | 104,061 g · mol −1 |
| Densidade | 1,619 g / cm 3 |
| Ponto de fusão | 135 a 137 ° C (275 a 279 ° F; 408 a 410 K) (se decompõe) |
| Ponto de ebulição | decompõe-se |
| 763 g / L | |
| Acidez (p K a ) | pK a1 = 2,83 pK a2 = 5,69 |
| -46,3 · 10 −6 cm 3 / mol | |
| Compostos relacionados | |
|
Outros ânions
|
Malonate |
|
Ácidos carboxílicos relacionados
|
Ácido oxálico Ácido propiônico Ácido succínico Ácido fumárico |
|
Compostos relacionados
|
Malondialdeído Dimetil malonato |
| Perigos | |
| Ficha de dados de segurança | MSDS externo |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
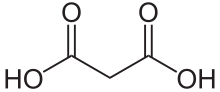
O ácido malônico ( nome sistemático IUPAC : ácido propanodioico ) é um ácido dicarboxílico com estrutura CH 2 (COOH) 2 . A forma ionizada do ácido malônico, assim como seus ésteres e sais , são conhecidos como malonatos . Por exemplo, o malonato dietílico é o éster dietílico do ácido malônico . A denominação tem origem do grego palavra μᾶλον ( Malon ) que significa 'maçã'.
História
O ácido malônico é uma substância natural encontrada em muitas frutas e vegetais. Há uma sugestão de que frutas cítricas produzidas na agricultura orgânica contêm níveis mais elevados de ácido malônico do que frutas produzidas na agricultura convencional.
O ácido malônico foi preparado pela primeira vez em 1858 pelo químico francês Victor Dessaignes por meio da oxidação do ácido málico .
Estrutura e preparação
A estrutura foi determinada por raios-X cristalografia e extensos dados de propriedades, incluindo para termoquímica fase condensada estão disponíveis no Instituto Nacional de Padrões e Tecnologia . Uma preparação clássica de ácido malônico começa com ácido cloroacético :

O carbonato de sódio gera o sal de sódio , que então reage com o cianeto de sódio para fornecer o sal de sódio do ácido cianoacético por meio de uma substituição nucleofílica . O grupo nitrila pode ser hidrolisado com hidróxido de sódio em malonato de sódio e a acidificação fornece ácido malônico. Industrialmente, no entanto, o ácido malônico é produzido pela hidrólise do malonato de dimetila ou malonato de dietila . Também foi produzido através da fermentação da glicose.
Reações orgânicas
O ácido malônico reage como um ácido carboxílico típico: formando derivados de amida , éster, anidrido e cloreto . O anidrido malônico pode ser usado como um intermediário para derivados de monoéster ou amida, enquanto o cloreto de malonila é mais útil para obter diésteres ou diamidas. Em uma reação bem conhecida, o ácido malônico se condensa com a uréia para formar o ácido barbitúrico . O ácido malônico também pode ser condensado com acetona para formar o ácido de Meldrum , um intermediário versátil em transformações posteriores. Os ésteres de ácido malónico são também utilizados como um - CH 2 COOH sintão na síntese de éster malónico .
Além disso, o derivado da coenzima A do malonato, malonil-CoA , é um importante precursor na biossíntese de ácidos graxos junto com a acetil CoA . O malonil CoA é formado a partir da acetil CoA pela ação da acetil-CoA carboxilase , e o malonato é transferido para uma proteína transportadora de acila para ser adicionado a uma cadeia de ácido graxo.
Reação de Briggs – Rauscher
O ácido malônico é um componente chave na reação de Briggs – Rauscher , o exemplo clássico de uma reação química oscilante .
Condensação Knoevenagel
Na condensação de Knoevenagel , o ácido malônico ou seus diésteres reagem com o grupo carbonila de um aldeído ou cetona , seguido por uma reação de desidratação .
Quando o próprio ácido malônico é utilizado, normalmente é porque o produto desejado é aquele em que ocorreu uma segunda etapa, com perda de dióxido de carbono , na chamada modificação de Doebner .
Assim, por exemplo, o produto da reação de acroleína e ácido malônico em piridina é ácido trans-2,4-pentadienóico com um grupo de ácido carboxílico e não dois.
Preparação de subóxido de carbono
O subóxido de carbono é preparado aquecendo uma mistura seca de pentóxido de fósforo ( P
4O
10) e ácido malônico. Ele reage de maneira semelhante ao anidrido malônico , formando malonatos.
Formulários
O ácido malônico é um precursor de poliésteres especiais . Ele pode ser convertido em 1,3-propanodiol para uso em poliésteres e polímeros e um tamanho de mercado projetado de US $ 621,2 milhões até 2021. Também pode ser um componente em resinas alquídicas , que são usadas em várias aplicações de revestimentos para proteção contra danos causada por luz ultravioleta, oxidação e corrosão. Uma aplicação do ácido malônico é na indústria de tintas como reticulador para tintas em pó de cura em baixa temperatura, que estão se tornando cada vez mais valiosas para substratos sensíveis ao calor e um desejo de acelerar o processo de tintas. O mercado global de revestimentos para automóveis foi estimado em US $ 18,59 bilhões em 2014, com taxa de crescimento anual combinada projetada de 5,1% até 2022.
É usado em vários processos de fabricação como uma especialidade química de alto valor, incluindo a indústria eletrônica , indústria de aromas e fragrâncias, solventes especiais, reticulação de polímero e indústria farmacêutica. Em 2004, a produção global anual de ácido malônico e diésteres relacionados foi de mais de 20.000 toneladas métricas. O crescimento potencial desses mercados pode resultar de avanços na biotecnologia industrial que busca substituir produtos químicos à base de petróleo em aplicações industriais.
O ácido malônico foi listado como um dos 30 principais produtos químicos a serem produzidos a partir de biomassa pelo Departamento de Energia dos Estados Unidos.
Em aplicações de alimentos e medicamentos, o ácido malônico pode ser usado para controlar a acidez, seja como um excipiente em formulações farmacêuticas ou como um aditivo conservante natural para alimentos.
O ácido malônico é usado como um bloco de construção químico para produzir vários compostos valiosos, incluindo os compostos de aroma e fragrância gama-nonalactona, ácido cinâmico e o composto farmacêutico valproato .
O ácido malônico (até 37,5% p / p) tem sido usado para reticular amidos de milho e batata para produzir um termoplástico biodegradável; o processo é realizado em água usando catalisadores não tóxicos. Os polímeros à base de amido representaram 38% do mercado global de polímeros biodegradáveis em 2014, com embalagens para alimentos, embalagens de espuma e sacos de compostagem como os maiores segmentos de uso final.
A empresa Eastman Kodak e outras empresas usam ácido malônico e derivados como adesivo cirúrgico.
Bioquímica
O ácido malônico é o exemplo clássico de inibidor competitivo da enzima succinato desidrogenase (complexo II), na cadeia de transporte de elétrons respiratórios . Ele se liga ao sítio ativo da enzima sem reagir, competindo com o substrato succinato usual, mas sem o grupo −CH 2 CH 2 - necessário para a desidrogenação. Esta observação foi usada para deduzir a estrutura do sítio ativo na succinato desidrogenase. A inibição desta enzima diminui a respiração celular. Como o ácido malônico é um componente natural de muitos alimentos, ele está presente em mamíferos, incluindo humanos.
Sais e ésteres
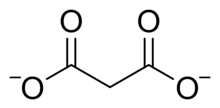
O ácido malônico é diprótico ; ou seja, pode doar dois prótons por molécula. O primeiro é 2,8 e o segundo é 5,7. Assim, o íon malonato pode ser H O O C CH
2COO - ou C H
2(C O O)2−
2. Compostos de malonato ou propanodioato incluem sais e ésteres de ácido malônico, tais como



