Cristalografia - Crystallography
Cristalografia é a ciência experimental que determina o arranjo dos átomos em sólidos cristalinos (ver estrutura cristalina ). A palavra "cristalografia" deriva das palavras gregas crystalon "gota fria, gota congelada", com seu significado estendendo-se a todos os sólidos com algum grau de transparência, e graphein "escrever". Em julho de 2012, as Nações Unidas reconheceram a importância da ciência da cristalografia ao proclamar que 2014 seria o Ano Internacional da Cristalografia.
Antes do desenvolvimento da cristalografia por difração de raios-X (veja abaixo), o estudo dos cristais era baseado em medições físicas de sua geometria usando um goniômetro . Isso envolvia medir os ângulos das faces do cristal em relação umas às outras e aos eixos de referência teórica (eixos cristalográficos), e estabelecer a simetria do cristal em questão. A posição no espaço 3D de cada face de cristal é plotada em uma rede estereográfica, como uma rede Wulff ou uma rede Lambert . O pólo de cada face é traçado na rede. Cada ponto é rotulado com seu índice de Miller . O gráfico final permite que a simetria do cristal seja estabelecida.
Os métodos cristalográficos agora dependem da análise dos padrões de difração de uma amostra visada por um feixe de algum tipo. Os raios X são os mais comumente usados; outros feixes usados incluem elétrons ou nêutrons . Os cristalógrafos freqüentemente declaram explicitamente o tipo de feixe usado, como nos termos cristalografia de raios X , difração de nêutrons e difração de elétrons . Esses três tipos de radiação interagem com o espécime de maneiras diferentes.
- Os raios X interagem com a distribuição espacial dos elétrons na amostra.
- Os elétrons são partículas carregadas e, portanto, interagem com a distribuição de carga total dos núcleos atômicos e dos elétrons da amostra.
- Os nêutrons são espalhados pelos núcleos atômicos por meio das forças nucleares fortes , mas, além disso, o momento magnético dos nêutrons é diferente de zero. Portanto, eles também são espalhados por campos magnéticos . Quando nêutrons são dispersos de materiais contendo hidrogênio , eles produzem padrões de difração com altos níveis de ruído. No entanto, o material às vezes pode ser tratado para substituir o hidrogênio por deutério .
Por causa dessas diferentes formas de interação, os três tipos de radiação são adequados para diferentes estudos cristalográficos.
Teoria
| Física de matéria condensada |
|---|
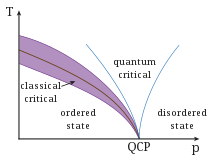 |
| Fases · Transição de fase · QCP |
Com técnicas convencionais de imagem, como microscopia óptica , a obtenção de uma imagem de um pequeno objeto requer a coleta de luz com uma lente de aumento . A resolução de qualquer sistema óptico é limitada pelo limite de difração da luz, que depende de seu comprimento de onda. Assim, a clareza geral dos mapas de densidade de elétrons cristalográficos resultantes é altamente dependente da resolução dos dados de difração, que podem ser categorizados como: baixo, médio, alto e atômico. Por exemplo, a luz visível tem um comprimento de onda de cerca de 4000 a 7000 ångström , que é três ordens de magnitude maior do que o comprimento das ligações atômicas típicas e dos próprios átomos (cerca de 1 a 2 Å). Portanto, um microscópio óptico convencional não pode resolver o arranjo espacial dos átomos em um cristal. Para fazer isso, precisaríamos de radiação com comprimentos de onda muito mais curtos, como raios-X ou feixes de nêutrons.
Infelizmente, focar os raios X com lentes ópticas convencionais pode ser um desafio. Os cientistas tiveram algum sucesso focalizando os raios X com placas microscópicas da zona de Fresnel feitas de ouro e por reflexão de ângulo crítico dentro de longos capilares cônicos. Raios-X difratados ou feixes de nêutrons não podem ser focados para produzir imagens, então a estrutura da amostra deve ser reconstruída a partir do padrão de difração .
Os padrões de difração surgem da interferência construtiva da radiação incidente (raios-x, elétrons, nêutrons), espalhada pelas características periódicas e repetitivas da amostra. Por causa de sua estrutura atômica altamente ordenada e repetitiva ( rede de Bravais ), os cristais difratam os raios X de maneira coerente, também conhecida como reflexo de Bragg.
Notação
- Coordenadas em quadrados suportes , tais como [100] denotam um vector de direcção (no espaço real).
- As coordenadas entre colchetes angulares ou divisas , como <100>, denotam uma família de direções relacionadas por operações de simetria. No sistema de cristal cúbico , por exemplo, <100> significaria [100], [010], [001] ou o negativo de qualquer uma dessas direções.
- Índices de Miller entre parênteses como (100) denotam um plano da estrutura cristalina e repetições regulares desse plano com um espaçamento particular. No sistema cúbico, o normal ao plano (hkl) é a direção [hkl], mas em casos de simetria inferior, o normal a (hkl) não é paralelo a [hkl].
- Índices entre colchetes ou chaves , como {100}, denotam uma família de planos e seus normais. Em materiais cúbicos, a simetria os torna equivalentes, assim como os colchetes angulares denotam uma família de direções. Em materiais não cúbicos, <hkl> não é necessariamente perpendicular a {hkl}.
Técnicas
Alguns materiais que foram analisados cristalograficamente, como proteínas , não ocorrem naturalmente como cristais. Normalmente, essas moléculas são colocadas em solução e cristalizadas lentamente por meio da difusão de vapor . Uma gota de solução contendo a molécula, tampão e precipitantes é selada em um recipiente com um reservatório contendo uma solução higroscópica . A água na gota se espalha para o reservatório, aumentando lentamente a concentração e permitindo a formação de um cristal. Se a concentração aumentasse mais rapidamente, a molécula simplesmente precipitaria da solução, resultando em grânulos desordenados, em vez de um cristal ordenado e, portanto, utilizável.
Uma vez que um cristal é obtido, os dados podem ser coletados usando um feixe de radiação. Embora muitas universidades que se dedicam à pesquisa cristalográfica tenham seus próprios equipamentos de produção de raios-X, os síncrotrons são frequentemente usados como fontes de raios-X, devido aos padrões mais puros e completos que essas fontes podem gerar. As fontes síncrotron também têm uma intensidade muito maior de feixes de raios-X, de modo que a coleta de dados leva uma fração do tempo normalmente necessário em fontes mais fracas. Técnicas complementares de cristalografia de nêutrons são usadas para identificar as posições dos átomos de hidrogênio, uma vez que os raios X interagem muito fracamente com elementos leves como o hidrogênio.
Produzir uma imagem a partir de um padrão de difração requer matemática sofisticada e muitas vezes um processo iterativo de modelagem e refinamento. Nesse processo, os padrões de difração previstos matematicamente de uma estrutura hipotética ou "modelo" são comparados ao padrão real gerado pela amostra cristalina. Idealmente, os pesquisadores fazem várias suposições iniciais, que, por meio do refinamento, convergem todas para a mesma resposta. Os modelos são refinados até que seus padrões previstos correspondam ao máximo que possa ser alcançado sem uma revisão radical do modelo. Este é um processo meticuloso, muito mais fácil hoje em dia pelos computadores.
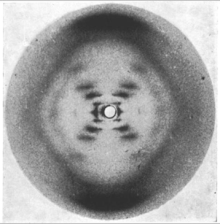
Os métodos matemáticos para a análise de dados de difração só se aplicam a padrões, que por sua vez resultam apenas quando as ondas difratam de matrizes ordenadas. Conseqüentemente, a cristalografia se aplica em sua maior parte apenas a cristais ou a moléculas que podem ser induzidas a cristalizar para fins de medição. Apesar disso, uma certa quantidade de informação molecular pode ser deduzida de padrões gerados por fibras e pós , que embora não sejam tão perfeitos quanto um cristal sólido, podem apresentar certo grau de ordem. Este nível de ordem pode ser suficiente para deduzir a estrutura de moléculas simples ou para determinar as características grosseiras de moléculas mais complicadas. Por exemplo, a estrutura em dupla hélice do DNA foi deduzida de um padrão de difração de raios-X gerado por uma amostra fibrosa.
Ciência de materiais
A cristalografia é usada por cientistas de materiais para caracterizar diferentes materiais. Em cristais únicos, os efeitos do arranjo cristalino dos átomos costumam ser fáceis de ver macroscopicamente, porque as formas naturais dos cristais refletem a estrutura atômica. Além disso, as propriedades físicas são frequentemente controladas por defeitos cristalinos. A compreensão das estruturas cristalinas é um pré-requisito importante para a compreensão dos defeitos cristalográficos . Na maioria das vezes, os materiais não ocorrem como um único cristal, mas na forma policristalina (ou seja, como um agregado de pequenos cristais com diferentes orientações). Devido a isso, o método de difração de pó , que obtém padrões de difração de amostras policristalinas com um grande número de cristais, desempenha um papel importante na determinação estrutural.
Outras propriedades físicas também estão ligadas à cristalografia. Por exemplo, os minerais na argila formam estruturas pequenas, planas e semelhantes a placas. A argila pode ser facilmente deformada porque as partículas em forma de placa podem deslizar umas ao longo das outras no plano das placas, embora permaneçam fortemente conectadas na direção perpendicular às placas. Esses mecanismos podem ser estudados por medições de textura cristalográfica .
Em outro exemplo, o ferro se transforma de uma estrutura cúbica centrada no corpo (bcc) chamada ferrita em uma estrutura cúbica centrada na face (fcc) chamada austenita quando é aquecida. A estrutura fcc é uma estrutura compacta, ao contrário da estrutura bcc; assim, o volume do ferro diminui quando essa transformação ocorre.
A cristalografia é útil na identificação de fases. Ao fabricar ou usar um material, geralmente é desejável saber quais compostos e quais fases estão presentes no material, pois sua composição, estrutura e proporções irão influenciar as propriedades do material. Cada fase possui um arranjo característico de átomos. A difração de raios-X ou de nêutrons pode ser usada para identificar quais padrões estão presentes no material e, portanto, quais compostos estão presentes. A cristalografia abrange a enumeração dos padrões de simetria que podem ser formados por átomos em um cristal e, por isso, está relacionada à teoria dos grupos .
Biologia
A cristalografia de raios-X é o principal método para determinar as conformações moleculares de macromoléculas biológicas , particularmente proteínas e ácidos nucléicos como DNA e RNA . Na verdade, a estrutura em dupla hélice do DNA foi deduzida de dados cristalográficos. A primeira estrutura cristalina de uma macromolécula foi resolvida em 1958, um modelo tridimensional da molécula de mioglobina obtido por análise de raios-X. O Protein Data Bank (PDB) é um repositório de livre acesso para as estruturas de proteínas e outras macromoléculas biológicas. Programas de computador como RasMol , Pymol ou VMD podem ser usados para visualizar estruturas moleculares biológicas. A cristalografia de nêutrons é freqüentemente usada para ajudar a refinar estruturas obtidas por métodos de raios X ou para resolver uma ligação específica; os métodos são frequentemente vistos como complementares, já que os raios X são sensíveis às posições dos elétrons e se espalham mais fortemente nos átomos pesados, enquanto os nêutrons são sensíveis às posições do núcleo e se espalham fortemente até mesmo em muitos isótopos leves, incluindo hidrogênio e deutério. A cristalografia de elétrons tem sido usada para determinar algumas estruturas de proteínas, principalmente proteínas de membrana e capsídeos virais .
Contribuição das mulheres para a cristalografia de raios-X
Várias mulheres foram pioneiras na cristalografia de raios X numa época em que foram excluídas da maioria dos outros ramos da ciência física.
Kathleen Lonsdale foi uma estudante pesquisadora de William Henry Bragg , que com seu filho Lawrence fundou a ciência da cristalografia de raios X no início do século XX. Bragg tinha 11 mulheres estudantes de pesquisa de um total de 18. Kathleen juntou-se à sua equipe de pesquisa em cristalografia no Royal Institution de Londres em 1923 e, depois de se casar e ter filhos, voltou a trabalhar com Bragg como pesquisadora. Ela confirmou a estrutura do anel de benzeno, realizou estudos de diamante, foi uma das duas primeiras mulheres a ser eleita para a Royal Society em 1945, e em 1949 foi nomeada a primeira professora titular de química e chefe do Departamento de cristalografia na University College London . Kathleen sempre defendeu uma maior participação das mulheres na ciência e disse em 1970: "Qualquer país que queira fazer uso total de todo o seu potencial de cientistas e tecnólogos poderia fazê-lo, mas não deve esperar obter as mulheres tão simplesmente como obtém o homens ... É utópico, então, sugerir que qualquer país que realmente deseja que as mulheres casadas retornem à carreira científica, quando seus filhos não precisam mais de sua presença física, deva fazer arranjos especiais para encorajá-la a fazê-lo? " . Durante este período, Kathleen iniciou uma colaboração com William T. Astbury em um conjunto de 230 tabelas de grupos espaciais que foi publicado em 1924 e se tornou uma ferramenta essencial para cristalógrafos.
Em 1932 Dorothy Hodgkin ingressou no laboratório do físico John Desmond Bernal, ex-aluno de Bragg, em Cambridge, no Reino Unido. Ela e Bernal tiraram as primeiras fotos de raios-X de proteínas cristalinas. Ela recebeu o Prêmio Nobel de Química em 1964 por seu trabalho usando técnicas de raios-X para estudar as estruturas da penicilina, insulina e vitamina B12. Ela é a única mulher britânica que já ganhou um Prêmio Nobel em uma disciplina de ciências.
Rosalind Franklin tirou a fotografia de raios-X de uma fibra de DNA que provou ser a chave para a descoberta da dupla hélice por James Watson e Francis Crick , pela qual ambos ganharam o Prêmio Nobel de Fisiologia ou Medicina em 1962. Watson revelou em seu relato autobiográfico da descoberta da estrutura do DNA, The Double Helix , que ele havia usado a fotografia de raios-X de Rosalind sem sua permissão. Franklyn morreu de câncer na casa dos 30 anos, antes de Watson receber o Prêmio Nobel. Franklyn também realizou estudos estruturais importantes de carbono em carvão e grafite, e de vírus de plantas e animais.
Isabella Karle, do Laboratório de Pesquisa Naval dos Estados Unidos, desenvolveu uma abordagem experimental da teoria matemática da cristalografia. Seu trabalho melhorou a velocidade e a precisão das análises químicas e biomédicas. No entanto, apenas seu marido Jerome compartilhou o Prêmio Nobel de Química de 1985 com Herbert Hauptman, "por realizações notáveis no desenvolvimento de métodos diretos para a determinação de estruturas cristalinas". Outros organismos de entrega de prêmios cobriram Isabella com prêmios em seu próprio direito.
As mulheres escreveram muitos livros didáticos e trabalhos de pesquisa no campo da cristalografia de raios-X. Por muitos anos, Lonsdale editou as International Tables for Crystallography , que fornecem informações sobre redes cristalinas, simetria e grupos espaciais, bem como dados matemáticos, físicos e químicos sobre estruturas. Olga Kennard, da University of Cambridge, fundou e dirigiu o Cambridge Crystallographic Data Center , uma fonte internacionalmente reconhecida de dados estruturais sobre pequenas moléculas, de 1965 a 1997. Jenny Pickworth Glusker , uma cientista britânica, é co-autora de Crystal Structure Analysis: A Primer , publicado pela primeira vez em 1971 e a partir de 2010 em sua terceira edição. Eleanor Dodson , uma bióloga australiana que começou como técnica de Dorothy Hodgkin, foi a principal instigadora por trás do CCP4 , o projeto de computação colaborativa que atualmente compartilha mais de 250 ferramentas de software com cristalógrafos de proteínas em todo o mundo.
Literatura de referência
The International Tables for Crystallography é uma série de oito livros que descreve as notações padrão para formatar, descrever e testar cristais. A série contém livros que abrangem métodos de análise e procedimentos matemáticos para determinar a estrutura orgânica por meio de cristalografia de raios-X, difração de elétrons e difração de nêutrons. As tabelas internacionais são focadas em procedimentos, técnicas e descrições e não listam as propriedades físicas dos próprios cristais. Cada livro tem cerca de 1000 páginas e os títulos dos livros são:
- Vol A - Simetria de Grupo Espacial ,
- Vol A1 - Relações de simetria entre grupos espaciais ,
- Vol B - Espaço Recíproco ,
- Vol C - Tabelas Matemáticas, Físicas e Químicas ,
- Vol D - Propriedades Físicas dos Cristais ,
- Vol E - Grupos Subperiódicos ,
- Vol F - Cristalografia de macromoléculas biológicas , e
- Vol G - Definição e Troca de Dados Cristalográficos .
Cientistas importantes
- William Astbury
- William Barlow
- C. Arnold Beevers
- John Desmond Bernal
- William Henry Bragg
- William Lawrence Bragg
- Auguste Bravais
- Glenn H. Brown
- Martin Julian Buerger
- Francis Crick
- Pierre Curie
- Peter Debye
- Johann Deisenhofer
- Boris Delone
- Gautam R. Desiraju
- Eleanor Dodson
- Jack Dunitz
- David Eisenberg
- Paul Peter Ewald
- Evgraf Stepanovich Fedorov
- Rosalind Franklin
- Georges Friedel
- Jenny Glusker
- Paul Heinrich von Groth
- Herbert A. Hauptman
- René Just Haüy
- Wayne Hendrickson
- Carl Hermann
- Johann Friedrich Christian Hessel
- Dorothy Crowfoot Hodgkin
- Judith Howard
- Robert Huber
- Louise Johnson
- Isabella Karle
- Jerome Karle
- Olga Kennard
- Aaron Klug
- Max von Laue
- Otto Lehmann
- Michael Levitt
- Henry Lipson
- Kathleen Lonsdale
- Ernest-François Mallard
- Charles-Victor Mauguin
- William Hallowes Miller
- Friedrich Mohs
- Paul Niggli
- Louis Pasteur
- Arthur Lindo Patterson
- Max Perutz
- Friedrich Reinitzer
- Hugo Rietveld
- Jean-Baptiste L. Romé de l'Isle
- Michael Rossmann
- Paul Scherrer
- Arthur Moritz Schönflies
- Dan Shechtman
- George M. Sheldrick
- Tej P. Singh
- Nicolas Steno
- Constance Tipper
- Daniel Vorländer
- Christian Samuel Weiss
- Don Craig Wiley
- Michael Woolfson
- Ralph Walter Graystone Wyckoff
- Ada Yonath
Veja também
- Crescimento anormal de grãos
- Fator de empacotamento atômico
- Beevers-tira Lipson
- Física de matéria condensada
- Engenharia de cristal
- Crescimento de cristal
- Ótica de cristal
- Estrutura de cristal
- Cristalite
- Processos de cristalização
- Banco de dados cristalográfico
- Grupo de pontos cristalográficos
- Grupo Cristalográfico
- Teoria dinâmica da difração
- Cristalografia de elétrons
- Isometria de plano euclidiano
- Pontos fixos de grupos de isometria no espaço euclidiano
- Coordenadas fracionárias
- Ação em grupo
- Ano Internacional da Cristalografia
- Crescimento do pedestal aquecido a laser
- Ciência de materiais
- Metalurgia
- Mineralogia
- Modelagem de cristais de polímero
- Cristalografia de nêutrons
- Difração de nêutrons em OPAL
- Difração de nêutrons no ILL
- Cristalografia NMR
- Grupo de permutação
- Grupo de pontos
- Difração de elétrons de precessão
- Mineralogia quântica
- Quasicristal
- Química de estado sólido
- Grupo espacial
- Grupo simétrico
- Cristalografia de raio-x
- Estrutura constante
Referências
links externos
- American Crystallographic Association
- Aprendendo Cristalografia
- Estruturas de rede de cristal
- 100 anos de cristalografia animação da Royal Institution
- Entrevistas da Vega Science Trust em Crystallography Freeview vídeo entrevistas com Max Perutz, Rober Huber e Aaron Klug.
- Comissão de Ensino Cristalográfico, Panfletos
- Laboratório de Ames, recursos de pesquisa de cristalografia do US DOE
- União Internacional de Cristalografia
- Linha do tempo da cristalografia interativa da Royal Institution
- Marcos da natureza na cristalografia
- Cristalografia no século 21 (editorial na seção A da Acta Crystallographica)
- Cristalografia em In Our Time na BBC