Foldamer - Foldamer
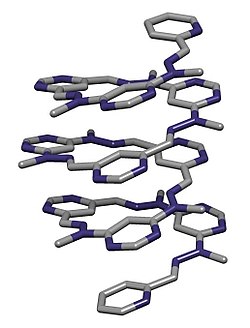
Em química , um dobrâmero é uma molécula de cadeia discreta ou oligômero que se dobra em um estado conformacionalmente ordenado em solução. Eles são moléculas artificiais que imitam a capacidade de proteínas , ácidos nucléicos e polissacarídeos se dobrarem em conformações bem definidas, como hélices e folhas β . A estrutura de um foldamer é estabilizada por interações não covalentes entre monômeros não adjacentes . As pastas são estudadas com o objetivo principal de projetar moléculas grandes com estruturas previsíveis. O estudo de dobrâmeros está relacionado aos temas de automontagem molecular, reconhecimento molecular e química hospedeiro-hóspede.
Projeto
As pastas podem variar em tamanho, mas são definidas pela presença de interações não covalentes e não adjacentes. Esta definição exclui moléculas como poli (isocianatos) (comumente conhecidos como ( poliuretano )) e poli (prolinas), uma vez que se dobram em hélices de forma confiável devido a interações covalentes adjacentes ., Os dobradores têm uma reação dinâmica de dobramento [desdobrado → dobrado], em que grande o dobramento macroscópico é causado por efeitos solvofóbicos (colapso hidrofóbico), enquanto o estado de energia final do dobrador dobrado é devido às interações não covalentes. Essas interações funcionam cooperativamente para formar a estrutura terciária mais estável, já que os estados completamente dobrado e desdobrado são mais estáveis do que qualquer estado parcialmente dobrado.
Previsão de dobramento
A estrutura de um dobrâmero pode frequentemente ser prevista a partir de sua sequência primária . Este processo envolve simulações dinâmicas dos equilíbrios de dobramento no nível atômico sob várias condições. Este tipo de análise pode ser aplicado a pequenas proteínas também, entretanto a tecnologia computacional é incapaz de simular todas as sequências, exceto as mais curtas.
A via de dobramento de um dobrador pode ser determinada medindo a variação da estrutura favorecida determinada experimentalmente sob diferentes condições termodinâmicas e cinéticas . A mudança na estrutura é medida calculando o desvio quadrático médio da raiz da posição atômica do backbone da estrutura favorecida. A estrutura do foldamer em diferentes condições pode ser determinada computacionalmente e, em seguida, verificada experimentalmente. Mudanças na temperatura, viscosidade do solvente , pressão , pH e concentração de sal podem gerar informações valiosas sobre a estrutura do dobrador. Medir a cinética de dobramento, bem como o equilíbrio de dobramento, permite observar os efeitos dessas diferentes condições na estrutura do dobrador.
O solvente freqüentemente influencia a dobradura. Por exemplo, uma via de dobramento envolvendo o colapso hidrofóbico se dobraria de maneira diferente em um solvente não polar. Essa diferença se deve ao fato de que diferentes solventes estabilizam diferentes intermediários da via de dobramento, bem como diferentes estruturas de dobrâmero finais com base em interações intermoleculares não covalentes.
Interações não covalentes
Interações intermoleculares não covalentes , embora individualmente pequenas, sua soma altera as reações químicas de maneiras importantes. Listadas abaixo estão as forças intermoleculares comuns que os químicos usaram para projetar as dobras.
- Ligações de hidrogênio (especialmente com ligações peptídicas )
- Empilhamento de Pi
- Efeitos solvofóbicos , que levam ao colapso hidrofóbico
- Forças de Van der Waals
- Atração Eletrostática
Designs comuns
As pastas são classificadas em três categorias diferentes: dobras peptidomiméticas , dobras nucleotidomiméticas e dobras abióticas. As dobras peptidomiméticas são moléculas sintéticas que mimetizam a estrutura das proteínas, enquanto as dobras nucleotidomiméticas são baseadas nas interações em ácidos nucléicos. As dobras abióticas são estabilizadas por interações aromáticas e de transferência de carga que geralmente não são encontradas na natureza. Os três designs descritos abaixo desviam-se da definição estrita de Moore de dobrador, que exclui dobradores helicoidais.
Peptidomimético
As dobras peptidomiméticas freqüentemente quebram a definição mencionada anteriormente de dobras, pois muitas vezes adotam estruturas helicoidais . Eles representam um marco importante na pesquisa do foldamer devido ao seu design e capacidades. Os maiores grupos de peptidomiméticos consistem em β - peptídeos , γ - peptídeos e δ - peptídeos, e as possíveis combinações monoméricas. Os aminoácidos desses peptídeos diferem apenas em um (β), dois (γ) ou três (δ) carbonos de metileno, mas as mudanças estruturais foram profundas. Estas sequências de peptídeos são altamente estudadas como o controle de sequência leva a uma previsão confiável de dobramento. Além disso, com vários carbonos de metileno entre os terminais carboxila e amino das ligações peptídicas flanqueadoras, cadeias laterais variáveis do grupo R podem ser projetadas. Um exemplo da novidade dos β-peptídeos pode ser visto nas descobertas de Reiser e colaboradores. Usando um heteroligopeptídeo que consiste em α-aminoácidos e ácidos cis-β-aminociclopropanocarboxulic (cis-β-ACCs) eles encontraram a formação de sequências helicoidais em oligômeros tão curtos quanto sete resíduos e conformação definida em cinco resíduos; uma qualidade única para peptídeos contendo β-aminoácidos cíclicos.
Nucleotidomimético
Os nucleotidomiméticos geralmente não se qualificam como dobradores. A maioria é projetada para imitar bases, nucleosídeos ou nucleotídeos simples de DNA, a fim de direcionar o DNA de forma não específica. Estes têm vários usos medicinais diferentes, incluindo aplicações anticâncer , antivirais e antifúngicas .
Abiótico
As dobras abióticas são, novamente, moléculas orgânicas projetadas para exibir dobramento dinâmico. Eles exploram uma ou algumas interações intermoleculares chave conhecidas, conforme otimizadas por seu design. Um exemplo são os oligopirróis que se organizam ao se ligar a ânions, como o cloreto, por meio de ligações de hidrogênio (veja a figura). O dobramento é induzido na presença de um ânion: os grupos polipirrol têm pouca restrição conformacional de outra forma.
Outros exemplos
- Os oligômeros de m- fenileno etinileno são levados a dobrar em uma conformação helicoidal por forças solvofóbicas e interações de empilhamento aromático .
-
β-peptídeos são compostos de aminoácidos contendo um CH adicional
2unidade entre a amina e o ácido carboxílico . Eles são mais estáveis à degradação enzimática e demonstraram ter atividade antimicrobiana. - Os peptoides são poliglicinas substituídas em N que utilizam interações estéricas para se dobrarem em estruturas helicoidais semelhantes a poliprolina tipo I.
- Aedâmeros que se dobram em soluções aquosas impulsionadas por interações de empilhamento hidrofóbico e aromático.
- Pastas aromáticas de oligoamida Estes exemplos são algumas das maiores e mais bem caracterizadas pastas estruturalmente.
- Dobrâmeros de arilamida, por exemplo Brilacidina
Referências
Leitura adicional
- Ivan Huc; Stefan Hecht (2007). Pastas: Estrutura, Propriedades e Aplicativos . Weinheim: Wiley-VCH. ISBN 978-3-527-31563-5.
- Goodman CM, Choi S, Shandler S, DeGrado WF (2007). "Foldamers como frameworks versáteis para o design e evolução da função" . Nat. Chem. Biol . 3 (5): 252–62. doi : 10.1038 / nchembio876 . PMC 3810020 . PMID 17438550 .
Avaliações
- ^ Gellman, SH (1998). "Pastas: um manifesto" (PDF) . Acc. Chem. Res . 31 (4): 173-180. doi : 10.1021 / ar960298r . Arquivado do original (PDF) em 13/05/2008.
- ^ Zhang DW, Zhao X, Hou JL, Li ZT (2012). "Pastas de amida aromática: estruturas, propriedades e funções". Chem. Rev . 112 (10): 5271–5316. doi : 10.1021 / cr300116k . PMID 22871167 .
- ^ Juwarker, H .; Jeong, KS. (2010). "Pastilhas controladas por ânion" . Chem. Soc. Rev . 39 (10): 3664–3674. doi : 10.1039 / b926162c . PMID 20730154 .



