Alfa-amilase - Alpha-amylase
| Alfa-amilase | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Identificadores | |||||||||
| EC nº | 3.2.1.0 | ||||||||
| CAS no. | 9000-90-2 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| Domínio catalítico GH13 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Ciclodextrina glucanotransferase (ec2.4.1.19) (cgtase)
| |||||||||
| Identificadores | |||||||||
| Símbolo | Alfa-amilase | ||||||||
| Pfam | PF00128 | ||||||||
| Clã Pfam | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| Superfamília OPM | 117 | ||||||||
| Proteína OPM | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
| |||||||||
| Domínio de folha beta alfa-amilase C-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
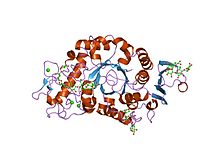 Estrutura de cristal da isoenzima 1 (amy1) mutante inativo da alfa-amilase da cevada d180a em complexo com maltoheptaose
| |||||||||
| Identificadores | |||||||||
| Símbolo | Alfa-amil_C2 | ||||||||
| Pfam | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
| |||||||||
| Alfa amilase, domínio totalmente beta C-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
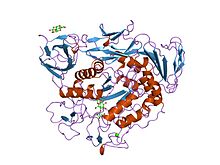 complexo de maltotriose da ciclodextrina glicosiltransferase mutante pré-condicionada
| |||||||||
| Identificadores | |||||||||
| Símbolo | Alfa-amilase_C | ||||||||
| Pfam | PF02806 | ||||||||
| Clã Pfam | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| |||||||||
Alfa-amilase , (α-amilase) é uma enzima EC 3.2.1.1 que hidrolisa ligações alfa de grandes polissacarídeos ligados a alfa , como amido e glicogênio , produzindo cadeias mais curtas dos mesmos, dextrinas e maltose . É a principal forma de amilase encontrada em humanos e outros mamíferos. Também está presente em sementes que contêm amido como reserva alimentar e é secretado por muitos fungos. É um membro da família da glicosídeo hidrolase 13 .
Em biologia humana
Embora encontrada em muitos tecidos, a amilase é mais proeminente no suco pancreático e na saliva , cada um dos quais tem sua própria isoforma de α-amilase humana. Eles se comportam de maneira diferente na focalização isoelétrica e também podem ser separados em testes usando anticorpos monoclonais específicos . Em humanos, todas as isoformas de amilase se ligam ao cromossomo 1p 21 (ver AMY1A ).
Amilase salivar (ptialina)
A amilase é encontrada na saliva e quebra o amido em maltose e dextrina . Esta forma de amilase é também chamado de "ptyalin" / t aɪ əl ɪ n / , que foi nomeado pelo químico sueco Jöns Jacob Berzelius . O nome deriva da palavra grega πτυω (eu cuspo), pois a substância foi obtida da saliva. Ele irá quebrar grandes moléculas de amido insolúveis em amidos solúveis ( amilodextrina , eritrodextrina e acrodextrina ) produzindo amidos sucessivamente menores e, por fim, maltose . A ptialina atua nas ligações lineares α (1,4) glicosídicas , mas a hidrólise do composto requer uma enzima que atua nos produtos ramificados. A amilase salivar é inativada no estômago pelo ácido gástrico . No suco gástrico ajustado para pH 3,3, a ptialina foi totalmente inativada em 20 minutos a 37 ° C. Em contraste, 50% da atividade da amilase permaneceu após 150 minutos de exposição ao suco gástrico em pH 4,3. Tanto o amido, substrato da ptialina, quanto o produto (cadeias curtas de glicose) são capazes de protegê-lo parcialmente contra a inativação pelo ácido gástrico. A ptialina adicionada ao tampão em pH 3,0 sofreu inativação completa em 120 minutos; no entanto, a adição de amido a um nível de 0,1% resultou em 10% da atividade restante, e a adição semelhante de amido a um nível de 1,0% resultou em cerca de 40% da atividade restante em 120 minutos.
Condições ideais para ptialina
- PH ótimo - 7,0
- Temperatura do corpo humano
- Presença de certos ânions e ativadores:
Variação genética na amilase salivar humana
O gene da amilase salivar sofreu duplicação durante a evolução, e estudos de hibridização de DNA indicam que muitos indivíduos têm múltiplas repetições em tandem do gene. O número de cópias do gene se correlaciona com os níveis de amilase salivar, conforme medido por ensaios de blot de proteína usando anticorpos para amilase humana. O número de cópias do gene está associado à aparente exposição evolutiva a dietas ricas em amido. Por exemplo, um indivíduo japonês tinha 14 cópias do gene da amilase (um alelo com 10 cópias e um segundo alelo com quatro cópias). A dieta japonesa tradicionalmente contém grandes quantidades de amido de arroz . Em contraste, um indivíduo Biaka carregava seis cópias (três cópias em cada alelo). Os Biaka são caçadores-coletores da floresta tropical que tradicionalmente consumiam uma dieta pobre em amido. Perry e seus colegas especularam que o aumento do número de cópias do gene da amilase salivar pode ter aumentado a sobrevivência coincidente com uma mudança para uma dieta rica em amido durante a evolução humana.
Amilase pancreática
A α-amilase pancreática cliva aleatoriamente as ligações α (1-4) glicosídicas da amilose para produzir dextrina , maltose ou maltotriose . Adota um mecanismo de duplo deslocamento com retenção da configuração anomérica . Em humanos, a amilase salivar evoluiu de uma cópia dela.
Em patologia
O teste para amilase é mais fácil de realizar do que para lipase , tornando-o o principal teste usado para detectar e monitorar a pancreatite . Os laboratórios médicos geralmente medem a amilase pancreática ou a amilase total. Se apenas a amilase pancreática for medida, um aumento não será observado com caxumba ou outro trauma de glândula salivar.
No entanto, devido à pequena quantidade presente, o tempo é crítico ao coletar sangue para esta medição. O sangue deve ser coletado logo após um surto de dor de pancreatite, caso contrário, é excretado rapidamente pelos rins .
A α-amilase salivar tem sido usada como biomarcador de estresse e como marcador substituto da atividade do sistema nervoso simpático (SNS) que não requer coleta de sangue.
Interpretação
Níveis plasmáticos aumentados em humanos são encontrados em:
- Trauma salivar (incluindo intubação anestésica )
- Caxumba - devido a inflamação das glândulas salivares
- Pancreatite - devido a danos nas células que produzem amilase
- Insuficiência renal - devido à redução da excreção
As leituras de amilase total de mais de 10 vezes o limite superior do normal (LSN) são sugestivas de pancreatite. Cinco a 10 vezes o LSN pode indicar íleo ou doença duodenal ou insuficiência renal, e elevações mais baixas são comumente encontradas na doença das glândulas salivares.
Genes
Inerente
A atividade da α-amilase em grãos é medida, por exemplo, pelo número de queda de Hagberg – Perten , um teste para avaliar danos aos brotos ou o método Phadebas . Ocorre no trigo .
Uso industrial
A α-amilase é usada na produção de etanol para quebrar amidos em grãos em açúcares fermentáveis.
A primeira etapa na produção do xarope de milho com alto teor de frutose é o tratamento do amido de milho com α-amilase, produzindo cadeias mais curtas de oligossacarídeos de açúcares .
Uma α-amilase chamada "Termamyl", proveniente do Bacillus licheniformis , também é usada em alguns detergentes, especialmente em detergentes para lavar louças e para remover amido.
Veja amilase para mais usos da família da amilase em geral.
Potencial para uso médico
A α-amilase exibiu eficácia na degradação de biofilmes bacterianos polimicrobianos por meio da hidrólise das ligações glicosídicas α (1-4) dentro dos exopolissacarídeos estruturais da matriz da substância polimérica extracelular (EPS).
Inibição de tampão
A molécula tris é relatada para inibir uma série de α-amilases bacterianas, portanto, eles não devem ser usados em tampão tris.
Determinação
Vários métodos estão disponíveis para a determinação da atividade da α-amilase, e diferentes indústrias tendem a confiar em diferentes métodos. O teste de amido-iodo, um desenvolvimento do teste de iodo , é baseado na mudança de cor, pois a α-amilase degrada o amido e é comumente usado em muitas aplicações. Um teste semelhante, mas produzido industrialmente, é o teste de amilase Phadebas , que é usado como um teste qualitativo e quantitativo em muitas indústrias, como detergentes, várias farinhas, grãos e alimentos de malte e biologia forense.
Arquitetura de domínio
As α-amilases contêm vários domínios de proteína distintos. O domínio catalítico tem uma estrutura que consiste em um barril alfa / beta de oito fitas que contém o sítio ativo, interrompido por um domínio de ligação de cálcio de ~ 70 aminoácidos que se projeta entre a fita beta 3 e a hélice alfa 3, e um terminal carboxila grego domínio beta-barrel chave . Várias alfa-amilases contêm um domínio de folha beta, geralmente no terminal C. Este domínio é organizado como uma folha beta antiparalela de cinco cadeias. Várias alfa-amilases contêm um domínio totalmente beta, geralmente no terminal C.
Veja também
Referências
links externos
- A proteína alfa-amilase
- alfa-amilase na Biblioteca Nacional de Medicina dos Estados Unidos em títulos de assuntos médicos (MeSH)
