Química Organoboron - Organoboron chemistry
Compostos organoborano ou organoboro são compostos químicos de boro e carbono que são derivados orgânicos de BH 3 , por exemplo trialquilboranos. A química do organoboro ou química do organoboro é a química desses compostos.
Os compostos organoboron são reagentes importantes na química orgânica, permitindo muitas transformações químicas, a mais importante delas chamada de hidroboração . As reações de organoboratos e boranos envolvem a transferência de um grupo nucleofílico ligado ao boro para um centro eletrofílico inter ou intramolecularmente. Os boratos α, β-insaturados, bem como os boratos com um grupo de saída na posição α, são altamente suscetíveis à migração 1,2 intramolecular de um grupo do boro para a posição α eletrofílica. A oxidação ou protonólise dos organoboranos resultantes pode gerar uma variedade de produtos orgânicos, incluindo álcoois, compostos carbonílicos, alcenos e halogenetos.
Propriedades do título BC
A ligação CB tem baixa polaridade (a diferença na eletronegatividade de 2,55 para o carbono e 2,04 para o boro) e, portanto, os compostos alquil-boro são em geral estáveis, embora facilmente oxidados.
Em parte devido à sua eletronegatividade mais baixa, o boro freqüentemente forma compostos deficientes em elétrons , como os triorganoboranos. Grupos vinil e grupos aril doam elétrons e tornam o boro menos eletrofílico e a ligação CB ganha algum caráter de ligação dupla . Como o borano original, o diborano , os organoboranos são classificados na química orgânica como eletrófilos fortes porque o boro é incapaz de obter um octeto completo de elétrons. Ao contrário do diborano, entretanto, a maioria dos organoboranos não forma dímeros .
Síntese
De reagentes Grignard
Organoboranos simples como trietilborano ou tris (pentafluorofenil) boro podem ser preparados a partir de trifluoroborano (como o complexo de éter ) e o reagente de Grignard etil ou pentafluorofenil . Os boratos (R 4 B - ) são gerados por meio da adição de R - equivalentes (RMgX, RLi, etc.) a R 3 B.
De alcenos
Os alcenos se inserem nas ligações BH dos boranos em um processo denominado hidroboração . O processo envolve a adição anti- Markovnikov . A hidroboração de alcenos ou alcinos com borano (BH 3 ) ou equivalentes de borano leva à conversão de apenas 33% da olefina inicial em produto após oxidação ou protonólise - a olefina restante é incorporada em subprodutos contendo boro. Um reagente organoboro freqüentemente empregado na síntese é o 9-BBN . Hidroborações ocorrem estereoespecificamente em modo syn , ou seja, na mesma face do alceno. Nesta reação combinada, o estado de transição é representado como um quadrado com os cantos ocupados por carbono, carbono, hidrogênio e boro com sobreposição máxima entre os dois orbitais p de olefina e o orbital de boro vazio.
Por borilação
As reações de boryilação CH catalisadas por metal são reações orgânicas catalisadas por metais de transição que produzem um composto organoboro por meio da funcionalização de ligações CH alifáticas e aromáticas. Um reagente comum nesse tipo de reação é o bis (pinacolato) diboro .
Classes de compostos organoboro
Organoboranos e hidretos
Dentre as classes mais estudadas de compostos organoboro, temos a fórmula BR n H 3 − n . Conforme discutido acima, esses compostos são usados como catalisadores, reagentes e intermediários sintéticos. Os derivados trialquil e triaril apresentam um centro de boro planar trigonal que é tipicamente apenas ligeiramente ácido de Lewis . Exceto por alguns derivados muito volumosos, os hidretos (BR n H 3 − n para n = 1 ou 2) existem como dímeros, uma reminiscência da estrutura do próprio diborano. Derivados trissubstituídos, por exemplo, trietilboro, são monômeros.
Ácidos e ésteres borínicos e borônicos (BR n (OR) 3-n )
Os compostos do tipo BR n (OR) 3-N são chamados ésteres Borínicos (n = 2), ésteres borónicos (n = 1), e boratos (n = 0). Os ácidos borônicos são usados na reação de Suzuki . Borato de trimetila , que não é discutivelmente um composto de organoboro, é um intermediário na produção de boro-hidreto de sódio.
Aglomerados de boro
O boro é conhecido por formar compostos de cluster, por exemplo, dodecaborato [B 12 H 12 ] 2- . Muitos derivados orgânicos são conhecidos por tais aglomerados. Um exemplo é [B 12 (CH 3 ) 12 ] 2- e seu derivado de radical [B 12 (CH 3 ) 12 ] - . Os compostos de cluster relacionados com vértices de carbono são chamados carboranos . O mais conhecido é o ortocarborano, com a fórmula C 2 B 10 H 12 . Embora tenham poucas aplicações comerciais, os carboranos têm atraído muita atenção porque são estruturalmente incomuns. Derivados aniônicos, dicarbolídeos, por exemplo, [C 2 B 9 H 11 ] 2− são ligantes que se comportam como ciclopentadienida .
Compostos aromáticos substituídos por bora
No borabenzeno , um centro CH no benzeno é substituído pelo boro. Estes compostos são invariavelmente isolados como adutos, por exemplo, C 5 H 5 B-piridina. O composto cíclico borol , um análogo estrutural do pirrol , não foi isolado, mas são conhecidos derivados substituídos conhecidos como boroles. O composto cíclico borepin é aromático.
Compostos de boril
Os ânions Boryl têm a fórmula R 2 B - . Compostos boril aniônicos nucleofílicos há muito tempo são esquivos, mas um estudo de 2006 descreveu um composto borilítio , que reage como nucleófilo : Compostos organometálicos com ligações de metal a boro, (isto é, M – BR 2 ), são conhecidos como complexos de boril. Ligantes relacionados são borilenos (M – B (R) –M).
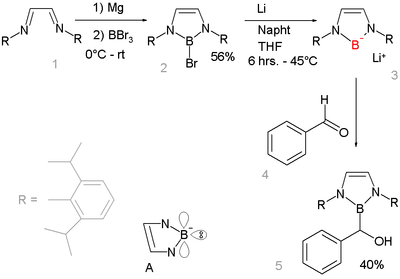
A ausência de compostos de borila de lítio é notável porque em outro período 2 elementos os sais de lítio são comuns, por exemplo , fluoreto de lítio , hidróxido de lítio , amida de lítio e metil - lítio . A lacuna destaca a eletronegatividade muito baixa do boro. A reação da base com um boro-hidreto R 2 BH não resulta em desprotonação para o ânion boril R 2 B - mas na formação do ânion boril R 2 B - H (base) + . Este produto de reação tem um octeto completo . Em vez disso, o composto é preparado por borilo redutiva heterólise de uma ligação boro-brometo de lítio de metal. O novo composto boril-lítio é muito semelhante e isoeletrônico aos carbenos N-heterocíclicos . Ele é projetado para se beneficiar da estabilização aromática (sistema de 6 elétrons contando os pares solitários de nitrogênio e um orbital p de boro vazio , consulte a estrutura A) e da estabilização cinética dos grupos 2,6-diisopropilfenil volumosos. A difração de raios-X confirma a hibridização sp2 em boro e sua reação de adição nucleofílica com benzaldeído dá mais provas da estrutura proposta.
Alquilideneboranos
Alquilidenoboranos do tipo RB = CRR com uma ligação dupla boro-carbono são raramente encontrados. Um exemplo é o borabenzeno . O composto original é HB = CH 2, que pode ser detectado em baixas temperaturas. Um derivado razoavelmente estável é CH 3 B = C (SiMe 3 ) 2, mas é propenso a ciclodimerização .
Adutos NHC de boro
NHCs e boranos formam adutos de borano NHC estáveis . Os adutos de trietilborano podem ser sintetizados diretamente a partir do sal de imidazólio e trietilboro-hidreto de lítio . Os membros desta classe de compostos são investigados para uso como reagente ou catalisador.
Diborenes
Os compostos químicos com ligações duplas de boro a boro são raros. Em 2007, o primeiro diboreno neutro (RHB = BHR) foi apresentado por Gregory Robinson, da Universidade da Geórgia . Cada átomo de boro tem um próton ligado a ele e cada átomo de boro é coordenado a um carbeno NHC . A estrutura parental com os ligantes de carbeno adicionais é o diborano (2) .
Um diboryne relatado é baseado em uma química semelhante.
Reações
Organoboranos (R 3 B) e boratos (R 4 B - , gerados pela adição de R - a R 3 B) possuem ligações boro-carbono que são polarizadas em direção ao carbono. Assim, o carbono ligado ao boro é nucleofílico e, nos boratos, esta propriedade pode ser aproveitada para transferir um dos grupos R para um centro eletrofílico inter ou (mais frequentemente) intramolecularmente. No último caso, o grupo R nucleofílico é capaz de sofrer migração 1,2 em direção a um carbono eletrofílico ligado ao boro. O borano reorganizado resultante pode então ser oxidado ou sujeito a protonólise para produzir produtos orgânicos. Os exemplos cobertos neste artigo são mostrados abaixo.
A hidroboração de alcenos ou alcinos é um método eficiente para a geração de boranos; no entanto, o uso de borano (BH 3 ) ou equivalentes de borano leva à conversão de apenas 33% da olefina inicial em produto após a oxidação ou protonólise - a olefina restante é incorporada em subprodutos contendo boro. O uso de uma quantidade estequiométrica de 9-borabiciclo [3.3.1] nonano (9-BBN) como o reagente de hidroboração fornece uma solução para este problema.
Hidroboração-oxidação
Na síntese orgânica, a reação de hidroboração é levada adiante para gerar outros grupos funcionais no lugar do grupo de boro. A reação de hidroboração-oxidação oferece uma rota para os álcoois pela oxidação do borano com peróxido de hidrogênio ou para o grupo carbonila com o agente oxidante mais forte , óxido de cromo .
Reorganizações
O monóxido de carbono reage com os trialquilboranos. O que se segue é um rearranjo 1,2 por meio do qual um substituinte alquil migra do boro para o carbono do grupo carbonil. Os álcoois primários homologados resultam do tratamento de organoboranos com monóxido de carbono e um hidreto.
Alilboração
A alilboração assimétrica demonstra outra aplicação útil de organoboranos na formação de ligações carbono-carbono. Neste exemplo da síntese de epotilonas de Nicolaou , alilboração assimétrica (usando um alilborano derivado de alfa-pineno quiral ) é usada em conjunto com proteção TBS e ozonólise . No geral, isso fornece uma sequência de homologação de dois carbonos que fornece a sequência de acetogenina necessária .
Como agente redutor
Hidretos de borano, como 9-BBN e L-selectride (tri-sec-butilboro-hidreto de lítio) são agentes redutores . Um exemplo de um catalisador assimétrico para reduções de carbonil é o catalisador CBS . Este catalisador também é baseado em boro, cujo objetivo é a coordenação com o átomo de oxigênio da carbonila.
Boratos
Os trialquilboranos, BR 3 , podem ser oxidados aos boratos correspondentes , B (OR) 3 . Um método para a determinação da quantidade de ligações CB em um composto é por oxidação de R 3 B com óxido de trimetilamina (Me 3 NO) em B (OR) 3 . A trimetilamina (Me 3 N) formada pode então ser titulada .
Ácidos borônicos RB (OH) 2 reagem com bifluoreto de potássio K [HF 2 ] para formar sais trifluoroborato K [RBF 3 ] que são precursores de alquil nucleofílico e difluoretos de aril boro, ArBF 2 . Os sais são mais estáveis do que os próprios ácidos borônicos e usados, por exemplo, na alquilação de certos aldeídos :
Os compostos de organoboro também se prestam a reações de transmetalação , especialmente com os compostos de organopaládio . Este tipo de reacção é exemplificada na reacção de Suzuki , que envolve o acoplamento de arilo - ou vinilo - ácido borónico com um aril - ou vinil - halogeneto catalisado por um paládio (0) complexo ,
-
( 1 )
Esta reação é um método importante para fazer ligações carbono-carbono.
Mecanismo e estereoquímica
Boranos sozinhos geralmente não são nucleofílicos o suficiente para transferir um grupo alquil para um centro eletrofílico. No entanto, após o ataque nucleofílico, o borato resultante é altamente nucleofílico. Se o nucleófilo contém funcionalidade insaturada ou um grupo de saída na posição α, um dos grupos R ligados ao boro é capaz de migrar para o carbono α eletrofílico (ver equação (2) abaixo). A propensão de um grupo orgânico a migrar depende de sua capacidade de estabilizar a carga negativa: alquinil> aril ≈ alquenil> alquil primário> alquil secundário> alquil terciário. A migração ocorre com retenção da configuração no carbono em migração e inversão da configuração no terminal de migração (desde que seja hibridizado sp 3 ). Bis (norbornil) borano e 9-BBN são frequentemente usados como reagentes de hidroboração "fictícios" por este motivo - apenas o grupo R derivado da olefina hidroborada tem probabilidade de migrar após a ativação nucleofílica.
Os enolatos α-Halo são comumente usados como nucleófilos neste contexto. Após o ataque nucleofílico ao boro, o cetoboronato resultante se reorganiza em um enolborano neutro. Após a protonólise, resulta um composto de carbonila funcionalizado. Os enolboranos intermediários também podem ser extintos com eletrófilos.
Alquinilboronatos são intermediários versáteis que podem ser convertidos em cetonas ou olefinas após a migração simultânea e o ataque do alcino em um eletrófilo separado. O eletrófilo e o grupo de migração acabam sendo trans no alquenilborano resultante. A protonólise desse intermediário gera olefinas, enquanto a oxidação leva a cetonas após a tautomerização.
Escopo e limitações das reações
O escopo dos organoboranos e boratos como reagentes para a síntese orgânica é extremamente amplo. As reações de compostos de organoboro podem produzir álcoois, compostos carbonílicos, halogenetos, peróxidos, aminas e outras funcionalidades, dependendo de outros materiais de partida empregados e das condições de reação. Esta seção cobre um pequeno subconjunto desses métodos, enfocando a síntese de álcoois, compostos carbonílicos e halogenetos.
A síntese de álcool a partir de organoboranos e boratos depende da transferência de um grupo nucleofílico para um grupo carbonila ou da oxidação de um organoborano intermediário. Os álcoois primários homologados resultam do tratamento de organoboranos com monóxido de carbono e um hidreto.
Álcoois terciários com dois grupos idênticos ligados ao carbono do álcool podem ser sintetizados por meio de uma reação de dupla migração de alquinilboratos na presença de ácido. O uso de um único equivalente de ácido e oxidação ou protonólise leva a cetonas ou olefinas, respectivamente (consulte a seção Mecanismo e Estereoquímica acima).
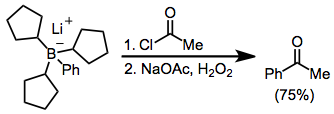
A acilação de boratos é possível na presença de um halogeneto de acila. Aqui, o borato foi gerado a partir de tri (ciclopentil) borano e fenilítio; os três grupos ciclopentil estão servindo como grupos "fictícios" e não migram para uma quantidade significativa.
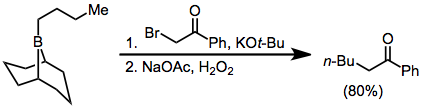
O tratamento de trialquilboranos com α-halo enolatos leva a cetonas funcionalizadas. Como a migração é estereoespecífica (retentiva em relação ao grupo de migração e inversa no carbono α), este método fornece um meio para a síntese de α-alquil ou -aril cetonas enantiopuras.
Os enolatos de éster α-halo também se adicionam aos boranos para, eventualmente, fornecer produtos α-funcionalizados; no entanto, os rendimentos são ligeiramente mais baixos. Diazoésteres e diazocetonas também podem ser usados neste contexto sem a necessidade de base externa. Os enolatos α, α'-dialo reagem com boranos para formar compostos α-halo carbonil que podem ser posteriormente funcionalizados na posição α.
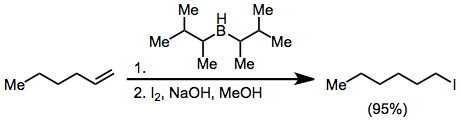
Haletos podem ser sintetizados a partir de organoboranos por ativação com hidróxido ou alcóxido e tratamento com X 2 . Dois dos três grupos alquil ligados ao borano podem ser convertidos em halogeneto na presença de excesso de base, mas o uso de disiamilborano como reagente de hidroboração permite a halogenação seletiva apenas da olefina hidroborada.
O tratamento de um alquenilborano com iodo ou bromo leva à migração de um dos grupos orgânicos ligados ao boro. Os grupos alquinila migram seletivamente, formando eninas após o tratamento com acetato de sódio e peróxido de hidrogênio.
Outros usos
TEB - Trietilborano foi usado para inflamar o combustível JP-7 dos motores de ciclo variável Pratt & Whitney J58 que acionam o Lockheed SR-71 Blackbird .






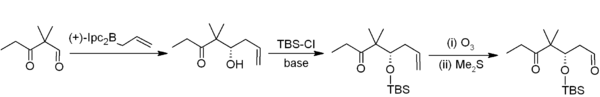

![A reação da Suzuki {\ displaystyle {\ begin {matrix} {} \\ {\ ce {{R1-BY2} + R2-X -> [{\ underset {\ text {catalyst}} {\ text {Pd}}}] [{ \ text {Base}}] R1-R2}} \\ {} \ end {matriz}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c35df36f38fec8abbc8e9d1d9f04e9b2687ae245)