Trióxido de boro - Boron trioxide
![Estrutura cristalina de B2O3 [1]](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/B2O3powder.JPG/220px-B2O3powder.JPG)
|
|
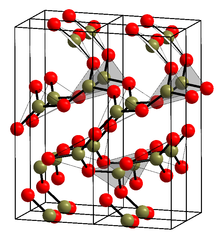
|
|
| Nomes | |
|---|---|
| Outros nomes
óxido de boro, trióxido de diboro, sesquióxido de boro, óxido bórico, boria
anidrido de ácido bórico |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.013.751 |
| Número EC | |
| 11108 | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| B 2 O 3 | |
| Massa molar | 69,6182 g / mol |
| Aparência | branco, sólido vítreo |
| Densidade | 2,460 g / cm 3 , líquido; 2,55 g / cm 3 , trigonal; |
| Ponto de fusão | 450 ° C (842 ° F; 723 K) (trigonal) 510 ° C (tetraédrico) |
| Ponto de ebulição | 1.860 ° C (3.380 ° F; 2.130 K), sublima a 1500 ° C |
| 1,1 g / 100mL (10 ° C) 3,3 g / 100mL (20 ° C) 15,7 g / 100mL (100 ° C) |
|
| Solubilidade | parcialmente solúvel em metanol |
| Acidez (p K a ) | ~ 4 |
| -39,0 · 10 −6 cm 3 / mol | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
66,9 J / mol K |
|
Entropia molar padrão ( S |
80,8 J / mol K |
| -1254 kJ / mol | |
|
Energia livre de Gibbs (Δ f G ˚)
|
-832 kJ / mol |
| Perigos | |
| Riscos principais | Irritante |
| Ficha de dados de segurança | Veja: página de dados |
| Pictogramas GHS |

|
| Palavra-sinal GHS | perigo |
| H360FD | |
| P201 , P202 , P281 , P308 + 313 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | não combustível |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
3163 mg / kg (oral, camundongo) |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 15 mg / m 3 |
|
REL (recomendado)
|
TWA 10 mg / m 3 |
|
IDLH (perigo imediato)
|
2000 mg / m 3 |
| Página de dados suplementares | |
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
| UV , IR , NMR , MS | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O trióxido de boro (ou trióxido de diboro ) é um dos óxidos de boro . É um sólido vítreo branco com a fórmula B 2 O 3 . Quase sempre é encontrado na forma vítrea (amorfa); entretanto, pode ser cristalizado após um recozimento extenso (isto é, sob calor prolongado).
Pensa-se que o óxido de boro vítreo (gB 2 O 3 ) é composto de anéis de boroxol que são anéis de seis membros compostos por boro de 3 coordenadas alternadas e oxigênio de 2 coordenadas. Devido à dificuldade de construir modelos desordenados na densidade correta com muitos anéis de boroxol , essa visão foi inicialmente controversa, mas tais modelos foram construídos recentemente e exibem propriedades em excelente concordância com o experimento. Reconhece-se agora, a partir de estudos experimentais e teóricas, que a fracção de átomos de boro pertencentes aos anéis boroxol no vítreo B 2 O 3 está algures entre 0,73 e 0,83, com 0,75 ( 3 / 4 ) correspondente a uma proporção de 1: 1 entre unidades em anel e sem anel. O número de anéis de boroxol decai no estado líquido com o aumento da temperatura.
A forma cristalina (α-B 2 O 3 ) (ver estrutura na infobox) é composta exclusivamente por triângulos BO 3 . Este trigonal, quartzo do tipo de rede passa por um coesite -like transformação para monoclica β-B 2 O 3 em vários gigapascais (9,5 GPa).
Preparação
O trióxido de boro é produzido tratando o bórax com ácido sulfúrico em um forno de fusão . Em temperaturas acima de 750 ° C, a camada de óxido de boro fundido separa-se do sulfato de sódio . Em seguida, é decantado, resfriado e obtido com pureza de 96–97%.
Outro método é o aquecimento do ácido bórico acima de ~ 300 ° C. O ácido bórico irá se decompor inicialmente em vapor (H 2 O (g) ) e ácido metaborico (HBO 2 ) a cerca de 170 ° C, e aquecimento adicional acima de 300 ° C produzirá mais vapor e trióxido de diboro. As reações são:
- H 3 BO 3 → HBO 2 + H 2 O
- 2 HBO 2 → B 2 O 3 + H 2 O
O ácido bórico vai para o B 2 O 3 microcristalino anidro em um leito fluidizado aquecido. A taxa de aquecimento cuidadosamente controlada evita respingos à medida que a água evolui. O óxido de boro fundido ataca os silicatos. Tubos grafitados internamente via decomposição térmica do acetileno são passivados.
A cristalização de α-B 2 O 3 fundido à pressão ambiente é fortemente desfavorecida cineticamente (compare as densidades de líquido e cristal). As condições limiares para a cristalização do sólido amorfo são 10 kbar e ~ 200 ° C. Sua estrutura cristalina proposta em grupos espaciais enantiomórficos P3 1 (# 144); P3 2 (# 145) (por exemplo, γ-glicina) foi revisado para grupos espaciais enantiomórficos P3 1 21 (# 152); P3 2 21 (# 154) (por exemplo, α-quartzo).
O óxido de boro também se formará quando o diborano (B 2 H 6 ) reagir com o oxigênio do ar ou vestígios de umidade:
- 2B 2 H 6 (g) + 3O 2 (g) → 2B 2 O 3 (s) + 6H 2 (g)
- B 2 H 6 (g) + 3H 2 O (g) → B 2 O 3 (s) + 6H 2 (g)
Formulários
- Agente de fluxo para vidro e esmaltes
- Material de partida para sintetizar outros compostos de boro , como carboneto de boro
- Um aditivo usado em fibras de vidro ( fibras ópticas )
- Componente utilizado na produção de vidro de borosilicato
- A camada de cobertura inerte no processo Czochralski de encapsulamento líquido para a produção de cristal único de arseneto de gálio
- Como um catalisador ácido em síntese orgânica

