Carboneto de boro - Boron carbide

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Carboneto de boro
|
|
| Outros nomes
Tetrabor
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.907 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| B 4 C | |
| Massa molar | 55,255 g / mol |
| Aparência | pó cinza escuro ou preto, inodoro |
| Densidade | 2,52 g / cm 3 , sólido. |
| Ponto de fusão | 2.763 ° C (5.005 ° F; 3.036 K) |
| Ponto de ebulição | 3.500 ° C (6.330 ° F; 3.770 K) |
| insolúvel | |
| Estrutura | |
| Romboédrico | |
| Perigos | |
| Ficha de dados de segurança | MSDS externo |
| Compostos relacionados | |
|
Compostos relacionados
|
Nitreto de boro |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Carboneto de boro (fórmula química aproximadamente B 4 C) é uma cerâmica de boro - carbono extremamente dura e material covalente usado em blindagens de tanques , coletes à prova de balas , pós de sabotagem de motores , bem como em inúmeras aplicações industriais. Com uma dureza Vickers de> 30 GPa, é um dos materiais mais duros conhecidos, atrás do nitreto de boro cúbico e do diamante .
História
O carboneto de boro foi descoberto no século 19 como um subproduto de reações envolvendo boretos metálicos, mas sua fórmula química era desconhecida. Não foi até a década de 1930 que a composição química foi estimada em B 4 C. A controvérsia permaneceu sobre se o material tinha ou não esta estequiometria exata de 4: 1 , já que, na prática, o material é sempre ligeiramente deficiente em carbono em relação a este A fórmula e a cristalografia de raios-X mostram que sua estrutura é altamente complexa, com uma mistura de cadeias de hemácias e icosaedra B 12 .
Essas características argumentam contra uma fórmula empírica B 4 C exata muito simples . Por causa da unidade estrutural B 12 , a fórmula química do carboneto de boro "ideal" é muitas vezes escrita não como B 4 C, mas como B 12 C 3 , e a deficiência de carbono do carboneto de boro descrita em termos de uma combinação de B 12 C 3 e B 12 unidades CBC.
Estrutura de cristal
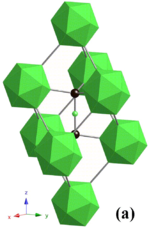
O carboneto de boro tem uma estrutura cristalina complexa típica dos boretos à base de icosaedro . Lá, o icosaedra B 12 forma uma unidade de rede romboédrica (grupo espacial: R 3 m (No. 166), constantes de rede: a = 0,56 nm ec = 1,212 nm) em torno de uma cadeia CBC que reside no centro da célula unitária , e ambos os átomos de carbono ligam os três icosaedras vizinhos. Essa estrutura é em camadas: o icosaedra B 12 e os carbonos em ponte formam um plano de rede que se espalha paralelamente ao plano C e se empilha ao longo do eixo C. A rede tem duas unidades de estrutura básica - o icosaedro B 12 e o octaedro B 6 . Devido ao pequeno tamanho do octaedro B 6 , eles não podem se interconectar. Em vez disso, eles se ligam à icosaedra B 12 na camada vizinha, e isso diminui a força de ligação no plano c .
Por causa da unidade estrutural B 12 , a fórmula química do carboneto de boro "ideal" é muitas vezes escrita não como B 4 C, mas como B 12 C 3 , e a deficiência de carbono do carboneto de boro descrita em termos de uma combinação de B 12 Unidades C 3 e B 12 C 2 . Alguns estudos indicam a possibilidade de incorporação de um ou mais átomos de carbono na icosaedra de boro, dando origem a fórmulas como (B 11 C) CBC = B 4 C na extremidade pesada em carbono da estequiometria, mas fórmulas como B 12 (CBB) = B 14 C na extremidade rica em boro. "Carboneto de boro" não é, portanto, um único composto, mas uma família de compostos de diferentes composições. Um intermediário comum, que se aproxima de uma proporção comumente encontrada de elementos, é B 12 (CBC) = B 6,5 C. Cálculos mecânicos quânticos demonstraram que a desordem configuracional entre os átomos de boro e carbono nas diferentes posições no cristal determina várias das propriedades dos materiais - em particular, a simetria cristalina da composição B 4 C e o caráter elétrico não metálico da composição B 13 C 2 .
Propriedades
O carboneto de boro é conhecido como um material robusto com dureza extremamente alta (cerca de 9,5 até 9,75 na escala de dureza de Mohs ), alta seção transversal para absorção de nêutrons (ou seja, boas propriedades de proteção contra nêutrons), estabilidade à radiação ionizante e a maioria dos produtos químicos. Sua dureza Vickers (38 GPa), módulo elástico (460 GPa) e tenacidade à fratura (3,5 MPa · m 1/2 ) se aproximam dos valores correspondentes para o diamante (1150 GPa e 5,3 MPa · m 1/2 ).
Em 2015, o carboneto de boro é a terceira substância mais dura conhecida, depois do diamante e do nitreto cúbico de boro , ganhando o apelido de "diamante negro".
Propriedades semicondutoras
O carboneto de boro é um semicondutor , com propriedades eletrônicas dominadas pelo transporte do tipo salto. O gap de energia depende da composição e também do grau de ordem. O gap é estimado em 2,09 eV, com múltiplos estados de mid-bandgap que complicam o espectro de fotoluminescência. O material é tipicamente do tipo p.
Preparação
O carboneto de boro foi sintetizado pela primeira vez por Henri Moissan em 1899, pela redução do trióxido de boro com carbono ou magnésio na presença de carbono em um forno elétrico a arco . No caso do carbono, a reação ocorre em temperaturas acima do ponto de fusão de B 4 C e é acompanhada pela liberação de grande quantidade de monóxido de carbono :
- 2 B 2 O 3 + 7 C → B 4 C + 6 CO
Se o magnésio for usado, a reação pode ser realizada em um cadinho de grafite , e os subprodutos de magnésio são removidos por tratamento com ácido.
Formulários

- Cadeados
- Revestimento de blindagem anti-balística pessoal e de veículos
- Bicos de jateamento
- Bicos de corte a jato de água de alta pressão
- Revestimentos resistentes a arranhões e desgaste
- Ferramentas de corte e matrizes
- Abrasivos
- Absorvente de nêutrons em reatores nucleares (veja abaixo)
- Compósitos de matriz de metal
- Combustível de alta energia para ramjets de combustível sólido
- Em lonas de freio de veículos
Aplicações Nucleares
A capacidade do carboneto de boro de absorver nêutrons sem formar radionuclídeos de vida longa o torna atraente como absorvente para a radiação de nêutrons que surge em usinas nucleares e de bombas de nêutrons antipessoal . As aplicações nucleares do carboneto de boro incluem blindagem, hastes de controle e pellets de desligamento. Dentro das hastes de controle, o carboneto de boro é frequentemente pulverizado, para aumentar sua área de superfície.
Veja também
Referências
Bibliografia
- Alan W. Weimer (1997). Síntese e Processamento de Materiais de Carboneto, Nitreto e Boreto . Chapman & Hall (Londres, Nova York). ISBN 0-412-54060-6.

