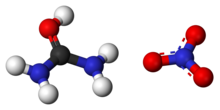
Nitrato de uréia - Urea nitrate

|
|
|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100,004,276 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CH 5 N 3 O 4 | |
| Massa molar | 123,068 g / mol |
| Densidade | 1,67 ± 0,011 g / cm 3 |
| Ponto de fusão | 157–159 ° C (315–318 ° F; 430–432 K) |
| 167,2 ± 0,5 mg / mL | |
| Solubilidade | Etanol 14,2 ± 0,1 mg / mL
Metanol 54,8 ± 0,9 mg / mL Acetona 10,4 ± 0,2 mg / mL |
| Dados explosivos | |
| Sensibilidade ao choque | Baixo |
| Sensibilidade ao atrito | Baixo |
| Velocidade de detonação | 4700 m / s |
| Perigos | |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H201 , H271 , H301 , H304 , H314 , H332 | |
| P220 , P233 , P260 , P250 , P305 + 351 + 338 | |
| NFPA 704 (diamante de fogo) | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O nitrato de ureia é um alto explosivo à base de fertilizantes que tem sido usado em dispositivos explosivos improvisados no Afeganistão , Paquistão , Iraque e em vários atos terroristas em outras partes do mundo, como nos atentados de 1993 ao World Trade Center . Tem um poder destrutivo semelhante aos explosivos de nitrato de amônio mais conhecidos , com uma velocidade de detonação entre 11.155 pés / s (3.400 m / s) e 15.420 pés / s (4.700 m / s).
O nitrato de ureia é produzido em uma etapa pela reação da ureia com o ácido nítrico . Esta é uma reação exotérmica , portanto, devem ser tomadas medidas para controlar a temperatura.
Explosões de nitrato de uréia podem ser iniciadas usando uma tampa de detonação .
Química
A uréia contém um grupo carbonila . O átomo de oxigênio mais eletronegativo puxa os elétrons para longe do carbono, formando uma maior densidade de elétrons ao redor do oxigênio, dando ao oxigênio uma carga parcial negativa e formando uma ligação polar. Quando o ácido nítrico é apresentado, ele se ioniza. Um cátion de hidrogênio contribuído pelo ácido é atraído para o oxigênio e forma uma ligação covalente [eletrófilo H + ]. O íon NO 3 - eletronegativo é então atraído pelo íon de hidrogênio positivo. Isso forma uma ligação iônica e, portanto, o nitrato de ureia composto.
(NH 2 ) 2 CO (aq) + HNO 3 (aq) → (NH 2 ) 2 COHNO 3 (s)
O composto é preferido por muitos entusiastas de explosivos amadores como o principal explosivo para uso em cargas maiores. Nessa função, ele atua como um substituto para os explosivos à base de nitrato de amônio. Isso se deve à facilidade de aquisição dos materiais necessários para sintetizá-lo, e sua maior sensibilidade à iniciação em relação aos explosivos à base de nitrato de amônio.
Referências
Leitura adicional
- Almog J, Burda G, Shloosh Y, Abramovich-Bar S, Wolf E, Tamiri T (novembro de 2007). "Recuperação e detecção de nitrato de ureia em vestígios". J. Forensic Sei . 52 (6): 1284–90. doi : 10.1111 / j.1556-4029.2007.00551.x . PMID 17868267 .
- Mr.X (julho de 2008). "Nitrato de uréia improvisado" . ciente eZine Gamma . Arquivado do original em 20/09/2008 . Página visitada em 2008-11-11 .
links externos
-
 Mídia relacionada ao nitrato de ureia no Wikimedia Commons
Mídia relacionada ao nitrato de ureia no Wikimedia Commons


