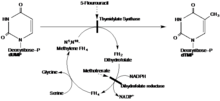Timidilato sintase - Thymidylate synthase
| timidilato sintase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| EC nº | 2.1.1.45 | ||||||||
| CAS no. | 9031-61-2 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
| Sintase de timidilato | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Thymidylat_synt | ||||||||
| Pfam | PF00303 | ||||||||
| InterPro | IPR000398 | ||||||||
| PRÓSITO | PDOC00086 | ||||||||
| SCOP2 | 1tys / SCOPe / SUPFAM | ||||||||
| |||||||||
A timidilato sintase (TS) ( EC 2.1.1.45 ) é uma enzima que catalisa a conversão de monofosfato de desoxiuridina (dUMP) em monofosfato de desoxitimidina (dTMP). A timidina é um dos nucleotídeos do DNA. Com a inibição de TS, surge um desequilíbrio de desoxinucleotídeos e níveis aumentados de dUMP . Ambos causam danos ao DNA.
Função
A seguinte reação é catalisada pela timidilato sintase:
- 5,10-metilenotetra-hidrofolato + dUMP di-hidrofolato + dTMP
Por meio de metilação redutiva , monofosfato de desoxiuridina (dUMP) e N5, N10-tetrahidrofolato de metileno são usados juntos para formar dTMP, produzindo dihidrofolato como produto secundário.
Isso fornece a única via de novo para a produção de dTMP e é a única enzima no metabolismo do folato em que o 5,10-metilenotetra-hidrofolato é oxidado durante a transferência de um carbono. A enzima é essencial para regular o suprimento equilibrado dos 4 precursores do DNA na replicação normal do DNA: defeitos na atividade da enzima que afetam o processo de regulação causam várias anormalidades biológicas e genéticas, como a morte sem tina. A enzima é um alvo importante para certos medicamentos quimioterápicos. A timidilato sintase é uma enzima de cerca de 30 a 35 k Da na maioria das espécies, exceto em protozoários e plantas, onde existe como uma enzima bifuncional que inclui um domínio dihidrofolato redutase. Um resíduo de cisteína está envolvido no mecanismo catalítico (liga-se covalentemente ao intermediário 5,6-diidro-dUMP). A sequência em torno do sítio ativo desta enzima é conservada de fagos a vertebrados.
A timidilato sintase é induzida por um fator de transcrição LSF / TFCP2 e LSF é um oncogene no carcinoma hepatocelular . A LSF e a timidilato sintase desempenham um papel significativo na proliferação e progressão do câncer de fígado e na resistência aos medicamentos.
Significado clínico
A timidilato sintase (TS) desempenha um papel crucial nas fases iniciais da biossíntese de DNA . Danos ou deleção de DNA ocorrem diariamente como resultado de fatores endógenos e ambientais. Esses fatores ambientais incluem danos ultravioleta e fumaça de cigarro que contém uma variedade de carcinógenos. Portanto, a síntese e a inserção de DNA saudável são vitais para as funções normais do corpo e para evitar a atividade cancerosa. Além disso, a inibição na síntese de nucleotídeos importantes necessários para o crescimento celular é importante. Por esse motivo, a TS tornou-se um importante alvo para o tratamento do câncer por meio da quimioterapia . A sensibilidade da TS para sucumbir aos inibidores da TS é uma parte fundamental para seu sucesso como tratamento para câncer colorretal, pancreático, ovariano, gástrico e de mama.
Usando TS como alvo de drogas
O uso de inibidores de TS tornou-se o foco principal do uso de TS como alvo de drogas. O inibidor mais amplamente utilizado é o 5-fluorouracil (5-FU), que atua como um antimetabólito que inibe irreversivelmente o TS por ligação competitiva. No entanto, devido a um baixo nível de 5-FU encontrado em muitos pacientes, foi descoberto que, em combinação com a leucovorina (LV), o 5-FU tem maior sucesso em diminuir os mecanismos de progressão tumoral e aumentar a atividade do sistema imunológico.
Experimentalmente, foi demonstrado que baixos níveis de expressão de TS levam a uma melhor resposta ao 5-FU e maiores taxas de sucesso e sobrevida de pacientes com câncer de cólon e fígado. No entanto, experimentos adicionais apenas afirmaram que os níveis de TS podem estar associados ao estágio da doença, proliferação celular e diferenciação tumoral para aqueles com adenocarcinoma de pulmão, mas níveis baixos não são necessariamente indicadores de alto sucesso. Os níveis de expressão do mRNA de TS podem ser úteis na previsão do potencial maligno de certas células cancerosas, melhorando assim os alvos do tratamento do câncer e gerando taxas de sobrevida mais altas entre os pacientes com câncer [Hashimoto].
A relação do TS com o ciclo celular também contribui para seu uso no tratamento do câncer. Várias quinases dependentes do ciclo celular e fatores de transcrição influenciam os níveis de TS no ciclo celular que aumentam sua atividade durante a fase S, mas diminuem sua atividade enquanto as células não estão mais proliferando. De maneira autorregulatória, a TS não controla apenas sua própria tradução, mas também a de outras proteínas como a p53 que, por meio de mutação, é a raiz de grande parte do crescimento tumoral. Por meio de sua tradução, o TS tem uma expressão variável em células cancerosas e tumores, o que leva à morte celular precoce.
Mapa de caminho interativo
Clique nos genes, proteínas e metabólitos abaixo para acessar os respectivos artigos.
Descrição do mecanismo
No mecanismo proposto, o TS forma uma ligação covalente ao substrato dUMP por meio de uma adição 1,4 envolvendo um nucleófilo de cisteína. O substrato tetrahidrofolato doa um grupo metil ao carbono alfa enquanto reduz o novo metil em dUMP para formar dTMP.
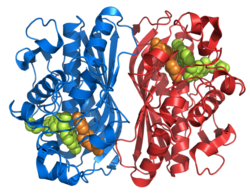
Está comprovado que a imina formada pela reação com THF e dUMP é um intermediário na reação com dUMP por meio de mutações na estrutura do TS que inibem a conclusão do mecanismo. V316Am TS, um mutante com deleção de valinas C terminais de ambas as subunidades, permite a catálise de desalogenação de BrdUMP precedendo o mecanismo descrito acima e a ligação covalente a THF e dUMP. O mutante TS é incapaz de realizar a mudança conformacional C-terminal necessária para quebrar ligações covalentes para formar dTMP, mostrando assim que o mecanismo proposto é verdadeiro. A estrutura foi deduzida por meio de cristalografia de raios-X de V316Am TS para ilustrar a estrutura completa do homodímero TS (Figura 1). Além disso, mostrou possíveis interações do 175Arg e 174Arg entre os dímeros. Acredita-se que essas argininas estabilizem as estruturas UMP dentro dos sítios ativos, criando ligações de hidrogênio ao grupo fosfato (Figura 2). [Stroud and Finer-Moore] 5-FU é um inibidor de TS. Ao entrar na célula, o 5-fluorouracil (5-FU) é convertido em uma variedade de metabólitos ativos, intracelularmente. Um desses metabólitos é o FdUMP, que difere do dUMP por um flúor no lugar de um hidrogênio no carbono alfa. FdUMP é capaz de inibir TS ligando-se ao sítio de ligação de nucleotídeo do dUMP. Esta ligação competitiva inibe a função normal da síntese de dTMP a partir de dUMP [Longley]. Assim, o dUMP é incapaz de ter uma reação de eliminação e completar a doação de metil do THF.
Figura 1. Esta figura mostra o homodímero que é TS. Como você pode ver, os backbones laranja e azul-petróleo nunca se conectam ou se entrelaçam, mas há interações de cadeias laterais entre os dímeros. Na proteína laranja, você pode detectar visivelmente duas longas cadeias laterais que entram na proteína azul-petróleo (localizadas dentro do círculo amarelo). As outras partes bege são cadeias laterais que interagem dentro do site ativo. Logo abaixo do círculo amarelo, você pode ver o mesmo padrão de cadeias laterais e configuração.
Figura 2. Esta figura mostra as possíveis interações de ligação H entre as argininas e o UMP no sítio ativo da timidilato sintase. Isso pode ser visto pelas linhas tênues entre as pontas azuis e vermelhas. Essas argininas são usadas para manter a posição da molécula de UMP para que a interação possa ocorrer corretamente. As duas argininas no canto superior direito localizadas próximas uma da outra na coluna vertebral são, na verdade, da outra proteína desta enzima dímero. Essa interação é uma das muitas forças intermoleculares que mantêm essas duas estruturas terciárias juntas. O suporte amarelo na região superior média mostra uma ligação de enxofre que se forma entre uma cadeia lateral de cisteína e UMP. Este mantém covalentemente o UMP dentro do sítio ativo até que ele reaja para produzir TMP.
Veja também
- Análogos de pirimidina
- Inibidor da timidilato sintase
- Timidina quinase
- Timidina quinase em química clínica
- Timidilato quinase
Referências
Leitura adicional
- Carreras CW, Santi DV (1995). "The Catalytic Mechanism and Structure of Thymidylate Synthase". Revisão Anual de Bioquímica . 64 (1): 721–762. doi : 10.1146 / annurev.bi.64.070195.003445 . PMID 7574499 .
- Banerjee D, Mayer-Kuckuk P, Capiaux G, et al. (2002). "Novos aspectos de resistência a drogas direcionadas a dihidrofolato redutase e timidilato sintase" . Biochim. Biophys. Acta . 1587 (2–3): 164–73. doi : 10.1016 / S0925-4439 (02) 00079-0 . PMID 12084458 .
- Liu J, Schmitz JC, Lin X, et al. (2002). "Timidilato sintase como um regulador translacional da expressão do gene celular" . Biochim. Biophys. Acta . 1587 (2–3): 174–82. doi : 10.1016 / s0925-4439 (02) 00080-7 . PMID 12084459 .
- Chu J, Dolnick BJ (2002). "O RNA antisense natural (rTSalpha) induz a clivagem específica do local do mRNA da timidilato sintase" . Biochim. Biophys. Acta . 1587 (2–3): 183–93. doi : 10.1016 / s0925-4439 (02) 00081-9 . PMID 12084460 .
- Peters GJ, Backus HH, Freemantle S, et al. (2002). "Indução da sintase do timidilato como um mecanismo de resistência do 5-fluorouracil" . Biochim. Biophys. Acta . 1587 (2–3): 194–205. doi : 10.1016 / S0925-4439 (02) 00082-0 . PMID 12084461 .
- Costi MP, Tondi D, Rinaldi M, et al. (2002). "Estudos com base na estrutura da inibição específica da espécie da timidilato sintase" . Biochim. Biophys. Acta . 1587 (2–3): 206–14. doi : 10.1016 / s0925-4439 (02) 00083-2 . PMID 12084462 .
- Lin D, Li H, Tan W, et al. (2007). Polimorfismos genéticos em enzimas metabolizadoras de folato e risco de câncer gastroesofágico: uma potencial interação nutriente-gene no desenvolvimento do câncer . Fórum de Nutrição. 60 . pp. 140-5. doi : 10.1159 / 000107090 . ISBN 978-3-8055-8216-2. PMID 17684410 .
links externos
- Timidilato + sintetase nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)
- PDBe-KB fornece uma visão geral de todas as informações de estrutura disponíveis no PDB para sintase de timidilato humano