Trietilalumínio - Triethylaluminium

|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Trietilalumano
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| Abreviações | TEA, TEAl, TEAL |
| ChemSpider | |
| ECHA InfoCard |
100,002,382 |
| Número EC | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
| Propriedades | |
| C 12 H 30 Al 2 | |
| Massa molar | 228,335 g · mol −1 |
| Aparência | Líquido incolor |
| Densidade | 0,8324 g / mL a 25 ° C |
| Ponto de fusão | −46 ° C (−51 ° F; 227 K) |
| Ponto de ebulição | 128 a 130 ° C (262 a 266 ° F; 401 a 403 K) a 50 mmHg |
| Perigos | |
| Riscos principais | pirofórico |
| Frases R (desatualizado) | R14 R17 R34 |
| Frases S (desatualizado) | S16 S43 S45 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | −18 ° C (0 ° F; 255 K) |
| Compostos relacionados | |
|
Compostos relacionados
|
Trimetilalumínio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
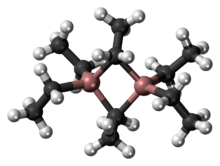
O trietilalumínio é um dos exemplos mais simples de um composto organoalumínio . Apesar do nome, possui a fórmula Al 2 ( C 2 H 5 ) 6 (abreviado como Al 2 Et 6 ou TEA), pois existe na forma de dímero . Este líquido incolor é pirofórico . É um composto industrialmente importante, intimamente relacionado ao trimetilalumínio .
Estrutura e ligação
A estrutura e ligação em Al 2 R 6 e diborano são análogas (R = alquil). Com referência a Al 2 Me 6 , as distâncias Al-C (terminal) e Al-C (ponte) são 1,97 e 2,14 Å, respectivamente. O centro de Al é tetraédrico. Os átomos de carbono dos grupos etil em ponte são cada um rodeado por cinco vizinhos: carbono, dois átomos de hidrogênio e dois átomos de alumínio. Os grupos etil trocam facilmente intramolecularmente. Em temperaturas mais altas, o dímero se quebra em AlEt 3 monomérico .
Síntese e reações
O trietilalumínio pode ser formado por várias vias. A descoberta de uma rota eficiente foi uma conquista tecnológica significativa. O processo de várias etapas usa alumínio metálico, gás hidrogênio e etileno , resumidos da seguinte forma:
- 2 Al + 3 H 2 + 6 C 2 H 4 → Al 2 Et 6
Por causa dessa síntese eficiente, o trietilalumínio é um dos compostos organoalumínicos mais disponíveis.
O trietilalumínio também pode ser gerado a partir do sesquicloreto de etilalumínio (Al 2 Cl 3 Et 3 ), que surge tratando o pó de alumínio com cloroetano . A redução do sesquicloreto de etilalumínio com um metal alcalino , como o sódio, dá trietilalumínio:
- 3 Al 2 Cl 3 Et 3 + 9 Na → 2 Al 2 Et 6 + 2 Al + 9 NaCl
Reatividade
As ligações Al-C do trietilalumínio são polarizadas a tal ponto que o carbono é facilmente protonado , liberando etano:
- Al 2 Et 6 + 6 HX → 2 AlX 3 + 6 EtH
Para esta reação, mesmo ácidos fracos podem ser empregados, como acetilenos terminais e álcoois.
A ligação entre o par de centros de alumínio é relativamente fraca e pode ser clivada por bases de Lewis (L) para dar adutos com a fórmula AlEt 3 L:
- Al 2 Et 6 + 2 L → 2 LAlEt 3
Formulários
Precursores de álcoois graxos
O trietilalumínio é utilizado industrialmente como intermediário na produção de álcoois graxos , que são convertidos em detergentes . A primeira etapa envolve a oligomerização do etileno pela reação de Aufbau , que dá uma mistura de compostos de trialquilalumínio (simplificados aqui como grupos octilos ):
- Al 2 (C 2 H 5 ) 6 + 18 C 2 H 4 → Al 2 (C 8 H 17 ) 6
Posteriormente, esses compostos de trialquila são oxidados em alcóxidos de alumínio , que são então hidrolisados:
- Al 2 (C 8 H 17 ) 6 + 3 O 2 → Al 2 (OC 8 H 17 ) 6
- Al 2 (OC 8 H 17 ) 6 + 6 H 2 O → 6 C 8 H 17 OH + 2 "Al (OH) 3 "
Co-catalisadores na polimerização de olefinas
Uma grande quantidade de TEAL e alquilos de alumínio relacionados são usados na catálise de Ziegler-Natta . Eles servem para ativar o catalisador de metal de transição tanto como agente redutor quanto como agente alquilante . O TEAL também funciona para limpar a água e o oxigênio.
Reagente em química orgânica e organometálica
O trietilalumínio tem nicho de uso como um precursor de outros compostos organoalumínio, como o cianeto de dietilalumínio :
Agente pirofórico
O trietilalumínio se inflama em contato com o ar e se inflama e / ou se decompõe em contato com água e com qualquer outro oxidante - é uma das poucas substâncias suficientemente pirofóricas para acender em contato com oxigênio líquido criogênico . A entalpia de combustão , Δ c H °, é –5105,70 ± 2,90 k J / mol (–22,36 kJ / g ). Sua fácil ignição o torna particularmente desejável como um ignitor de motor de foguete . A SpaceX Falcon 9 foguete utiliza um triethylaluminium- trietilborano mistura como um dispositivo de ignição de primeira fase.
O trietilalumínio espessado com poliisobutileno é utilizado como arma incendiária , como alternativa pirofórica ao napalm ; por exemplo, no clipe M74 segurando quatro foguetes para os lançadores M202A1 . Nesta aplicação é conhecido como TPA, para agente pirotécnico espessado ou agente pirofórico espessado . A quantidade normal de espessante é de 6%. A quantidade de espessante pode ser diminuída para 1% se outros diluentes forem adicionados. Por exemplo, n-hexano pode ser usado com segurança aumentada tornando o composto não pirofórico até que o diluente evapore, ponto em que uma bola de fogo combinada resulta de ambos os vapores de trietilalumínio e hexano. O M202 foi retirado de serviço em meados da década de 1980 devido a questões de segurança, transporte e armazenamento. Alguns viram uso limitado na Guerra do Afeganistão contra cavernas e compostos fortificados.
Veja também
- Trietilborano , usado como ignitor nos motores turbojato / ramjet Pratt & Whitney J58 .
- Trimetilalumínio


![{\ displaystyle {\ ce {{1 / 2Al2Et6} + HCN ->}} \ {\ tfrac {1} {n}} {\ ce {[Et2AlCN]}} _ {n} + {\ ce {C2H6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b73bebe835386dae4e699b7a9b65a76a0f6853f3)