Toxina da difteria - Diphtheria toxin
| precursor da toxina da difteria tox | |||||||
|---|---|---|---|---|---|---|---|
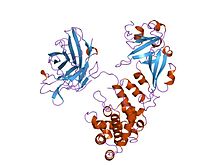 Representação dos desenhos animados da proteína da toxina da difteria
| |||||||
| Identificadores | |||||||
| Organismo | |||||||
| Símbolo | tox | ||||||
| Entrez | 2650491 | ||||||
| RefSeq (Prot) | NP_938615 | ||||||
| UniProt | P00587 | ||||||
| Outros dados | |||||||
| Número CE | 2.4.2.36 | ||||||
| Cromossoma | genoma: 0,19 - 0,19 Mb | ||||||
| |||||||
| Toxina da difteria, domínio C | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_C | ||||||||
| Pfam | PF02763 | ||||||||
| Clã Pfam | CL0084 | ||||||||
| InterPro | IPR022406 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
| Toxina da difteria, domínio T | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_T | ||||||||
| Pfam | PF02764 | ||||||||
| InterPro | IPR022405 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
| Toxina da difteria, domínio R | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_R | ||||||||
| Pfam | PF01324 | ||||||||
| InterPro | IPR022404 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
A toxina da difteria é uma exotoxina secretada pelo Corynebacterium , a bactéria patogênica que causa a difteria . O gene da toxina é codificado por um profago denominado corinefago β . A toxina causa a doença em humanos ao entrar no citoplasma da célula e inibir a síntese de proteínas .
Estrutura
A toxina da difteria é uma única cadeia polipeptídica de 535 aminoácidos que consiste em duas subunidades ligadas por pontes dissulfeto , conhecidas como toxina AB . A ligação à superfície celular da subunidade B (a menos estável das duas subunidades) permite que a subunidade A (a parte mais estável da proteína) penetre na célula hospedeira .
A estrutura cristalina do homodímero da toxina da difteria foi determinada para resolução de 2,5 Ångstrom . A estrutura revela uma molécula em forma de Y que consiste em três domínios . O fragmento A contém o domínio C catalítico , e o fragmento B consiste nos domínios T e R:
- O domínio catalítico do terminal amino , conhecido como domínio C, tem uma dobra beta + alfa incomum . O domínio C bloqueia a síntese de proteínas por transferência de ADP-ribose de NAD para um resíduo de diftamida do fator de alongamento eucariótico 2 (eEF-2).
- Um domínio de translocação central, conhecido como domínio T ou domínio TM, tem uma dobra semelhante a globina multi-helicoidal com duas hélices adicionais no terminal amino, mas nenhuma contraparte para a primeira hélice de globina . Acredita-se que esse domínio se desdobra na membrana . Uma mudança conformacional induzida por pH no domínio T desencadeia a inserção na membrana endossômica e facilita a transferência do domínio C para o citoplasma .
- Um domínio de ligação ao receptor do terminal carboxi , conhecido como domínio R, tem uma dobra em sanduíche beta que consiste em nove fitas em duas folhas com topologia de chave grega; é uma subclasse de dobra semelhante à imunoglobulina . Se liga o domínio R para um receptor da superfície celular , que permitem a toxina de introduzir a célula por receptor mediada por endocitose .
Mecanismo
- Em processamento
- A região líder é clivada durante a secreção.
- O corte proteolítico separa as subunidades A e B, que permanecem unidas por ligações dissulfeto até atingirem o citosol.
- A toxina se liga ao precursor do fator de crescimento epidérmico de ligação à heparina (HB-EGF).
- O complexo sofre endocitose pela célula hospedeira.
- A acidificação dentro do endossomo induz a translocação da subunidade A para o citosol.
- As ligações dissulfeto são quebradas.
- A subunidade B permanece no endossomo como um poro.
- Os ribosilatos de ADP da subunidade A hospedam eEF-2. eEF-2 é necessário para a síntese de proteínas; quando é inativado, o hospedeiro não consegue produzir proteína e, portanto, morre.
A toxina diftérica tem o mesmo mecanismo de ação da enzima NAD (+) - diftamida ADP-ribosiltransferase ( EC 2.4.2.36 ). Catalisa a transferência de NAD + para um resíduo de diftamida no eEF-2, inativando essa proteína. Fá-lo por ADP-ribosylating o incomum aminoácido diftamida . Dessa forma, atua como um inibidor da tradução do RNA . A reação catalisada é a seguinte:
- NAD + + péptido diftamida nicotinamida + péptido N- (ADP-D-ribosil) diftamida.
A exotoxina A de Pseudomonas aeruginosa usa um mecanismo de ação semelhante.
Dose letal e efeitos
A toxina da difteria é extraordinariamente potente. A dose letal para humanos é de cerca de 0,1 μg de toxina por kg de peso corporal. A morte ocorre por necrose do coração e do fígado . A toxina da difteria também foi associada ao desenvolvimento de miocardite. A miocardite secundária à toxina diftérica é considerada um dos maiores riscos para crianças não imunizadas.
História
A toxina da difteria foi descoberta em 1888 por Émile Roux e Alexandre Yersin . Em 1890, Emil Adolf von Behring desenvolveu uma antitoxina baseada no sangue de cavalos imunizados com bactérias atenuadas. Em 1951, Freeman descobriu que o gene da toxina não era codificado no cromossomo bacteriano, mas por um fago lisogênico ( corinefago β ) infectando todas as cepas toxigênicas.
Uso clínico
A droga denileucina diftitox usa a toxina da difteria como agente antineoplásico .
Resimmune é uma imunotoxina que está em ensaios clínicos em pacientes com linfoma cutâneo de células T. Ele usa a toxina da difteria (truncada pelo domínio de ligação da célula) acoplada a um anticorpo para CD3ε (UCHT1).
Pesquisar
Semelhante a outras toxinas AB, a toxina da difteria é adepta do transporte de proteínas exógenas através das membranas das células de mamíferos, que geralmente são impermeáveis a proteínas grandes. Esta capacidade única pode ser reaproveitada para entregar proteínas terapêuticas, em vez do domínio catalítico da toxina.
Essa toxina também tem sido usada em pesquisas neurocientíficas e de câncer para eliminar populações específicas de células que expressam o receptor da toxina da difteria ( fator de crescimento semelhante ao EGF de ligação à heparina ). A administração da toxina no organismo que não expressa naturalmente esse receptor (por exemplo, camundongos) resultará na ablação seletiva da população de células que a expressa.
Anotações
Referências
links externos
- Difteria + Toxina nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)
- Como funciona a toxina da difteria - animação


