Coranuleno - Corannulene

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dibenzo [ ghi , mno ] fluoranteno
|
|
| Outros nomes
[5] circulene
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 20 H 10 | |
| Massa molar | 250,29 g / mol |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
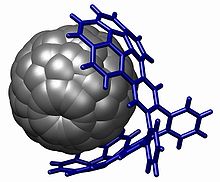
O coranuleno é um hidrocarboneto aromático policíclico com fórmula química C 20 H 10 . A molécula consiste em um anel de ciclopentano fundido com 5 anéis de benzeno , então outro nome para ela é [5] circulene . É de interesse científico porque é um poliareno geodésico e pode ser considerado um fragmento de buckminsterfullereno . Devido a essa conexão e também ao seu formato de tigela, o coranuleno também é conhecido como buckybowl . O coranuleno exibe uma inversão tigela a tigela com uma barreira de inversão de 10,2 kcal / mol (42,7 kJ / mol) a -64 ° C.
Síntese
Existem várias rotas sintéticas para o coranuleno. As técnicas de pirólise instantânea a vácuo geralmente têm rendimentos químicos mais baixos do que as sínteses de solução química, mas oferecem rotas para mais derivados. O Corannulane foi isolado pela primeira vez em 1966 por síntese orgânica em várias etapas. Em 1971, a síntese e as propriedades do coranulano foram relatadas. Um método de pirólise flash a vácuo seguido em 1991. Uma síntese baseada na química da solução consiste em um deslocamento nucleofílico - reação de eliminação de um octabrometo com hidróxido de sódio :
Os substituintes do bromo são removidos com um excesso de n- butil-lítio .
Uma síntese em escala de quilograma de coranuleno foi alcançada.
Muitos esforços são direcionados à funcionalização do anel coranuleno com novos grupos funcionais, como grupos etinil, grupos éter, grupos tioéter, grupos funcionais platina, grupos aril, fenalenil fundido e extensões indeno. e grupos ferroceno .
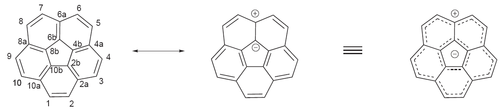
Aromaticidade
A aromaticidade observada para este composto é explicada com o denominado modelo de anuleno dentro de um anuleno . De acordo com este modelo, o coranuleno é constituído por um ânion ciclopentadienil aromático de 6 elétrons rodeado por um cátion anulenil aromático de 14 elétrons . Este modelo foi sugerido por Barth e Lawton na primeira síntese do coranuleno em 1966. Eles também sugeriram o nome trivial de 'coranuleno', que é derivado do modelo anuleno dentro de um anuleno: núcleo + anuleno.
No entanto, cálculos teóricos posteriores contestaram a validade dessa aproximação.
Reações
Redução
O coranuleno pode ser reduzido a até um tetraanião em uma série de reduções de um elétron . Isso tem sido feito com metais alcalinos , eletroquimicamente e com bases. O dianião é corannulene antiaromáticas e tetraanion é novamente aromático . Com o lítio como agente redutor, dois tetraanions formam um dímero supramolecular com duas tigelas empilhadas uma na outra com 4 íons de lítio entre e 2 pares acima e abaixo da pilha. Este motivo de automontagem foi aplicado na organização dos fulerenos. Fulerenos pentassubstituídos (com grupos metil ou fenil) carregados com cinco elétrons formam dímeros supramoleculares com uma tigela de tetraânion coranuleno complementar, 'costurada' por cátions de lítio intersticiais. Em um sistema relacionado, 5 íons de lítio são ensanduichados entre duas tigelas de coranuleno
Em um ciclopenta [bc] coranuleno, um agregado côncavo-côncavo é observado por espectroscopia de NMR com ligações 2 C-Li-C conectando os tetraânions.
Os metais tendem a se ligar à face convexa do anuleno. A ligação côncava foi relatada para um sistema de césio / éter de coroa
Oxidação
A fotoionização UV de 193 nm remove efetivamente um elétron π do degenerado duplo E 1 -HOMO localizado na rede aromática de elétrons produzindo um cátion radical coranuleno. Devido à degenerescência no orbital HOMO, o cátion radical coranuleno é instável em seu arranjo molecular C 5v original e, portanto, sujeito à distorção vibrônica de Jahn-Teller (JT).
Usando a ionização por eletropulverização, um cátion coranuleno protonado foi produzido no qual o local de protonação foi observado como estando em um átomo de carbono sp 2 periférico .
Reação com eletrófilos
O coranuleno pode reagir com eletrófilos para formar um carbocátion de coranuleno . A reação com clorometano e cloreto de alumínio resulta na formação de um sal AlCl 4 - com um grupo metil situado no centro com o centro catiônico na borda. A análise de difração de raios-X mostra que a nova ligação carbono-carbono é alongada (157 pm)
Bicoranulenil
Bicoranulenil é o produto do acoplamento desidrogenativo do coranuleno. Com a fórmula C 20 H 9 - C 20 H 9 , consiste em duas unidades de coranuleno conectadas por uma única ligação CC. A estereoquímica da molécula consiste em dois elementos quirais: a assimetria de um coranulenil substituído individualmente e a torção helicoidal em torno da ligação central. No estado neutro, o bicoranulenil existe como 12 conformadores, que se intercalam por meio de múltiplas inversões de tigela e rotações de ligação. Quando o bicoranulenil é reduzido a um dianião com o metal de potássio, a ligação central assume um caráter de ligação dupla significativo. Essa mudança é atribuída à estrutura orbital, que possui um orbital LUMO localizado na ligação central. Quando o bicoranulenil é reduzido a uma octaânion com o metal de lítio, ele se auto-monta em oligômeros supramoleculares. Este motivo ilustra "empilhamento de poliareno carregado".
Pesquisar
O grupo coranuleno é usado na química hospedeiro-hóspede com interações baseadas no empilhamento pi , notavelmente com fulerenos (o buckycatcher), mas também com nitrobenzeno
Os coranulenos alquil-substituídos formam uma mesofase cristalina líquida hexagonal colunar termotrópica . O coranuleno também foi usado como o grupo principal em um dendrímero . Como outros PAHs, o coranuleno liga os metais. Coranulenos com grupos etinil são investigados quanto ao seu uso potencial como emissores azuis. A estrutura foi analisada por espectroscopia de infravermelho, espectroscopia Raman e espectroscopia de fotoelétrons de raios-X.


![Ciclopenta [bc] coranuleno](https://upload.wikimedia.org/wikipedia/commons/thumb/2/21/Cyclopenta-bc-corannulene.png/100px-Cyclopenta-bc-corannulene.png)