Cromato e dicromato - Chromate and dichromate
|
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC sistemático
Cromato e dicromato |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| DrugBank | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
|
CrO2− 4e Cr 2O2− 7 |
|||
| Massa molar | 115,994 g mol −1 e 215,988 g mol −1 | ||
| Ácido conjugado | Ácido crômico | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
| Referências da Infobox | |||
Os sais de cromato contêm o ânion cromato, CrO2−
4. Os sais de dicromato contêm o ânion dicromato, Cr
2O2−
7. Eles são oxiânions de cromo no estado de oxidação 6+ e são agentes oxidantes moderadamente fortes . Em uma solução aquosa , os íons cromato e dicromato podem ser interconvertíveis.
Propriedades quimicas
Os cromatos reagem com o peróxido de hidrogênio , gerando produtos nos quais o peróxido , O2−
2, substitui um ou mais átomos de oxigênio. Em solução ácida, o peróxido de cromo (VI) óxido de cromo (VI) complexo azul instável , CrO (O 2 ) 2 , é formado; é uma molécula covalente sem carga , que pode ser extraída para o éter . A adição de piridina resulta na formação do complexo mais estável CrO (O 2 ) 2 py.
Propriedades ácido-base
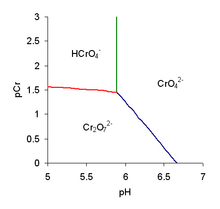
Em solução aquosa, os ânions cromato e dicromato existem em equilíbrio químico .
- 2 CrO2−
4+ 2 H + ⇌ Cr
2O2−
7+ H 2 S
O diagrama de predominância mostra que a posição de equilíbrio depende tanto do pH quanto da concentração analítica de cromo. O íon cromato é a espécie predominante em soluções alcalinas, mas o dicromato pode se tornar o íon predominante em soluções ácidas.
Outras reações de condensação podem ocorrer em solução fortemente ácida com a formação de tricromatos , Cr
3O2 a
10, e tetracromatos , Cr
4O2−
13. Todos os polioxiânions de cromo (VI) têm estruturas feitas de unidades tetraédricas de CrO 4 compartilhando cantos.
O íon cromato de hidrogênio, HCrO 4 - , é um ácido fraco :
-
HCrO-
4⇌ CrO2−
4+ H + ; p K a ≈ 5,9
Também está em equilíbrio com o íon dicromato:
- 2 HCrO-
4⇌ Cr
2O2−
7+ H 2 S
Este equilíbrio não envolve uma mudança na concentração de íons de hidrogênio, o que poderia prever que o equilíbrio é independente do pH. A linha vermelha no diagrama de predominância não é totalmente horizontal devido ao equilíbrio simultâneo com o íon cromato. O íon cromato de hidrogênio pode ser protonado, com a formação de ácido crômico molecular , H 2 CrO 4 , mas o p K a para o equilíbrio
- H 2 CrO 4 ⇌ HCrO-
4+ H +
não está bem caracterizado. Os valores relatados variam entre cerca de -0,8 e 1,6.
O íon dicromato é uma base um pouco mais fraca do que o íon cromato:
-
HCr
2O-
7⇌ Cr
2O2−
7+ H + , p K = 1,18
O valor de p K para esta reação mostra que ela pode ser ignorada em pH> 4.
Propriedades de oxidação-redução
Os íons cromato e dicromato são agentes oxidantes bastante fortes . Normalmente três elétrons são adicionados a um átomo de cromo, reduzindo -o ao estado de oxidação +3. Em solução ácida, o íon aquado Cr 3+ é produzido.
-
Cr
2O2−
7+ 14 H + + 6 e - → 2 Cr 3+ + 7 H 2 O ε 0 = 1,33 V
Em solução alcalina, o hidróxido de cromo (III) é produzido. O potencial redox mostra que os cromatos são agentes oxidantes mais fracos em solução alcalina do que em solução ácida.
-
CrO2−
4+ 4 H
2O + 3 e - → Cr (OH)
3+ 5 OH-
ε 0 = −0,13 V
Formulários
Aproximadamente 136.000 toneladas métricas (150.000 toneladas) de cromo hexavalente , principalmente dicromato de sódio, foram produzidas em 1985. Cromatos e dicromatos são usados no revestimento de cromo para proteger os metais da corrosão e melhorar a aderência da tinta. Os sais de cromato e dicromato de metais pesados , lantanídeos e metais alcalino-terrosos são apenas ligeiramente solúveis em água e, portanto, são usados como pigmentos. O pigmento amarelo cromo contendo chumbo foi usado por muito tempo antes que as regulamentações ambientais desencorajassem seu uso. Quando usados como agentes oxidantes ou titulantes em uma reação química redox , os cromatos e dicromatos se convertem em cromo trivalente, Cr 3+ , cujos sais normalmente têm uma cor azul-esverdeada distintamente diferente.
Ocorrência natural e produção
O principal minério de cromo é o óxido metálico misto de cromita , FeCr 2 O 4 , encontrado na forma de grânulos ou cristais pretos metálicos frágeis. O minério de cromita é aquecido com uma mistura de carbonato de cálcio e carbonato de sódio na presença de ar. O cromo é oxidado à forma hexavalente, enquanto o ferro forma óxido de ferro (III), Fe 2 O 3 :
- 4 FeCr 2 O 4 + 8 Na 2 CO 3 + 7 O 2 → 8 Na 2 CrO 4 + 2 Fe 2 O 3 + 8 CO 2
A lixiviação subsequente deste material em temperaturas mais altas dissolve os cromatos, deixando um resíduo de óxido de ferro insolúvel. Normalmente, a solução de cromato é posteriormente processada para produzir cromo metálico, mas um sal de cromato pode ser obtido diretamente do licor.
Minerais contendo cromato são raros. A crocoita, PbCrO 4 , que pode ocorrer como cristais vermelhos longos espetaculares, é o mineral cromato mais comumente encontrado. Minerais raros de cromato de potássio e compostos relacionados são encontrados no deserto de Atacama . Entre eles está a lópezita - o único mineral dicromato conhecido.
Toxicidade
Todos os compostos de cromo hexavalente são tóxicos (devido ao seu poder oxidante) e carcinogênicos ( IARC Grupo 1 ), especialmente se transportados pelo ar e inalados onde causam câncer de pulmão . Também associações positivas foram observadas entre a exposição a compostos de cromo (VI) e câncer de nariz e seios nasais . O uso de compostos de cromato em produtos manufaturados é restrito na UE (e pelo mercado comum no resto do mundo) pela diretiva do Parlamento da UE sobre a Diretiva de Restrição de Substâncias Perigosas (RoHS) (2002/95 / EC) .