Óxido de berílio - Beryllium oxide
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Monóxido de berílio (II) |
|
|
Nome IUPAC sistemático
Oxoberyllium |
|
| Outros nomes
Beryllia, Thermalox, Bromellite, Thermalox 995.
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3902801 | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.013.758 |
| Número EC | |
| Malha | berílio + óxido |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1566 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Be O | |
| Massa molar | 25,011 g · mol −1 |
| Aparência | Cristais vítreos incolores |
| Odor | Inodoro |
| Densidade | 3,01 g / cm 3 |
| Ponto de fusão | 2.507 ° C (4.545 ° F; 2.780 K) |
| Ponto de ebulição | 3.900 ° C (7.050 ° F; 4.170 K) |
| 0,00002 g / 100 mL | |
| Gap de banda | 10,6 eV |
| Condutividade térmica | 330 W / (K · m) |
|
Índice de refração ( n D )
|
1.719 |
| Estrutura | |
| Hexagonal | |
| P6 3 mc | |
| C 6v | |
| Tetragonal | |
| Linear | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
25,5 J / (K · mol) |
|
Entropia molar padrão ( S |
13,73-13,81 J / (K · mol) |
| -599 kJ / mol | |
|
Energia livre de Gibbs (Δ f G ˚)
|
-582 kJ / mol |
| Perigos | |
| Riscos principais | Muito tóxico, cancerígeno |
| Ficha de dados de segurança | Veja: página de dados |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H301 , H315 , H317 , H319 , H330 , H335 , H350 , H372 | |
| P201 , P260 , P280 , P284 , P301 + 310 , P305 + 351 + 338 | |
| NFPA 704 (diamante de fogo) | |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
2.062 mg / kg (camundongo, oral) |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 0,002 mg / m 3 C 0,005 mg / m 3 (30 minutos), com um pico máximo de 0,025 mg / m 3 (como Be) |
|
REL (recomendado)
|
Ca C 0,0005 mg / m 3 (como Be) |
|
IDLH (perigo imediato)
|
Ca [4 mg / m 3 (as Be)] |
| Compostos relacionados | |
|
Outros ânions
|
Telureto de berílio |
|
Outros cátions
|
|
| Página de dados suplementares | |
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
| UV , IR , NMR , MS | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O óxido de berílio ( BeO ), também conhecido como berílio , é um composto inorgânico com a fórmula BeO. Este sólido incolor é um isolante elétrico notável com uma condutividade térmica mais alta do que qualquer outro não metálico, exceto o diamante , e excede a da maioria dos metais. Como um sólido amorfo , o óxido de berílio é branco. Seu alto ponto de fusão leva ao seu uso como material refratário . Ocorre na natureza como bromelite mineral . Historicamente e na ciência dos materiais, o óxido de berílio foi chamado de glucina ou óxido de glucínio.
Preparação e propriedades químicas
O óxido de berílio pode ser preparado pela calcinação (torrefação) do carbonato de berílio , desidratação do hidróxido de berílio ou ignição do berílio metálico :
- BeCO 3 → BeO + CO 2
- Be (OH) 2 → BeO + H 2 O
- 2 Be + O 2 → 2 BeO
A ignição do berílio no ar dá uma mistura de BeO e nitreto de Be 3 N 2 . Ao contrário dos óxidos formados pelos outros elementos do Grupo 2 (metais alcalino-terrosos), o óxido de berílio é anfotérico em vez de básico.
O óxido de berílio formado em altas temperaturas (> 800 ° C) é inerte, mas se dissolve facilmente em bifluoreto de amônio aquoso quente (NH 4 HF 2 ) ou uma solução de ácido sulfúrico concentrado quente (H 2 SO 4 ) e sulfato de amônio ((NH 4 ) 2 SO 4 ).
Estrutura
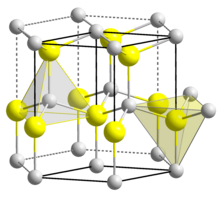
BeO cristaliza na estrutura wurtzita hexagonal , apresentando centros tetraédricos Be 2+ e O 2− , como lonsdaleita e w- BN (com ambos os quais é isoeletrônico ). Em contraste, os óxidos dos metais do grupo 2 maior, ou seja, MgO , CaO , SrO , BaO , cristalizam no motivo de sal-gema cúbico com geometria octaédrica em torno dos dianiões e diânions. Em alta temperatura, a estrutura se transforma em uma forma tetragonal.
Na fase de vapor, o óxido de berílio está presente como moléculas diatômicas discretas . Na linguagem da teoria das ligações de valência , essas moléculas podem ser descritas como adotando a hibridização orbital sp em ambos os átomos, caracterizando um σ (entre um orbital sp em cada átomo) e uma ligação π (entre orbitais p alinhados em cada átomo orientado perpendicularmente ao eixo molecular). A teoria orbital molecular fornece uma imagem ligeiramente diferente sem ligação sigma líquida (porque os orbitais 2 s dos dois átomos se combinam para formar um orbital de ligação sigma preenchido e um orbital anti-ligação sigma * preenchido) e duas ligações pi formadas entre os dois pares de orbitais p orientados perpendicularmente ao eixo molecular. O orbital sigma formado pelos orbitais p alinhados ao longo do eixo molecular não está preenchido. O estado fundamental correspondente é ... (2sσ) 2 (2sσ *) 2 (2pπ) 4 (como na molécula C 2 isoeletrônica ), onde ambas as ligações podem ser consideradas ligações dativas do oxigênio para o berílio.
Formulários
Cristais de alta qualidade podem ser cultivados hidrotermicamente ou de outra forma pelo método Verneuil . Na maior parte, o óxido de berílio é produzido como um pó branco amorfo, sinterizado em formas maiores. Impurezas, como o carbono, podem dar uma variedade de cores aos cristais hospedeiros, de outra forma incolores.
O óxido de berílio sinterizado é uma cerâmica muito estável . O óxido de berílio é usado em motores de foguete e como um revestimento protetor transparente em espelhos telescópicos aluminizados .
O óxido de berílio é usado em muitas peças semicondutoras de alto desempenho para aplicações como equipamentos de rádio porque tem boa condutividade térmica ao mesmo tempo que é um bom isolante elétrico. É usado como enchimento em alguns materiais de interface térmica, como graxa térmica . Alguns dispositivos semicondutores de potência têm usado cerâmica de óxido de berílio entre o chip de silício e a base de montagem de metal da embalagem para atingir um valor mais baixo de resistência térmica do que uma construção semelhante de óxido de alumínio . Ele também é usado como uma cerâmica estrutural para dispositivos de micro-ondas de alto desempenho, tubos de vácuo , magnetrons e lasers de gás . BeO foi proposto como um moderador de nêutrons para reatores navais marítimos de alta temperatura refrigerados a gás (MGCR), bem como o reator nuclear Kilopower da NASA para aplicações espaciais.
Segurança
BeO é cancerígeno na forma de pó e pode causar beriliose de doença pulmonar alérgica crônica . Depois de queimado na forma sólida, é seguro manusear se não for submetido a usinagem que gera poeira. A quebra limpa libera pouca poeira, mas ações de trituração ou trituração podem representar um risco. A cerâmica de óxido de berílio não é um resíduo perigoso segundo as leis federais dos EUA.

