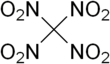Tetranitrometano - Tetranitromethane
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Tetranitrometano
|
|||
| Outros nomes
TNM
Tetan |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,007,359 |
||
| Número EC | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1510 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| CN 4 O 8 | |||
| Massa molar | 196,04 g / mol | ||
| Aparência | Líquido ou sólido incolor a amarelo pálido | ||
| Odor | Pungente | ||
| Densidade | 1,623 g / cm 3 | ||
| Ponto de fusão | 13,8 ° C (56,8 ° F; 286,9 K) | ||
| Ponto de ebulição | 126 ° C (259 ° F; 399 K) | ||
| insol | |||
| Pressão de vapor | 8 mmHg (20 ° C) | ||
| -43,02 · 10 −6 cm 3 / mol | |||
| Perigos | |||
| Riscos principais | Oxidante, pode formar misturas explosivas | ||
| Ficha de dados de segurança | ICSC 1468 | ||
| Pictogramas GHS |
   
|
||
| Palavra-sinal GHS | Perigo | ||
| H271 , H301 , H315 , H319 , H330 , H335 , H351 | |||
| P201 , P202 , P210 , P220 , P221 , P260 , P261 , P264 , P270 , P271 , P280 , P281 , P283 , P284 , P301 + 310 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P306 + 360 , P308 + 313 , P310 , P312 , P320 , P321 , P330 | |||
| NFPA 704 (diamante de fogo) | |||
| Dose ou concentração letal (LD, LC): | |||
|
LC 50 ( concentração média )
|
18 ppm (rato, 4 horas) 100 ppm (gato, 20 minutos) 54 ppm (camundongo, 4 horas) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 1 ppm (8 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 1 ppm (8 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
4 ppm | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
Hexanitroetano Octanitropentano Trinitrometano |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
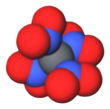
O tetranitrometano ou TNM é um oxidante orgânico com fórmula química C (NO 2 ) 4 . Sua estrutura química consiste em quatro grupos nitro ligados a um átomo de carbono. Em 1857 foi sintetizado pela primeira vez pela reação de cianoacetamida de sódio com ácido nítrico .
Usos
Foi investigado para uso como oxidante em foguetes bipropelentes ; no entanto, seu alto ponto de fusão o torna inadequado. O tetranitrometano altamente purificado não pode explodir, mas sua sensibilidade aumenta drasticamente por contaminantes oxidáveis, como aditivos anticongelantes. Isso o torna efetivamente inutilizável como propelente. No laboratório é utilizado como reagente para a detecção de ligações duplas em compostos orgânicos e como reagente nitrante. Também encontrou uso como aditivo ao combustível diesel para aumentar o número de cetano .
Preparação
TNM é um líquido amarelo claro que pode ser preparado em laboratório pela nitração de anidrido acético com ácido nítrico anidro (método de Chattaway). Este método foi tentado em escala industrial na década de 1950 pela Nitroform Products Company em Newark, EUA, mas a planta inteira foi destruída por uma explosão em 1953.
A primeira produção em escala industrial foi iniciada na Alemanha durante a Segunda Guerra Mundial, em um esforço para melhorar o índice de cetano do óleo diesel. Esse processo aprimorou o método original, que começou com ácido acético e ácido nítrico. Sem levar em conta o rendimento ou custo, aproximadamente 10 toneladas de TNM foram produzidas em poucas semanas. No entanto, este processo de produção não voltou a ser utilizado industrialmente após o fim da guerra, devido aos elevados custos associados.
Para uso comercial, foi usado um método mais barato começando com acetileno . Primeiro, o ácido nítrico contendo nitrato de mercúrio é reduzido pelo acetileno, resultando em trinitrometano (nitrofórmio) e uma mistura de dióxido de carbono e óxido de nitrogênio como gás residual. Os óxidos de nitrogênio são valiosos e normalmente recuperados como ácido nítrico em uma torre de absorção. O nitrofórmio resultante é convertido em TNM pela adição de ácido nítrico e ácido sulfúrico a temperaturas mais altas. Com este método, um rendimento de 90% (com base no ácido nítrico) antes que a purificação possa ser alcançada.
Estrutura
TNM é um excelente exemplo de flexibilidade molecular. Levou os métodos estruturais aos limites de sua aplicabilidade, como é demonstrado pelo fato de que a estrutura do TNM foi tentada a ser determinada por um período de mais de 70 anos em várias fases.
As primeiras investigações por difração de elétrons de gás não foram capazes de descrever o padrão de difração observado por completo e apenas a aplicação de um modelo quadridimensional relativo ao movimento correlacionado dos quatro grupos de NO 2 sobre as ligações CN foi capaz de descrever as observações experimentais completamente. O problema ocorre, porque a simetria local dupla das unidades C-NO 2 versus a simetria tripla da unidade C (NO 2 ) 3 , bem como a proximidade dos grupos NO 2 dificultando sua rotação livre, é a fonte de um movimento muito complicado, mutuamente impedido, dos grupos de NO 2 .
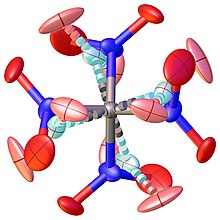
A estrutura de cristal também foi tentada várias vezes. Uma primeira solução decente para o problema exigiu um modelo que descreve uma fase cristalina de alta temperatura altamente desordenada de uma fase de alta temperatura (> 174,4 K), como é mostrado na Figura 1. A redução da simetria e a análise da geminação dos cristais levaram finalmente a um distúrbio resolvido da estrutura mostrada na Figura 2.
A estrutura de uma fase ordenada de baixa temperatura contém três moléculas independentes na unidade assimétrica. Os parâmetros estruturais das fases gasosa e sólida são listados na tabela a seguir para comparação.
| Parâmetro | GED | XRD (intervalo) |
| r C – N | 1,509 (5) | 1,502 (4) - 1,554 (5) |
| r N – O (eclipse) | 1,201 (3) | 1,198 (4) - 1,215 (5) |
| r N – O (veado) | 1,199 (3) | 1,178 (5) - 1,222 (4) |
| ∡NCN_1 | 105,1 (16) | 108,2 (3) - 110,9 (3) |
| ∡NCN_2 | 111,7 (8) | 107,3 (3) - 111,4 (2) |
| ∡NCN_3 | 106,6 (2) - 107,1 (3) | |
| ∡ONO | 129,2 (17) | 128,0 (4) - 132,3 (4) |
Segurança
A capacidade de detonação do TNM é muito afetada pela presença de impurezas, mesmo em pequenas quantidades. TNM forma misturas explosivas extremamente poderosas quando os combustíveis são adicionados em proporções estequiométricas. Muitas dessas misturas apresentam sensibilidade ao impacto ainda maior do que a da nitroglicerina .
O tetranitrometano pode ser usado como um componente de explosivos líquidos altamente explosivos como um agente oxidante. Forma misturas altamente explosivas com todas as substâncias inflamáveis. Ao fazer experiências com esta substância, não use papel para filtrar! Mesmo pequenas impurezas tornam o tetranitrometano um explosivo que explode com o impacto ou atrito. Um experimento trágico de palestra na Universidade de Münster em 1920 é bem conhecido, onde um pequeno tubo de aço contendo tetranitrometano, tolueno e algodão absorvente detonou pouco antes de queimar de tal forma que mais de 30 alunos ficaram feridos, alguns gravemente; no entanto, com base nos registros do gabinete do reitor, até 10 mortes e mais de uma dúzia de feridos estão documentados. Em seguida, o Reichsanstalt químico-técnico alemão determinou uma velocidade de detonação de 9300 metros por segundo. Alfred Stettbacher então provou comparativamente que essa mistura era muito mais explosiva do que hexogênio , pentrita , gelatina explosiva ou panclastita e, portanto, representava o explosivo mais destrutivo de todos.
TNM reage com a umidade em pH elevado para produzir trinitrometano (nitrofórmio) que reage facilmente com metais para formar sais altamente instáveis e explosivos.
O tetranitrometano é altamente tóxico. A absorção de apenas 2,5 mg / kg pode causar metemoglobinemia , edema pulmonar e danos ao fígado, rins e sistema nervoso central. É razoavelmente esperado que seja um carcinógeno humano.