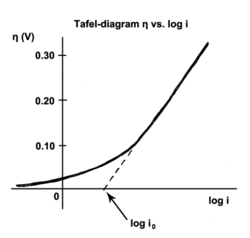
Equação de Tafel - Tafel equation
A equação de Tafel é uma equação em cinética eletroquímica que relaciona a taxa de uma reação eletroquímica ao superpotencial . A equação de Tafel foi primeiro deduzida experimentalmente e mais tarde demonstrou ter uma justificativa teórica. A equação leva o nome do químico suíço Julius Tafel .
"Ele descreve como a corrente elétrica através de um eletrodo depende da diferença de voltagem entre o eletrodo e o eletrólito em massa para uma reação redox simples e unimolecular".
Quando uma reação eletroquímica ocorre em duas meias reações em eletrodos separados , a equação de Tafel é aplicada a cada eletrodo separadamente. Em um único eletrodo, a equação de Tafel pode ser declarada como:
-
( 1 )
Onde
- o sinal de mais sob o expoente se refere a uma reação anódica e um sinal de menos a uma reação catódica,
- : overpotential
- : " Declive Tafel ", V
- : densidade de corrente , A / m 2
- : " densidade de corrente de troca ", A / m 2 .
Uma verificação e mais explicações para esta equação podem ser encontradas aqui. A equação de Tafel é uma aproximação da equação de Butler-Volmer no caso de .
"[A equação de Tafel] assume que as concentrações no eletrodo são praticamente iguais às concentrações no eletrólito bruto, permitindo que a corrente seja expressa apenas em função do potencial. Em outras palavras, assume que a taxa de transferência de massa do eletrodo é muito maior do que a taxa de reação, e que a reação é dominada pela taxa de reação química mais lenta ".
Além disso, em um determinado eletrodo, a equação de Tafel assume que a taxa de meia reação reversa é desprezível em comparação com a taxa de reação direta.
Visão geral dos termos
A corrente de troca é a corrente em equilíbrio, ou seja, a taxa na qual espécies oxidadas e reduzidas transferem elétrons com o eletrodo. Em outras palavras, a densidade da corrente de troca é a taxa de reação no potencial reversível (quando o sobrepotencial é zero por definição). No potencial reversível, a reação está em equilíbrio, o que significa que as reações direta e reversa progridem nas mesmas taxas. Essa taxa é a densidade da corrente de câmbio.
A inclinação Tafel é medida experimentalmente. Pode, no entanto, ser mostrado teoricamente que quando o mecanismo de reação dominante envolve a transferência de um único elétron que
onde A é definido como
-
( 2 )
Onde
- é a constante de Boltzmann ,
- é a temperatura absoluta ,
- é a carga elétrica elementar de um elétron,
- é a tensão térmica , e
- é o " coeficiente de transferência de carga ", cujo valor deve estar entre 0 e 1.
Equação em caso de transferência de massa de eletrodo não desprezível
Em um caso mais geral,
"A seguinte derivação da equação de Butler-Volmer estendida é adaptada daquela de Bard e Faulkner e Newman e Thomas-Alyea". "[...] a corrente é expressa como uma função não apenas do potencial (como na versão simples), mas também das concentrações dadas. A taxa de transferência de massa pode ser relativamente pequena, mas seu único efeito no produto químico a reação é através das concentrações alteradas (dadas). Na verdade, as concentrações também são função do potencial ".
A equação de Tafel também pode ser escrita como:
-
( 3 )
Onde
- n é o número de elétrons trocados, como na equação de Nernst ,
- o sinal de mais sob o expoente se refere a uma reação anódica e um sinal de menos a uma reação catódica,
- k é a constante de velocidade para a reação do eletrodo em s −1 ,
- R é a constante universal do gás ,
- C é a concentração de espécies reativas na superfície do eletrodo em mol / m².
Demonstração
Como visto na equação ( 1 ),
, então:
, como visto na equação ( 2 ) e porque .
Porque
devido à transferência de massa do eletrodo , que finalmente produz a equação ( 3 ).
Equação em caso de valores baixos de polarização
Uma outra equação é aplicável a baixos valores de polarização . Nesse caso, a dependência da corrente na polarização é geralmente linear (não logarítmica):
Essa região linear é chamada de resistência de polarização devido à sua semelhança formal com a lei de Ohm .
Veja também
- Superpotencial
- Equação Butler-Volmer
- Eletrocatalisador
- Limitando a corrente
- Leis de eletrólise de Faraday
Referências
- GT Burstein (2005). "A Century of Tafel's Equation: 1905–2005 A Commemorative Issue of Corrosion Science". Corrosion Science . 47 (12): 2858–2870. doi : 10.1016 / j.corsci.2005.07.002 .
links externos
-
 Mídia relacionada à equação de Tafel no Wikimedia Commons
Mídia relacionada à equação de Tafel no Wikimedia Commons