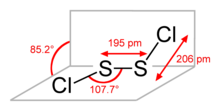
Dicloreto de dissulfur - Disulfur dichloride
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Dicloreto de dissulfur
|
|||
|
Nome IUPAC sistemático
Diclorodisulfano |
|||
| Outros nomes
Bis [cloridosulfur] ( S - S )
Cloreto sulfênico dimérico |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard |
100.030.021 |
||
| Número EC | |||
| Malha | Enxofre + monocloreto | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 3390 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| S 2 Cl 2 | |||
| Massa molar | 135,04 g / mol | ||
| Aparência | Líquido oleoso de âmbar claro a amarelo-vermelho | ||
| Odor | picante, nauseante, irritante | ||
| Densidade | 1,688 g / cm 3 | ||
| Ponto de fusão | −80 ° C (−112 ° F; 193 K) | ||
| Ponto de ebulição | 137,1 ° C (278,8 ° F; 410,2 K) | ||
| decompõe-se, com perda de HCl | |||
| Solubilidade | solúvel em etanol , benzeno , éter , clorofórmio , CCl 4 | ||
| Pressão de vapor | 7 mmHg (20 ° C) | ||
| −62,2 · 10 −6 cm 3 / mol | |||
|
Índice de refração ( n D )
|
1.658 | ||
| Estrutura | |||
| C 2 , gauche | |||
| 1,60 D | |||
| Perigos | |||
| Ficha de dados de segurança | ICSC 0958 | ||
| Tóxico ( T ) Nocivo ( Xn ) Corrosivo ( C ) Perigoso para o meio ambiente ( N ) |
|||
| Frases R (desatualizado) | R14 , R20 , R25 , R29 , R35 , R50 | ||
| Frases S (desatualizado) | (S1 / 2) , S26 , S36 / 37/39 , S45 , S61 | ||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 118,5 ° C (245,3 ° F; 391,6 K) | ||
| 234 ° C (453 ° F; 507 K) | |||
| Dose ou concentração letal (LD, LC): | |||
|
LC Lo (o mais baixo publicado )
|
150 ppm (mouse, 1 min) | ||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 1 ppm (6 mg / m 3 ) | ||
|
REL (recomendado)
|
C 1 ppm (6 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
5 ppm | ||
| Compostos relacionados | |||
|
Cloretos de enxofre relacionados
|
Dicloreto de enxofre Cloreto de tionila Cloreto de sulfurila |
||
|
Compostos relacionados
|
Difluoreto de dissulfur Dibrometo de dissulfur |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O dicloreto de dissulfur é o composto inorgânico de enxofre e cloro com a fórmula S 2 Cl 2 .
Alguns nomes alternativos para este composto são monocloreto de enxofre (o nome implícito em sua fórmula empírica , SCl), dicloreto de dissulfur (British English Spelling) e enxofre monocloride (British English Spelling). S 2 Cl 2 tem a estrutura implícita na fórmula Cl − S − S − Cl, onde o ângulo entre os planos Cl a −S − S e S − S − Cl b é de 90 °. Essa estrutura é conhecida como gauche e é semelhante à do H 2 O 2 . Um isômero raro de S 2 Cl 2 é S = SCl 2 ; este isômero se forma transitoriamente quando S 2 Cl 2 é exposto à radiação UV (veja tiossulfóxidos ).
Síntese, propriedades básicas, reações
O dicloreto de dissulfur puro é um líquido amarelo que "fumega" no ar úmido devido à reação com a água. Uma equação idealizada (mas complicada) é:
- 16 S 2 Cl 2 + 16 H 2 O → 8 SO 2 + 32 HCl + 3 S 8
É produzido por cloração parcial do enxofre elementar. A reação prossegue a taxas utilizáveis à temperatura ambiente. No laboratório, o gás cloro é conduzido para um frasco contendo enxofre elementar. Conforme o dicloreto de dissulfur é formado, o conteúdo se torna um líquido amarelo dourado:
- S 8 + 4 Cl 2 → 4 S 2 Cl 2 , ΔH = −58,2 kJ / mol
O excesso de cloro produz dicloreto de enxofre , que faz com que o líquido se torne menos amarelo e mais vermelho alaranjado:
- S 2 Cl 2 + Cl 2 ↔ 2 SCl 2 , ΔH = −40,6 kJ / mol
A reação é reversível e, após repouso, o SCl 2 libera cloro para reverter para o dicloreto de dissulfur. O dicloreto de dissulfur tem a capacidade de dissolver grandes quantidades de enxofre, o que reflete em parte a formação de polissulfanos :
- S 2 Cl 2 + n S → S 2 + n Cl 2
O dicloreto de dissulfur pode ser purificado por destilação do excesso de enxofre elementar.
S 2 Cl 2 também surge da cloração de CS 2 como na síntese de tiofosgênio .
Reações
S 2 Cl 2 hidrolisa em dióxido de enxofre e enxofre elementar. Quando tratados com sulfeto de hidrogênio, os polissulfanos são formados conforme indicado na seguinte fórmula idealizada:
- 2 H 2 S + S 2 Cl 2 → H 2 S 4 + 2 HCl
Ele reage com a amônia para dar heptassulfur imida (S 7 NH) e anéis S − N relacionados S 8 − x (NH) x (x = 2, 3).
Formulários
S 2 Cl 2 foi usado para introduzir ligações C − S. Na presença de cloreto de alumínio (AlCl 3 ), S 2 Cl 2 reage com benzeno para dar sulfeto de difenila:
- S 2 Cl 2 + 2 C 6 H 6 → (C 6 H 5 ) 2 S + 2 HCl + 1/8 S 8
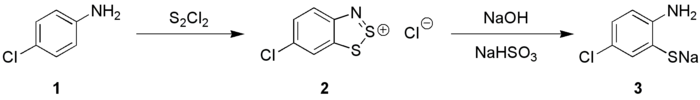
Anilinas (1) reagem com S 2 Cl 2 na presença de NaOH para dar sais de 1,2,3-benzoditiazólio (2) ( reação de Herz ) que podem ser transformados em orto- aminotiofenolatos (3), essas espécies são precursoras de tioíndigo tinturas.
Também é usado para preparar mostarda de enxofre , comumente conhecida como "gás de mostarda", por reação com etileno a 60 ° C (processo Levinstein):
- S 2 Cl 2 + 2 C 2 H 4 → (ClC 2 H 4 ) 2 S + 1/8 S 8
Outros usos de S 2 Cl 2 incluem a fabricação de corantes de enxofre, inseticidas e borrachas sintéticas. Também é utilizado na vulcanização a frio de borrachas, como catalisador de polimerização de óleos vegetais e para o endurecimento de madeiras macias.
Segurança e regulamentação
Esta substância está listada no Anexo 3 Parte B - Produtos Químicos Precursores da Convenção de Armas Químicas (CWC). Instalações que produzem e / ou processam e / ou consomem produtos químicos programados podem estar sujeitas a controle, mecanismos de relatório e inspeção pela OPAQ (Organização para a Proibição de Armas Químicas).