Grupo Pentil - Pentyl group
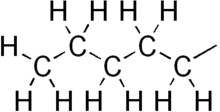
|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
|
|
|
| Propriedades | |
|
C 5 H 11 • |
|
| Massa molar | 71,1408 g mol −1 |
| Reage | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
Em química orgânica , pentil é um grupo alquil de cinco carbonos ou substituinte com a fórmula química -C 5 H 11 . É a forma substituinte do alcano pentano .
Na literatura mais antiga, o nome comum não sistemático amila era freqüentemente usado para o grupo pentila. Por outro lado, o nome pentil foi usado para vários grupos alquil ramificados de cinco carbonos, distinguidos por vários prefixos.
Um grupo ciclopentil é um anel com a fórmula -C 5 H 9 .
O nome também é usado para o radical pentil , um grupo pentil como uma molécula isolada. Este radical livre só é observado em condições extremas. Sua fórmula costuma ser escrita " C
5 H
11 • "ou" • C
5 H
11 "para indicar que tem uma ligação de valência não satisfeita .
Grupos "pentil" mais antigos
Os seguintes nomes ainda são usados às vezes:
| Nome | Estrutura | Status IUPAC | IUPAC recomendado. | Exemplos |
|---|---|---|---|---|
| n- pentil |
H 3 C - ( CH 2 ) 4 - |
pentil | ||
| terc- pentil |
H 3 C - CH 2 - ( H 3 C -) 2 C− |
Não é mais recomendado | 2-metilbutan-2-il (também conhecido como (1,1-Dimetilpropil) | |
| neopentil |
( H 3 C -) 3 C− CH 2 - |
Não é mais recomendado | 2,2-dimetilpropil | |
| isopentil |
( H 3 C -) 2 CH− ( CH 2 ) 2 - |
Não é mais recomendado | 3-metilbutil | |
| sec- pentil |
H 3 C - ( CH 2 ) 2 - ( H 3 C -) CH− |
pentan-2-il (ou (1-metilbutil)) | ||
| 3-pentil |
( H 3 C - CH 2 -) 2 CH− |
pentan-3-il (também conhecido como (1-etilpropil)) | ||
| sec -isopentil |
( H 3 C -) 2 CH - ( H 3 C -) CH− |
3-metilbutan-2-il (ou (1,2-Dimetilpropil) | ||
| pentil ativo |
H 3 C - CH 2 - ( H 3 C -) CH− CH 2 - |
2-metilbutil |
Radical pentil
O radical livre pentil foi estudado por Pacansky e Gutierrez em 1983. O radical foi obtido pela exposição do peróxido de bishexanoíla aprisionado no argônio congelado à luz ultravioleta , que causou sua decomposição em dois dióxido de carbono ( CO
2 ) moléculas e dois radicais pentil.
