PAX8 - PAX8
O gene 8 da caixa emparelhada , também conhecido como PAX8 , é uma proteína que, em humanos, é codificada pelo gene PAX8 .
Função
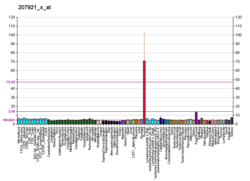
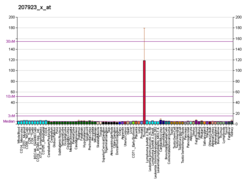
Este gene é membro da família de fatores de transcrição da caixa pareada ( PAX ) . Os membros desta família de genes normalmente codificam proteínas que contêm um domínio de caixa emparelhado , um octapeptídeo e um homeodomínio de tipo emparelhado . A família de genes PAX tem um papel importante na formação de tecidos e órgãos durante o desenvolvimento embrionário e na manutenção da função normal de algumas células após o nascimento. Os genes PAX fornecem instruções para a produção de proteínas que se ligam a certas áreas do DNA. Esta proteína nuclear está envolvida no desenvolvimento das células foliculares da tireoide e na expressão de genes específicos da tireoide. PAX8 libera hormônios importantes para regular o crescimento, o desenvolvimento do cérebro e o metabolismo. Também funciona nos estágios iniciais da organogênese renal, no sistema mülleriano e no timo. Além disso, o PAX8 é expresso no sistema excretor renal, células epiteliais da endocérvice, endométrio, ovário, trompa de Falópio, vesícula seminal, epidídimo, células das ilhotas pancreáticas e células linfóides. PAX8 e outros fatores de transcrição desempenham um papel na ligação ao DNA e na regulação dos genes que conduzem a síntese do hormônio tireoidiano (Tg, TPO, Slc5a5 e Tshr).
PAX8 (e PAX2) é um dos reguladores importantes da morfogênese do sistema urogenital. Eles desempenham um papel na especificação das primeiras células renais do embrião e permanecem como atores essenciais ao longo do desenvolvimento.
Foi demonstrado que o PAX8 interage com o homeobox 1 do NK2 .
Significado clínico
O gene PAX8 também está associado ao hipotireoidismo congênito devido à disgenesia tireoidiana devido ao seu papel no crescimento e desenvolvimento da glândula tireoide. Uma mutação no gene PAX8 pode prevenir ou interromper o desenvolvimento normal. Essas mutações podem afetar diferentes funções da proteína, incluindo ligação ao DNA, ativação do gene, estabilidade da proteína e cooperação com o coativador p300. As deficiências do gene PAX podem resultar em defeitos de desenvolvimento chamados Anomalias Congênitas do Rim e do Trato Urinário (CAKUT).
Câncer
As mutações PAX8 estão associadas a várias formas de câncer.
Mecanismos
PAX8 é considerado um "fator de transcrição do regulador mestre". Como regulador mestre, é possível que regule a expressão de genes diferentes dos específicos da tireoide. Vários genes supressores de tumor conhecidos, como TP53 e WT1, foram identificados como alvos de transcrição em células de astrocitoma humano. Mais de 90% dos tumores da tireoide surgem de células foliculares da tireoide. Uma proteína de fusão, PAX8-PPAR-γ , está implicada em alguns carcinomas foliculares da tireoide e carcinoma papilar da tireoide variante folicular. O mecanismo para essa transformação não é bem conhecido, mas existem várias possibilidades propostas.
- Inibição da função normal do PPAR y pela proteína quimérica PAX8 / PPARy por meio de um efeito negativo dominante
- Ativação de alvos PPARy normais devido à superexpressão da proteína quimérica que contém todos os domínios funcionais de PPARy de tipo selvagem
- Desregulação da função PAX8
- Ativação de um conjunto de genes não relacionados às vias de PPARy e PAX8 de tipo selvagem
O gene PAX 8 tem alguma associação com tumores foliculares da tireoide. Foi observado que os tumores positivos para PAX8 / PPAR y raramente expressam mutações RAS em combinação. Isso sugere que os carcinomas foliculares se desenvolvem em duas vias distintas com PAX8 / PPARy ou RAS .
Variantes de splice da transcrição alternativa, codificando diferentes isoformas, foram caracterizadas. O mecanismo de ativação dos genes é desconhecido. Alguns estudos sugeriram que os genes renais PAX atuam como fatores pró-sobrevivência e permitem que as células tumorais resistam à apoptose. A regulação negativa da expressão do gene PAX inibe o crescimento celular e induz a apoptose. Este poderia ser um caminho possível para alvos terapêuticos no câncer renal.
Alguns estudos de sequenciamento do genoma completo mostraram que PAX8 também tem como alvo BRCA1 (carcinogênese), vias de MAPK (doenças malignas da tireoide) e Ccnb1 e Ccnb2 (processos do ciclo celular). PAX8 mostra estar envolvido na proliferação e diferenciação de células tumorais, transdução de sinal, apoptose, polaridade e transporte celular, motilidade e adesão celular.
Tipos de câncer associados
Mutações neste gene têm sido associadas à disgenesia da tireoide , carcinomas foliculares da tireoide e adenomas foliculares atípicos da tireoide .
O rearranjo PAX8 / PPARy é responsável por 30-40% dos carcinomas foliculares do tipo convencional e menos de 5% dos carcinomas oncocíticos (também conhecidos como neoplasias de células de Hurthle).
A expressão de PAX8 está aumentada em tecidos renais neoplásicos, tumores de Wilms, câncer de ovário e carcinomas de Müller. Por esse motivo, a imunodetecção de PAX8 é amplamente utilizada para o diagnóstico de tumores renais primários e metastáticos. A reativação da expressão de PAX8 (ou Pax2) foi relatada em tumores Wilms pediátricos, quase todos os subtipos de carcinoma de células renais, adenomas nefrogênicos, células de câncer de ovário, bexiga, próstata e carcinomas endometriais. A expressão de PAX8 também é induzida durante o desenvolvimento do câncer cervical.
Os tumores que expressam o PAX8 / PPARy estão geralmente presentes em uma idade jovem, são pequenos em tamanho, apresentam um padrão de crescimento sólido / aninhado e frequentemente envolvem invasão vascular.
Veja também
Referências
Leitura adicional
- Poleev A, Fickenscher H, Mundlos S, Winterpacht A, Zabel B, Fidler A, Gruss P, Plachov D (novembro de 1992). "PAX8, um gene da caixa pareada humana: isolamento e expressão no desenvolvimento de tumores de tireóide, rim e Wilms". Desenvolvimento . 116 (3): 611–23. doi : 10.1242 / dev.116.3.611 . PMID 1337742 .
- Poleev A, Wendler F, Fickenscher H, Zannini MS, Yaginuma K, Abbott C, Plachov D (março de 1995). "Propriedades funcionais distintas de três proteínas de caixa pareada humana, PAX8, isoformas geradas por splicing alternativo em tumores de tireóide, rim e Wilms". European Journal of Biochemistry / FEBS . 228 (3): 899–911. doi : 10.1111 / j.1432-1033.1995.tb20338.x . PMID 7737192 .
- Stapleton P, Weith A, Urbánek P, Kozmik Z, Busslinger M (abril de 1993). "Localização cromossômica de sete genes PAX e clonagem de um novo membro da família, PAX-9". Nature Genetics . 3 (4): 292–8. doi : 10.1038 / ng0493-292 . PMID 7981748 . S2CID 21338655 .
- Maruyama K, Sugano S (janeiro de 1994). "Oligo-capping: um método simples para substituir a estrutura cap de mRNAs eucarióticos com oligoribonucleotídeos". Gene . 138 (1–2): 171–4. doi : 10.1016 / 0378-1119 (94) 90802-8 . PMID 8125298 .
- Kozmik Z, Kurzbauer R, Dörfler P, Busslinger M (outubro de 1993). "O splicing alternativo de transcritos do gene Pax-8 é regulado pelo desenvolvimento e gera isoformas com diferentes propriedades de transativação" . Biologia Molecular e Celular . 13 (10): 6024–35. doi : 10.1128 / mcb.13.10.6024 . PMC 364662 . PMID 8413205 .
- Pilz AJ, Povey S, Gruss P, Abbott CM (1993). "Mapeamento dos homólogos humanos dos genes contendo caixa emparelhada murina". Mammalian Genome . 4 (2): 78–82. doi : 10.1007 / BF00290430 . PMID 8431641 . S2CID 30845070 .
- Bonaldo MF, Lennon G, Soares MB (setembro de 1996). "Normalização e subtração: duas abordagens para facilitar a descoberta do gene" . Genome Research . 6 (9): 791–806. doi : 10.1101 / gr.6.9.791 . PMID 8889548 .
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K, Suyama A, Sugano S (outubro de 1997). "Construção e caracterização de uma biblioteca de cDNA enriquecida em comprimento total e enriquecida na extremidade 5 '". Gene . 200 (1–2): 149–56. doi : 10.1016 / S0378-1119 (97) 00411-3 . PMID 9373149 .
- Fraizer GC, Shimamura R, Zhang X, Saunders GF (dezembro de 1997). "PAX 8 regula a transcrição de WT1 humano através de um novo sítio de ligação ao DNA" . The Journal of Biological Chemistry . 272 (49): 30678–87. doi : 10.1074 / jbc.272.49.30678 . PMID 9388203 .
- Macchia PE, Lapi P, Krude H, Pirro MT, Missero C, Chiovato L, Souabni A, Baserga M, Tassi V, Pinchera A, Fenzi G, Grüters A, Busslinger M, Di Lauro R (maio de 1998). "Mutações PAX8 associadas ao hipotireoidismo congênito causado pela disgenesia da tireoide". Nature Genetics . 19 (1): 83–6. doi : 10.1038 / ng0598-83 . PMID 9590296 . S2CID 33957230 .
- Mansouri A, Chowdhury K., Gruss P (maio de 1998). "As células foliculares da glândula tireóide requerem a função do gene Pax8". Nature Genetics . 19 (1): 87–90. doi : 10.1038 / ng0598-87 . PMID 9590297 . S2CID 205342136 .
- Tell G, Pellizzari L, Esposito G, Pucillo C, Macchia PE, Di Lauro R, Damante G (julho de 1999). "Defeitos estruturais de um mutante Pax8 que dão origem ao hipotireoidismo congênito" . The Biochemical Journal . 341 (1): 89–93. doi : 10.1042 / 0264-6021: 3410089 . PMC 1220333 . PMID 10377248 .
- De Leo R, Miccadei S, Zammarchi E, Civitareale D (novembro de 2000). "Papel para p300 na indução Pax 8 da expressão do gene da tireoperoxidase" . The Journal of Biological Chemistry . 275 (44): 34100–5. doi : 10.1074 / jbc.M003043200 . PMID 10924503 .
- Roberts EC, Deed RW, Inoue T, Norton JD, Sharrocks AD (janeiro de 2001). "As proteínas de hélice-alça-hélice id antagonizam a atividade do fator de transcrição pax pela inibição da ligação ao DNA" . Biologia Molecular e Celular . 21 (2): 524–33. doi : 10.1128 / MCB.21.2.524-533.2001 . PMC 86614 . PMID 11134340 .
- Vilain C, Rydlewski C, Duprez L, Heinrichs C, Abramowicz M, Malvaux P, Renneboog B, Parma J, Costagliola S, Vassart G (janeiro de 2001). "Transmissão autossômica dominante de hipoplasia congênita da tireoide devido à mutação de perda de função de PAX8". The Journal of Clinical Endocrinology and Metabolism . 86 (1): 234–8. doi : 10.1210 / jc.86.1.234 . PMID 11232006 .
- Congdon T, Nguyen LQ, Nogueira CR, Habiby RL, Medeiros-Neto G, Kopp P (agosto de 2001). "Uma nova mutação (Q40P) em PAX8 associada com hipotireoidismo congênito e hipoplasia tireoidiana: evidência de variabilidade fenotípica em mãe e filho" . The Journal of Clinical Endocrinology and Metabolism . 86 (8): 3962–7. doi : 10.1210 / jc.86.8.3962 . PMID 11502839 .
- Miccadei S, De Leo R, Zammarchi E, Natali PG, Civitareale D (abril de 2002). "A atividade sinérgica do fator de transcrição da tireóide 1 e Pax 8 depende da interação promotor / intensificador" . Endocrinologia molecular . 16 (4): 837–46. doi : 10.1210 / me.16.4.837 . PMID 11923479 .
- Marques AR, Espadinha C, Catarino AL, Moniz S, Pereira T, Sobrinho LG, Leite V (agosto de 2002). "Expressão de rearranjos PAX8-PPAR gama 1 em ambos os carcinomas foliculares da tireóide e adenomas". The Journal of Clinical Endocrinology and Metabolism . 87 (8): 3947–52. doi : 10.1210 / jc.87.8.3947 . PMID 12161538 .
- Di Palma T, Nitsch R, Mascia A, Nitsch L, Di Lauro R, Zannini M (janeiro de 2003). "O fator Pax8 contendo o domínio emparelhado e o fator TTF-1 contendo o homeodomínio interagem diretamente e ativam sinergicamente a transcrição" . The Journal of Biological Chemistry . 278 (5): 3395–402. doi : 10.1074 / jbc.M205977200 . PMID 12441357 .
links externos
- PAX8 + proteína, + humano na Biblioteca Nacional de Medicina dos Estados Unidos em títulos de assuntos médicos (MeSH)
-
"Gene Xenbase: Resumo para pax8, espécie: Xenopus tropicalis" . Xenbase . xenbase.org . Página visitada em 17/07/2009 .
Um recurso de Xenopus laevis e tropicalis
Este artigo incorpora texto da Biblioteca Nacional de Medicina dos Estados Unidos , que é de domínio público .