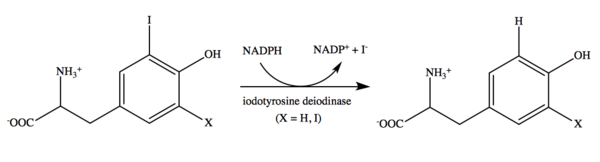
Iodotirosina desiodinase - Iodotyrosine deiodinase
| Iodotirosina deiodinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| EC nº | 1.21.1.1 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
A iodotirosina desiodinase, também conhecida como iodotirosina deshalogenase 1, é um tipo de enzima deiodinase que elimina o iodeto removendo-o de resíduos de tirosina iodada na glândula tireoide . Essas tirosinas iodadas são produzidas durante a biossíntese do hormônio tireoidiano . O iodeto eliminado pela iodotirosina desiodinase é necessário para sintetizar novamente os hormônios da tireoide. Após a síntese, os hormônios tireoidianos circulam pelo corpo para regular a taxa metabólica, a expressão de proteínas e a temperatura corporal. A iodotirosina desiodinase é, portanto, necessária para manter os níveis de iodeto e hormônios tireoidianos em equilíbrio.
A desalogenação em organismos aeróbios geralmente é feita por oxidação e hidrólise ; no entanto, a iodotirosina desiodase usa desalogenação redutiva. A iodotirosina desiodinase e a iodotironina desiodinase foram determinadas como as únicas duas enzimas conhecidas para catalisar a desalogenação redutiva em mamíferos. Embora essas duas enzimas desempenhem funções semelhantes, elas são estrutural e mecanicamente diferentes. A iodotironina desiodinase (não a enzima que é o tópico deste artigo) usa um sítio ativo de selenocisteína para catálise, é um membro da superfamília da tioredoxina e remove o iodeto apenas quando o substrato está na forma de tirosina dupla. Em contraste, a iodotirosina desiodinase (a enzima tópica) não requer selenocisteína ou cisteína para a catálise, faz parte da superfamília da NADH oxidase / flavina redutase e remove o iodeto quando o substrato é um único aminoácido . A pesquisa sobre a iodotirosina desiodase tem sido historicamente variável e lenta devido à sua falta de estabilidade e purificação árdua. Só recentemente essa enzima foi estudada mais profundamente.
Estrutura
O gene que codifica essa enzima foi identificado recentemente. A sequência de aminoácidos da iodotirosina desiodinase é altamente conservada entre os mamíferos e contém três domínios. A iodotirosina desiodinase é uma proteína de membrana , com o terminal N funcionando como uma âncora de membrana. Ele forma um dímero que é trocado por domínio. Inicialmente, pensava-se que a iodotirosina desiodase continha apenas um mononucleotídeo de flavina (FMN) em cada dímero, mas agora acredita-se que a iodotirosina desiodinase tenha duas moléculas de FMN para cada homodímero. A enzima tem uma dobra α-β característica que todas as proteínas da superfamília NADH oxidase / flavina redutase também têm. Dentro da interface do dímero, existem dois locais ativos equivalentes , cada um feito de resíduos de ambas as subunidades. Assim, a associação de subunidades deve ser necessária para a ligação e catálise de FMN. A ligação do substrato causa uma mudança conformacional na enzima de modo a fechar o sítio ativo, protegendo o substrato e a flavina do solvente.
Função
A iodotirosina desiodase facilita a recuperação do iodeto na tireóide, catalisando a desiodação da mono e diiodotirosina , os subprodutos halogenados da produção do hormônio tireoidiano . O iodeto também é um micronutriente importante na biossíntese do hormônio tireoidiano, criando um ciclo de uso de iodeto na tireóide. A homeostase do iodeto na glândula tireoide é essencial para a produção do hormônio tireoidiano em taxas adequadas. Assim, os níveis de iodeto devem ser regulados para manter os hormônios tireoidianos e, em última instância, a taxa metabólica e a saúde geral do organismo em bom estado.
Dentro da célula folicular da tireoide, a tireoglobulina é hidrolisada para formar hormônios da tireoide e mono- e diiodotirosina. Os hormônios da tireoide são liberados na corrente sanguínea e as tirosinas iodadas são recicladas. No entanto, a quebra da tireoglobulina produz 6 a 7 vezes mais tirosinas iodadas do que o hormônio tireoidiano. A iodotirosina desiodinase salva o iodeto da desiodação das tirosinas iodadas. A iodotirosina desiodase está localizada na membrana plasmática apical do coloide tireoidiano, onde a mono e a diiodotirosina são produzidas a partir dessa quebra da tireoglobulina. Sem a atividade da iodotirosina desiodase, o iodeto seria excretado com o aminoácido tirosina e a biossíntese do hormônio tireoidiano seria reduzida.
A atividade enzimática da iodotirosina desiodase também é conhecida por existir nos tecidos do fígado e rins; no entanto, o significado fisiológico desses achados ainda não está claro.
Mecanismo
A iodotirosina desiodase catalisa a desiodação mono e diiodotirosina. A reação é dependente de NADPH . O mononucleotídeo de flavina (FMN) é um cofator. Embora a flavina seja comumente utilizada em várias reações catalíticas, seu uso nesta desalogenação redutiva é único e ainda não totalmente compreendido. Também não está claro se o mecanismo enzimático utiliza uma reação de transferência de dois elétrons ou uma série de transferências de um elétron. Embora mais pesquisas devam ser feitas para determinar os detalhes desse mecanismo, evidências recentes parecem sugerir que a iodotirosina deiodinase atua por meio de reações de transferência de um elétron.
Significado clínico
Mutações no gene que codifica a iodotirosina desiodinase podem afetar a função da enzima e ser prejudiciais à saúde humana. O iodeto é um micronutriente essencial para a saúde dos mamíferos. Os baixos níveis de iodeto na dieta ou no metabolismo do iodeto estão associados a hipotireoidismo , retardo mental, bócio e defeitos de desenvolvimento. Como a iodotirosina desiodinase é responsável por eliminar o iodeto, as mutações nesta enzima resultam em deficiência de iodeto.
As altas concentrações de iodotirosina no sangue e na urina resultantes podem ser usadas como uma medida para o diagnóstico, uma vez que o iodeto não é removido dos resíduos de tirosina de forma eficaz. Em alguns países, os bebês recém-nascidos são testados para hipotireoidismo congênito e tratados imediatamente se a doença for detectada, evitando com segurança o desenvolvimento de retardo mental. No entanto, as mutações da iodotirosina deiodinase muitas vezes não são detectadas até que o dano de desenvolvimento já tenha ocorrido. Além disso, essas mutações podem não ser detectadas especificamente usando testes de função tireoidiana padrão. Para combater esse problema, foi criado recentemente um ensaio sensível que mede as quantidades de mono e diiodotirosina na urina.
Veja também
Referências
Leitura adicional
- Moreno JC (2003). "Identificação de novos genes envolvidos no hipotireoidismo congênito usando análise serial da expressão gênica". Hormone Research . 60 Suplemento 3 (3): 96–102. doi : 10.1159 / 000074509 . PMID 14671405 . S2CID 11397819 .
- Afink G, Kulik W, Overmars H, de Randamie J, Veenboer T, van Cruchten A, Craen M, Ris-Stalpers C (dezembro de 2008). "Caracterização molecular da deficiência de iodotirosina deshalogenase em pacientes com hipotireoidismo" . The Journal of Clinical Endocrinology and Metabolism . 93 (12): 4894–901. doi : 10.1210 / jc.2008-0865 . PMID 18765512 .
- Gieger C, Geistlinger L, Altmaier E, Hrabé de Angelis M, Kronenberg F, Meitinger T, Mewes HW, Wichmann HE, Weinberger KM, Adamski J, Illig T, Suhre K (novembro de 2008). Gibson G (ed.). "A genética encontra a metabolômica: um estudo de associação de todo o genoma de perfis de metabólitos no soro humano" . PLOS Genetics . 4 (11): e1000282. doi : 10.1371 / journal.pgen.1000282 . PMC 2581785 . PMID 19043545 .
- Thomas SR, McTamney PM, Adler JM, Laronde-Leblanc N, Rokita SE (julho de 2009). "Estrutura de cristal da iodotirosina deiodinase, uma nova flavoproteína responsável pelo salvamento de iodeto nas glândulas tireóide" . The Journal of Biological Chemistry . 284 (29): 19659–67. doi : 10.1074 / jbc.M109.013458 . PMC 2740591 . PMID 19436071 .
- Krause K, Karger S, Gimm O, Sheu SY, Dralle H, Tannapfel A, Schmid KW, Dupuy C, Fuhrer D (março de 2007). "Caracterização da expressão de DEHAL1 em patologias da tireoide" . European Journal of Endocrinology . 156 (3): 295–301. doi : 10.1530 / EJE-06-0596 . PMID 17322488 .
- Gnidehou S, Lacroix L, Sezan A, Ohayon R, Noël-Hudson MS, Morand S, Francon J, Courtin F, Virion A, Dupuy C (agosto de 2006). "Clonagem e caracterização de uma nova isoforma de iodotirosina deshalogenase 1 (DEHAL1) DEHAL1C da tireóide humana: comparações com DEHAL1 e DEHAL1B". Tireóide . 16 (8): 715–24. doi : 10.1089 / thy.2006.16.715 . PMID 16910871 .
- Otowa T, Yoshida E, Sugaya N, Yasuda S, Nishimura Y, Inoue K, Tochigi M, Umekage T, Miyagawa T, Nishida N, Tokunaga K, Tanii H, Sasaki T, Kaiya H, Okazaki Y (fevereiro de 2009). "Estudo de associação do genoma do transtorno do pânico na população japonesa" . Journal of Human Genetics . 54 (2): 122–6. doi : 10.1038 / jhg.2008.17 . PMID 19165232 .
links externos
- Iodotirosina + Deiodinase na Biblioteca Nacional de Medicina dos EUA. Cabeçalhos de Assuntos Médicos (MeSH)
- Visão geral de todas as informações estruturais disponíveis no PDB para UniProt : Q6PHW0 (Iodotirosina deiodinase 1 humana) no PDBe-KB .
- Visão geral de todas as informações estruturais disponíveis no PDB para UniProt : Q9DCX8 (Mouse Iodotirosina deiodinase 1) no PDBe-KB .
Este artigo incorpora texto da Biblioteca Nacional de Medicina dos Estados Unidos , que é de domínio público .