Hidrogenação de ligações duplas de carbono-nitrogênio - Hydrogenation of carbon–nitrogen double bonds
Na química, a hidrogenação das ligações duplas carbono-nitrogênio é a adição dos elementos de di-hidrogênio (H 2 ) através de uma ligação dupla carbono-nitrogênio, formando aminas ou derivados de amina. Embora uma variedade de métodos gerais tenham sido desenvolvidos para a hidrogenação enantiosseletiva de cetonas, os métodos para a hidrogenação de ligações duplas carbono-nitrogênio são menos gerais. A hidrogenação de iminas é complicada por isomerização sin / anti e tautomerização em enaminas, que podem ser hidrogenadas com baixa enantiosseletividade na presença de um catalisador quiral. Além disso, o substituinte ligado ao nitrogênio afeta a reatividade e as propriedades espaciais da imina, complicando o desenvolvimento de um sistema catalisador geral para a hidrogenação da imina. Apesar desses desafios, foram desenvolvidos métodos que abordam classes de substratos particulares, como N- aril, N- alquil e iminas endocíclicas.
Se o complexo for quiral e não racêmico e o substrato for próquiral, pode ocorrer um excesso de um único enantiômero de um produto quiral.

Mecanismo e estereoquímica
O hidrogênio para a redução da ligação dupla C = N pode ser fornecido pelo gás hidrogênio (H 2 ) ou transferido de fontes de H 2 , como álcoois e ácido fórmico. O processo geralmente é catalisado por complexos de metais de transição . Para reações catalisadas por metal, a transferência de H 2 para a imina pode ocorrer por mecanismos de esfera interna ou externa.
Mecanismos de esfera interna
Relevantes para o mecanismo da esfera interna são os dois modos pelos quais as iminas podem se coordenar, como um π ou como um ligante doador σ. As pi-iminas também são suscetíveis à conversão em ligantes de imínio após N-protonação. O modo de ligação para a imina não é claro, tanto η 1 (tipo σ) quanto η 2 (tipo π). A etapa final do mecanismo é a liberação da amina. Em algumas hidrogenações catalisadas por irídio, acredita-se que o mecanismo prossiga por meio de uma espécie de monohidreto. O estado de oxidação do irídio é sempre +3. Exemplos:
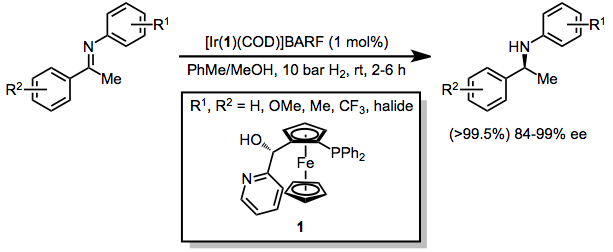

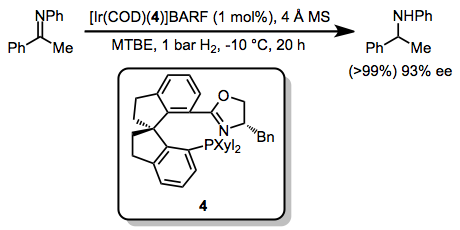
Mecanismos de esfera externa
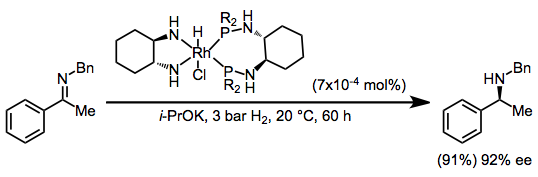
Os complexos de rutênio (II) de ligantes de amina são conhecidos por se engajarem no mecanismo da esfera externa, durante o qual o substrato imina / imínio não se liga ao centro metálico diretamente. Em vez disso, o substrato recebe os elementos de H 2 pela interação com os sítios Ru-H e NH. Este processo é utilizado pelo catalisador Shvo e muitos complexos de rutênio amina. Um desses complexos é o catalisador de Baratta RuCl 2 (PPh 3 ) 2 (ampia) (ampia = 2- picolilamina ) para hidrogenação de transferência .

Hidrogenações sem metal
Como os substituintes ligados ao nitrogênio da imina exercem uma profunda influência na reatividade, existem poucos sistemas catalisadores gerais para a hidrogenação enantiosseletiva de iminas e derivados de imina. No entanto, foram desenvolvidos sistemas de catalisador que catalisam a hidrogenação de classes particulares de iminas com alta enantiosseletividade e rendimento. Esta seção descreve alguns desses sistemas e é organizada pelo padrão de substituição da imina.
As α-carboximinas são precursores atraentes para os α-aminoácidos. A redução organocatalítica desses substratos é possível usando um éster de Hantzsch e um catalisador de ácido fosfórico quiral.

Formulários
A hidrogenação de imina fornece uma rota prática para aminas quirais. O metolacloro é o ingrediente ativo do herbicida Dual Magnum, amplamente utilizado. Uma etapa fundamental em sua produção industrial envolve a redução enantiosseletiva de uma N- aril imina. Esta redução é alcançada com um número de turnover extremamente alto (embora com enantiosseletividade moderada) através do uso de um sistema de catalisador especializado que consiste em [Ir (COD) Cl] 2 , ligante de Josiphos modificado 3 e aditivos de ácido e iodeto.
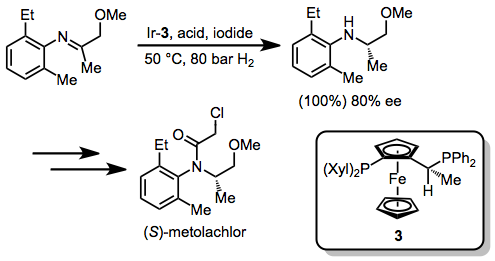
Comparação com outros métodos
As iminas podem ser reduzidas enantiosseletivamente usando quantidades estequiométricas de hidretos metálicos quirais. Esses métodos têm a vantagem de serem fáceis de implementar. A redução com hidrosilanos é uma segunda alternativa à hidrogenação catalisada por metais de transição.



