Ciclopamina - Cyclopamine
|
|
|
|
| Nomes | |
|---|---|
|
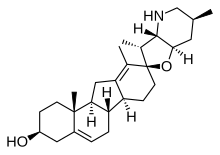
Nome IUPAC
(2 ′ R , 3 S , 3 ′ R , 3′a S , 6 ′ S , 6a S , 6b S , 7′a R , 11a S , 11b R ) -3 ′, 6 ′, 10,11b-Tetrametil -1,2,3,3′a, 4,4 ′, 5 ′, 6,6 ′, 6a, 6b, 7,7 ′, 7′a, 8,11,11a, 11b-octadecaidro-3 ′ H -espiro [benzo [ a ] fluoreno-9,2′-furo [3,2- b ] piridin] -3-ol
|
|
| Outros nomes
• 11-Deoxojervine
• (3β, 23 R ) -17,23-Epoxyveratraman-3-ol |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.156.363 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 27 H 41 N O 2 | |
| Massa molar | 411,630 g · mol −1 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
A ciclopamina (11-desoxojervina) é uma substância química natural que pertence à família dos alcalóides esteróides. É um teratógeno isolado do lírio do milho ( Veratrum californicum ) que causa defeitos congênitos fatais. Impede que o cérebro embrionário se separe em dois lobos (uma forma extrema de holoprosencefalia ), o que por sua vez causa o desenvolvimento de um único olho ( ciclopia ). O produto químico recebeu o nome desse efeito, como foi originalmente observado por criadores de cordeiros de Idaho que contataram o Departamento de Agricultura dos Estados Unidos depois que seus rebanhos deram à luz cordeiros ciclópticos em 1957. Em seguida, demorou mais de uma década para identificar o lírio-do-milho como o culpado . Trabalhos posteriores sugeriram que diferentes padrões de chuva faziam com que as ovelhas pastassem de maneira diferente, impactando a quantidade de lírio de milho ingerido por ovelhas prenhes. O veneno interrompe a via de sinalização do ouriço sônico durante o desenvolvimento, causando defeitos de nascença.
Descoberta e nomenclatura
Em 1957, criadores de ovelhas de Idaho contataram o Departamento de Agricultura dos Estados Unidos (DOA) quando suas ovelhas deram à luz cordeiros com uma deformidade ocular fatal e singular. Depois de coletar a flora local e alimentá-los com ratos, os cientistas do DOA lutaram para recriar a ciclopia . Após uma década de tentativa e erro, eles encontraram lírios de milho silvestres e aconselharam os fazendeiros a evitar os lírios de milho. A ciclopamina foi um dos três alcalóides esteróides isolados do Veratrum californicum , também conhecido como lírio do milho da Califórnia, mas o único desconhecido na época, e recebeu esse nome por causa de seus efeitos em embriões de ovelha. Quatro décadas depois, uma equipe liderada pelo professor Phillip Beachy relacionou o gene sonic hedgehog à ciclopamina. Após a experimentação, eles recriaram a ciclopia silenciando o gene sonic hedgehog. O professor Beachy então conectou seus resultados ciclópticos às ovelhas ciclópticas observadas quatro décadas antes.

Fonte e estrutura
A biossíntese da ciclopamina começa com o colesterol . Um esqueleto de esteróide tem um anel clássico de 6 membros, adjacente a outro 6, 6 e, em seguida, um cinco ou “6-6-6-5”. Veratrum foi determinado para conter cinco tipos de alcalóides, cada um dos quais tinha um precursor de colesterol comum: (1) alcalóides de solanidina , (2) alcalóides de verazina, (3) alcalóides de vertramina , (4) alcalóides de jervina , e (5) os alcalóides de cevanina . Na biossíntese, a ciclopamina tem um precursor de solanida (1), que por sua vez é feito de colesterol. Isso foi determinado por estudos iniciais que isolaram alcalóides do lírio do milho ( Veratrum californium) e os introduziram em ovelhas embrionárias. Na época, a jervina era um alcalóide já conhecido, isolado do lírio do milho ao lado de dois outros alcalóides: a desconhecida ciclopamina e a veratramina; cada um com diferentes toxicidades. Estudos posteriores demonstraram que a jervina se degradou em ciclopamina após uma redução de Wolff-Kishner , que ajudou a identificar o composto desconhecido.
Também foi demonstrado que o tratamento da ciclopamina com ácido de Lewis (pH <2) leva à produção de veratramina . O estômago fornece essas condições e, portanto, apenas uma pequena quantidade de ciclopamina passa pelo estômago após a ingestão. E embora apenas uma pequena quantidade da ciclopamina ingerida passe pelo estômago, ela permanece inalterada depois.
A veratramina é altamente tóxica, mesmo que não afete o desenvolvimento, pois excita o sistema nervoso central e pode causar convulsões - semelhante à serotonina . O mecanismo de produção da veratramina se concentra na clivagem de uma ligação carbono-oxigênio, que leva à formação de uma nova ligação dupla. A partir daí, este anel é quase aromático . A força motriz para se tornar aromática então empurra uma reação de eliminação, criando uma terceira ligação dupla e produzindo aromaticidade , conforme ilustrado na figura abaixo.

Mecanismo
A ciclopamina afeta o desenvolvimento embrionário ao impedir a via do ouriço sônico (Shh).
No desenvolvimento saudável, o gene Shh codifica as proteínas Shh. Essas proteínas têm alta afinidade por uma proteína de membrana de superfície chamada “ Patched ”. Após a ligação, as proteínas Shh inibem Patched. Com o Patch inibido, outra proteína de membrana de superfície chamada “ Smoothened ” pode sinalizar outras cascatas que afetam o desenvolvimento.
A ciclopamina tem alta afinidade para Smoothened - e ao se ligar, inibe o sinal. Embora Shh possa inibir Patched, Smoothened não pode sinalizar na presença de Ciclopamina e, portanto, a via é interrompida.
Embriológico
A ciclopamina causa a forma mais avançada de holoprosencefalia . Por bloquear a sinalização de Shh, o cérebro embrionário não mais se divide em lobos (torna-se alobar). Assim, apenas uma trilha ótica se desenvolve, daí o olho ciclóptico (singular). Além disso, esta doença é fatal e atualmente não tem cura.
Pode-se imaginar uma metade do cérebro saudável não se dividindo, mas crescendo e se assemelhando ao cérebro alobar. Isso ocorre em casos de envenenamento por ciclopamina. Essa malformação é sempre fatal, sendo importante ressaltar que há casos menores de holoprosencefalia e nem sempre fatais. No entanto, o envenenamento por ciclopamina embrionária causa os casos mais extremos e, portanto, fatais.
Potencial médico
A ciclopamina está sendo investigada atualmente como agente de tratamento no carcinoma basocelular , meduloblastoma e rabdomiossarcoma , tumores que comumente resultam da atividade SHh excessiva, glioblastoma e como agente de tratamento para mieloma múltiplo . Por exemplo, estudos de cânceres epiteliais demonstraram que as células tumorais secretam ligante Shh para sinalizar a produção de fatores de crescimento adjacentes pelas células do estroma, o que leva à angiogênese , proliferação de células tumorais e sobrevivência das células tumorais.
Com isso em mente, pode-se imaginar a ciclopamina como uma forma de atenuar o mecanismo do câncer. No entanto, embora a ciclopamina tenha demonstrado inibir o crescimento do tumor em modelos de xenoenxerto de camundongo, ela nunca atingiu potencial terapêutico, pois causou muitos efeitos colaterais, incluindo perda de peso, desidratação e morte em modelos de camundongo.
Dito isso, dois análogos funcionais da ciclopamina foram aprovados pelo FDA; vismodegib em 2012 e sonidegib em 2015. Além disso, vismodegib foi o primeiro medicamento da via Shh aprovado para o tratamento do câncer.
Embora a ciclopamina e o vismodegibe não pareçam muito semelhantes, o desenvolvimento do vismodegibe revelou quais aspectos da ciclopamina lhe conferem funcionalidade e usou esses resultados para fazer o vismodegibe. Por exemplo, o grupo de cloro adicionado no Vismodegib dá ao fármaco uma solubilidade muito maior do que a ciclopamina - a baixa solubilidade é um obstáculo para tornar a ciclopamina um fármaco prático. O desenvolvimento do vismodegib revelou relações de atividade de estrutura (SAR) e determinou que as ligações de hidrogênio em dois locais, assim como a solubilidade, impactam a eficácia do medicamento. Especificamente falando, as duas ligações de hidrogênio funcionam de maneiras opostas; em um local, um resíduo de tirosina no receptor Smoothened oferece um próton a ser aceito, enquanto um resíduo de arginina separado funciona como um aceitador de ligação de hidrogênio. Embora o grupo de aceitação seja mais impactante, ter os dois torna o vínculo mais forte.

Veja também
- Saridegib (também conhecido como IPI-926), um análogo semissintético da ciclopamina
- Vismodegib , um inibidor de sinalização Hh artificial
- Sonidegib , um inibidor de sinalização Hh artificial
- Alcalóide esteróide , a família de moléculas da ciclopamina se enquadra em
Referências
Leitura adicional
- Alam MM, Sohoni S, Kalainayakan SP, Garrossian M, Zhang L (fevereiro de 2016). "O tartarato de ciclopamina, um inibidor da sinalização Hedgehog, interfere fortemente com a função mitocondrial e suprime a respiração aeróbia nas células do câncer de pulmão" . BMC Cancer . 16 (1): 150. doi : 10.1186 / s12885-016-2200-x . PMC 4766751 . PMID 26911235 .
- Droga contra o câncer por trás do nascimento de um ciclope? , Wired News
- Bar EE, Chaudhry A, Lin A, Fan X, Schreck K, Matsui W, Piccirillo S, Vescovi AL, DiMeco F, Olivi A, Eberhart CG (outubro de 2007). "A inibição da via de hedgehog mediada por ciclopamina esgota as células cancerosas semelhantes a tronco no glioblastoma" . Células-tronco . 25 (10): 2524–33. doi : 10.1634 / stemcells.2007-0166 . PMC 2610257 . PMID 17628016 . Resumo de leigos - ScienceDaily (31 de agosto de 2007).
- Tabs S, Avci O (2004). “Indução da diferenciação e apoptose de células tumorais in vivo com eficiência e seletividade” . European Journal of Dermatology . 14 (2): 96–102. PMID 15196999 .
- Taş S, Avci O (2004). Rápida depuração de lesões cutâneas psoriáticas induzidas por ciclopamina tópica. Uma prova preliminar de estudo de conceito ". Dermatologia . 209 (2): 126–31. doi : 10.1159 / 000079596 . PMID 15316166 . S2CID 28753644 .
- Zhang J, Garrossian M, Gardner D, Garrossian A, Chang YT, Kim YK, Chang CW (fevereiro de 2008). "Estudos de síntese e atividade anticâncer de derivados de ciclopamina". Bioorganic & Medicinal Chemistry Letters . 18 (4): 1359–63. doi : 10.1016 / j.bmcl.2008.01.017 . PMID 18221872 .
- Fan Q, Gu D, He M, Liu H, Sheng T, Xie G, Li CX, Zhang X, Wainwright B, Garrossian A, Garrossian M, Gardner D, Xie J (julho de 2011). "Redução do tumor pelo tartarato de ciclopamina através da inibição da sinalização de hedgehog" . Jornal Chinês do Câncer . 30 (7): 472–81. doi : 10.5732 / cjc.011.10157 . PMC 4013422 . PMID 21718593 .

