Iodeto de cádmio - Cadmium iodide

|
|
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Iodeto de cádmio (II)
|
|
| Outros nomes
Diiodeto de cádmio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.029.294 |
| Número EC | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CdI 2 | |
| Massa molar | 366,22 g / mol |
| Aparência | cristais brancos a amarelos pálidos |
| Densidade | 5,640 g / cm 3 , sólido |
| Ponto de fusão | 387 ° C (729 ° F; 660 K) |
| Ponto de ebulição | 742 ° C (1.368 ° F; 1.015 K) |
| 787 g / L (0 ° C) 847 g / L (20 ° C) 1250 g / L (100 ° C) |
|
| Solubilidade | solúvel em etanol , acetona , éter e amônia |
| -117,2 · 10 −6 cm 3 / mol | |
| Estrutura | |
| Trigonal , hP3 , grupo espacial P 3 m1, No. 164 | |
| octaédrico | |
| Perigos | |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H301 , H331 , H351 , H373 , H400 , H410 | |
| P260 , P280 , P301 + 330 + 331 , P310 , P304 + 340 , P311 , P403 + 233 | |
| NFPA 704 (diamante de fogo) | |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
[1910,1027] TWA 0,005 mg / m 3 (como Cd) |
|
REL (recomendado)
|
Ca |
|
IDLH (perigo imediato)
|
Ca [9 mg / m 3 (como Cd)] |
| Compostos relacionados | |
|
Outros ânions
|
fluoreto de cádmio cloreto de cádmio brometo de cádmio |
|
Outros cátions
|
iodeto de zinco mercúrio (II) iodeto |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O iodeto de cádmio é o composto inorgânico com a fórmula CdI 2 . É um sólido higroscópico branco. Também pode ser obtido como mono- e tetra-hidrato. Possui poucos aplicativos. É notável por sua estrutura cristalina , típica de compostos da forma MX 2 com fortes efeitos de polarização .
Preparação
O iodeto de cádmio é preparado pela adição de cádmio metálico, ou seu óxido, hidróxido ou carbonato ao ácido iodídrico . Além disso, o composto pode ser feito aquecendo o cádmio com iodo.
Estrutura de cristal
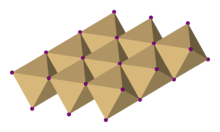
No iodeto de cádmio, os ânions de iodeto formam um arranjo hexagonal compactado, enquanto os cátions de cádmio preenchem todos os sítios octaédricos em camadas alternadas. A estrutura resultante consiste em uma estrutura em camadas. Essa mesma estrutura básica é encontrada em muitos outros sais e minerais . O iodeto de cádmio é principalmente ionicamente ligado, mas com caráter covalente parcial .
A estrutura cristalina do iodeto de cádmio é o protótipo no qual as estruturas cristalinas de muitos outros compostos podem ser consideradas baseadas. Os compostos com qualquer uma das seguintes características tendem a adotar a estrutura CdI 2 :
- Iodetos de cátions moderadamente polarizadores ; brometos e cloretos de cátions fortemente polarizadores
- Hidróxidos de medicações, ou seja, compostos com a fórmula geral M (OH) 2
- Sulfetos , selenetos e teluretos ( calcogenetos ) de tetracações, ou seja, compostos com a fórmula geral MX 2 , onde X = S, Se, Te


