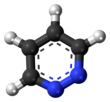
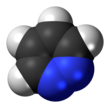
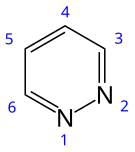
Piridazina - Pyridazine
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Piridazina |
|||
|
Nome IUPAC sistemático
1,2-diazabenzeno |
|||
| Outros nomes
1,2-diazina
ortodiazina oizina |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,005,478 |
||
| Número EC | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 4 H 4 N 2 | |||
| Massa molar | 80,090 g · mol −1 | ||
| Aparência | Líquido incolor | ||
| Densidade | 1,107 g / cm 3 | ||
| Ponto de fusão | -8 ° C (18 ° F; 265 K) | ||
| Ponto de ebulição | 208 ° C (406 ° F; 481 K) | ||
| miscível | |||
| Solubilidade | miscível em dioxano , etanol solúvel em benzeno , éter dietílico insignificante em ciclohexano , ligroína |
||
|
Índice de refração ( n D )
|
1,52311 (23,5 ° C) | ||
| Termoquímica | |||
| 224,9 kJ / mol | |||
| Perigos | |||
| Ponto de inflamação | 85 ° C (185 ° F; 358 K) | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
piridina , pirimidina , pirazina | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Piridazina é um heterocíclico composto orgânico com a fórmula molecular (CH) 4 N 2 . Ele contém um anel de seis membros com dois átomos de nitrogênio adjacentes e é aromático. É um líquido incolor com ponto de ebulição de 208 ° C. É isomérico com dois outros anéis (CH) 4 N 2 , pirimidina e pirazina .
Ocorrência
As piridazinas são raras na natureza, possivelmente refletindo a escassez de hidrazinas de ocorrência natural , blocos de construção comuns para a síntese desses heterociclos. A estrutura piridazina é um popular farmacóforo que se encontra dentro de uma série de herbicidas, tais como credazine , piridafol e piridato . Também é encontrada na estrutura de vários medicamentos, como cefozopran , cadralazina , minaprina , pipofezina e hidralazina .
Síntese
No curso de sua investigação clássica sobre a síntese de indol de Fischer , Emil Fischer preparou a primeira piridazina por meio da condensação de fenil - hidrazina e ácido levulínico . O heterociclo original foi primeiro preparado por oxidação de benzocinolina em ácido piridazinotetracarboxílico seguido por descarboxilação . Uma rota melhor para esse composto esotérico começa com a hidrazida maleica . Esses heterociclos são frequentemente preparados por condensação de 1,4- dicetonas ou 4-cetoácidos com hidrazinas .
Referências
- ^ "Matéria frontal". Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book) . Cambridge: The Royal Society of Chemistry . 2014. p. 141. doi : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ Gumus, S. (2011). "Um estudo computacional sobre diazabenzenos substituídos" (PDF) . Turk J Chem . 35 : 803–808. Arquivado do original (PDF) em 03/03/2016 . Página visitada em 2014-04-10 .
- ^ Fischer, E. (1886). "Indole aus Phenylhydrazin" . Justus Liebigs Annalen der Chemie . 236 (1–2): 126–151. doi : 10.1002 / jlac.18862360107 .
- ^ Tišler, M .; Stanovnik, B. (1968). "Pyridazines". Advances in Heterocyclic Chemistry . 9 : 211–320. doi : 10.1016 / S0065-2725 (08) 60374-8 . ISBN 9780120206094.