Neuropsicofarmacologia - Neuropsychopharmacology
Neuropsicofarmacologia , uma ciência interdisciplinar relacionada à psicofarmacologia (como as drogas afetam a mente) e neurociência fundamental , é o estudo dos mecanismos neurais sobre os quais as drogas atuam para influenciar o comportamento. Envolve a pesquisa de mecanismos de neuropatologia , farmacodinâmica (ação de drogas) , doenças psiquiátricas e estados de consciência . Esses estudos são instigados em nível detalhado envolvendo neurotransmissão / atividade do receptor , processos bioquímicos e circuitos neurais . A neuropsicofarmacologia substitui a psicofarmacologia nas áreas de "como" e "por quê" e, adicionalmente, aborda outras questões da função cerebral. Consequentemente, o aspecto clínico do campo inclui tratamentos baseados em farmacologia psiquiátrica (psicoativa), bem como neurológica (não psicoativa). Os desenvolvimentos em neuropsicofarmacologia podem impactar diretamente os estudos de transtornos de ansiedade , transtornos afetivos , transtornos psicóticos , transtornos degenerativos , comportamento alimentar e comportamento do sono .
História
Drogas como ópio , álcool e certas plantas têm sido usadas por milênios por humanos para aliviar o sofrimento ou mudar a consciência, mas até a era científica moderna, o conhecimento de como as substâncias realmente funcionavam era bastante limitado, a maioria dos conhecimentos farmacológicos sendo mais uma série de observações do que um modelo coerente. A primeira metade do século 20 viu a psicologia e a psiquiatria como amplamente fenomenológicas , em que os comportamentos ou temas que foram observados em pacientes podiam frequentemente ser correlacionados a uma variedade limitada de fatores, como experiência na infância, tendências hereditárias ou lesão em áreas cerebrais específicas. Modelos de função e disfunção mental foram baseados em tais observações. Na verdade, o ramo comportamental da psicologia dispensou completamente o que realmente acontecia dentro do cérebro, considerando a maioria das disfunções mentais como o que poderia ser apelidado de erros de "software". Na mesma época, o sistema nervoso estava sendo estudado progressivamente no nível microscópico e químico, mas não havia virtualmente nenhum benefício mútuo com os campos clínicos - até que vários desenvolvimentos após a Segunda Guerra Mundial começaram a uni-los. A neuropsicofarmacologia pode ser considerada como tendo começado no início dos anos 1950 com a descoberta de drogas como inibidores da MAO , antidepressivos tricíclicos , torazina e lítio, que mostraram alguma especificidade clínica para doenças mentais como depressão e esquizofrenia. Até então, os tratamentos que realmente visavam essas doenças complexas eram praticamente inexistentes. Os métodos proeminentes que podiam afetar diretamente os circuitos cerebrais e os níveis de neurotransmissores eram a lobotomia pré-frontal e a terapia eletroconvulsiva , a última das quais conduzida sem relaxantes musculares e ambas frequentemente causavam ao paciente grandes danos físicos e psicológicos.
O campo agora conhecido como neuropsicofarmacologia resultou do crescimento e extensão de muitos campos anteriormente isolados que se encontraram no cerne da medicina psiquiátrica e envolve uma ampla gama de profissionais de psiquiatras a pesquisadores em genética e química. O uso do termo ganhou popularidade desde 1990 com a fundação de vários periódicos e instituições, como o Hungarian College of Neuropsychopharmacology . Este campo de rápido amadurecimento mostra algum grau de fluxo, já que as hipóteses de pesquisa são frequentemente reestruturadas com base em novas informações.
Visão geral
Uma premissa implícita em neuropsicofarmacologia no que diz respeito aos aspectos psicológicos é que todos os estados mentais , incluindo os estados alterados normais e induzidos por drogas, e doenças envolvendo disfunção mental ou cognitiva , têm uma base neuroquímica no nível fundamental e certas vias de circuito em o sistema nervoso central em um nível superior. (Veja também: Doutrina do neurônio ) Portanto, a compreensão das células nervosas ou neurônios do cérebro é fundamental para a compreensão da mente. É argumentado que os mecanismos envolvidos podem ser elucidados por meio de métodos clínicos e de pesquisa modernos , como manipulação genética em animais, técnicas de imagem como imagem por ressonância magnética funcional ( fMRI ) e estudos in vitro usando agentes de ligação seletiva em culturas de tecidos vivos. Isso permite que a atividade neural seja monitorada e medida em resposta a uma variedade de condições de teste. Outras ferramentas observacionais importantes incluem imagens radiológicas , como tomografia por emissão de pósitrons ( PET ) e tomografia computadorizada por emissão de fóton único ( SPECT ). Essas técnicas de imagem são extremamente sensíveis e podem gerar imagens de concentrações moleculares minúsculas da ordem de 10-10 M, como as encontradas com o receptor D 1 extrastriatal para dopamina.
Um dos objetivos finais é conceber e desenvolver prescrições de tratamento para uma variedade de condições neuropatológicas e distúrbios psiquiátricos . Mais profundamente, porém, o conhecimento adquirido pode fornecer insights sobre a própria natureza do pensamento humano, habilidades mentais como aprendizado e memória, e talvez a própria consciência. Um produto direto da pesquisa neuropsicofarmacológica é a base de conhecimento necessária para desenvolver drogas que atuam em receptores muito específicos dentro de um sistema neurotransmissor. Essas drogas de "ação hiperseletiva" permitiriam o direcionamento direto de locais específicos de atividade neural relevante, maximizando assim a eficácia (ou tecnicamente a potência ) da droga dentro do alvo clínico e minimizando os efeitos adversos . No entanto, existem alguns casos em que algum grau de promiscuidade farmacológica é tolerável e até desejável, produzindo resultados mais desejáveis do que um agente mais seletivo produziria. Um exemplo disso é a Vortioxetina , uma droga que não é particularmente seletiva como um inibidor da recaptação da serotonina, tendo um grau significativo de atividade modulatória da serotonina, mas que demonstrou sintomas de descontinuação reduzidos (e probabilidade reduzida de recaída ) e incidência muito reduzida de disfunção sexual , sem perda da eficácia antidepressiva.
A base está sendo pavimentada para a próxima geração de tratamentos farmacológicos , que irão melhorar a qualidade de vida com eficiência crescente. Por exemplo, ao contrário do que se pensava, agora se sabe que o cérebro adulto, em certa medida, desenvolve novos neurônios - o estudo dos quais, além de fatores neurotróficos , pode conter esperança para doenças neurodegenerativas como Alzheimer , Parkinson , ALS e tipos de coréia . Todas as proteínas envolvidas na neurotransmissão são uma pequena fração das mais de 100.000 proteínas no cérebro. Assim, existem muitas proteínas que nem mesmo estão no caminho direto da transdução de sinal , qualquer uma das quais ainda pode ser um alvo para terapia específica. Atualmente, novas abordagens farmacológicas para doenças ou condições são relatadas a uma taxa de quase uma por semana.
Neurotransmissão
Até onde sabemos, tudo o que percebemos, sentimos, pensamos, sabemos e fazemos é resultado de neurônios disparando e reiniciando. Quando uma célula do cérebro dispara, pequenas oscilações químicas e elétricas chamadas de potencial de ação podem afetar o disparo de até mil outros neurônios em um processo chamado neurotransmissão . Dessa forma, os sinais são gerados e transportados por redes de neurônios, cujo efeito elétrico em massa pode ser medido diretamente no couro cabeludo por um dispositivo de EEG .
Na última década do século 20, o conhecimento essencial de todas as características centrais da neurotransmissão foi adquirido. Esses recursos são:
- A síntese e armazenamento de substâncias neurotransmissoras ,
- O transporte de vesículas sinápticas e subsequente liberação na sinapse ,
- Ativação do receptor e função em cascata ,
- Mecanismos de transporte (recaptação) e / ou degradação enzimática
Os avanços mais recentes envolvem a compreensão no nível molecular orgânico ; ação bioquímica dos ligantes endógenos , enzimas , proteínas receptoras , etc. As mudanças críticas que afetam o disparo das células ocorrem quando os neurotransmissores de sinalização de um neurônio, agindo como ligantes, se ligam aos receptores de outro neurônio. Muitos sistemas neurotransmissores e receptores são bem conhecidos, e a pesquisa continua em direção à identificação e caracterização de um grande número de subtipos de receptores muito específicos. Para os seis neurotransmissores mais importantes Glu , GABA , Ach , NE , DA e 5HT (listados no neurotransmissor ), existem pelo menos 29 subtipos principais de receptor. Outros "sub-subtipos" existem junto com variantes, totalizando centenas apenas para esses 6 transmissores. - (ver receptor de serotonina, por exemplo.) Frequentemente, verifica-se que os subtipos de receptores têm funções diferenciadas, o que, em princípio, abre a possibilidade de um controle intencional refinado sobre a função cerebral.
Foi anteriormente conhecido que o controle final sobre a tensão da membrana ou potencial de uma célula nervosa e, portanto, o disparo da célula, reside nos canais de íons transmembrana que controlam as correntes de membrana através dos íons K + , Na + e Ca + + , e de menor importância Mg ++ e Cl - . As diferenças de concentração entre o interior e o exterior da célula determinam a voltagem da membrana.
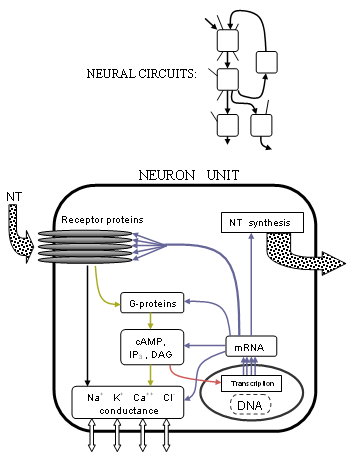
Precisamente como essas correntes são controladas, tornou-se muito mais claro com os avanços na estrutura do receptor e nos processos acoplados à proteína G. Descobriu-se que muitos receptores são agrupamentos pentaméricos de cinco proteínas transmembrana (não necessariamente as mesmas) ou subunidades de receptor , cada uma delas uma cadeia de muitos aminoácidos. Os transmissores normalmente se ligam na junção entre duas dessas proteínas, nas partes que se projetam da membrana celular. Se o receptor for do tipo ionotrópico , um poro ou canal central no meio das proteínas será movido mecanicamente para permitir que certos íons fluam, alterando assim a diferença de concentração de íons. Se o receptor for do tipo metabotrópico , as proteínas G causarão metabolismo dentro da célula que pode eventualmente alterar outros canais iônicos. Os pesquisadores estão entendendo melhor exatamente como essas mudanças ocorrem com base nas formas da estrutura da proteína e nas propriedades químicas.
O escopo dessa atividade foi ampliado ainda mais para o próprio projeto da vida, desde o esclarecimento do mecanismo subjacente à transcrição do gene . A síntese de proteínas celulares a partir do DNA nuclear tem o mesmo mecanismo fundamental para todas as células; cuja exploração agora tem uma base sólida graças ao Projeto Genoma Humano, que enumerou toda a sequência de DNA humano, embora muitos dos cerca de 35.000 genes ainda não tenham sido identificados. O processo de neurotransmissão completo se estende ao nível genético. A expressão do gene determina as estruturas das proteínas por meio da RNA polimerase do tipo II . Assim, as enzimas que sintetizam ou quebram neurotransmissores, receptores e canais iônicos são, cada uma, feitas de mRNA por meio da transcrição de DNA de seus respectivos genes ou genes. Mas a neurotransmissão, além de controlar os canais iônicos diretamente ou de outra forma por meio de processos metabotrópicos , também modula a expressão gênica. Isso é alcançado de forma mais proeminente por meio da modificação do processo de iniciação da transcrição por uma variedade de fatores de transcrição produzidos a partir da atividade do receptor.
Além das importantes possibilidades farmacológicas das vias de expressão gênica, a correspondência de um gene com sua proteína permite a importante ferramenta analítica de nocaute gênico . Espécimes vivos podem ser criados usando recombinação homóloga na qual um gene específico não pode ser expresso. O organismo será então deficiente na proteína associada, que pode ser um receptor específico. Este método evita o bloqueio químico que pode produzir efeitos secundários confusos ou ambíguos, de modo que os efeitos da falta de receptor podem ser estudados em um sentido mais puro.
Drogas
O início de muitas classes de drogas é, em princípio, simples: qualquer produto químico que possa aumentar ou diminuir a ação de uma proteína-alvo pode ser investigado posteriormente para tal uso. O truque é encontrar um produto químico específico para o receptor (cf. " droga suja ") e seguro para consumir. The 2005 Physicians 'Desk Reference lista duas vezes o número de medicamentos prescritos que a versão de 1990. Muitas pessoas agora estão familiarizadas com " inibidores seletivos da recaptação da serotonina ", ou SSRIs que exemplificam os produtos farmacêuticos modernos . Esses antidepressivos SSRI , como Paxil e Prozac, seletivamente e, portanto, inibem principalmente o transporte de serotonina, que prolonga a atividade na sinapse. Existem inúmeras categorias de drogas seletivas, e o bloqueio do transporte é apenas um modo de ação. O FDA aprovou drogas que atuam seletivamente em cada um dos principais neurotransmissores, como antidepressivos inibidores de recaptação de NE , antipsicóticos bloqueadores de DA e tranquilizantes agonistas GABA ( benzodiazepínicos ).
Novos produtos químicos endógenos são continuamente identificados. Receptores específicos foram encontrados para as drogas THC (cannabis) e GHB , com transmissores endógenos anandamida e GHB. Outra grande descoberta recente ocorreu em 1999, quando se descobriu que a orexina , ou hipocretina, desempenha um papel na excitação, uma vez que a falta de receptores de orexina reflete a condição de narcolepsia . O agonismo de Orexin pode explicar a ação antinarcoléptica do medicamento modafinil, que já era usado apenas um ano antes.
A próxima etapa, que as principais empresas farmacêuticas estão trabalhando arduamente para desenvolver, são os medicamentos específicos para o subtipo de receptor e outros agentes específicos. Um exemplo é a busca por melhores agentes ansiolíticos ( ansiolíticos ) baseados em agonistas GABA A (α2), antagonistas de CRF 1 e antagonistas de 5HT 2c . Outra é a proposta de novas rotas de exploração de antipsicóticos como os inibidores da recaptação da glicina . Embora existam recursos para drogas específicas do receptor, uma deficiência da terapia com drogas é a falta de capacidade de fornecer especificidade anatômica . Ao alterar a função do receptor em uma parte do cérebro, a atividade anormal pode ser induzida em outras partes do cérebro devido ao mesmo tipo de mudanças no receptor. Um exemplo comum é o efeito de drogas alteradoras de D 2 (neurolépticos) que podem ajudar a esquizofrenia, mas causam uma variedade de discinesias por sua ação no córtex motor.
Estudos modernos estão revelando detalhes de mecanismos de danos ao sistema nervoso, como apoptose (morte celular programada) e ruptura por radicais livres . A fenciclidina foi encontrada para causar morte celular em células estriatopalidais e vacuolização anormal no hipocampo e outros neurônios. O distúrbio de percepção persistente de alucinógeno (HPPD), também conhecido como distúrbio de percepção pós-psicodélico , foi observado em pacientes até 26 anos após o uso de LSD. A causa plausível do HPPD é o dano ao circuito inibitório do GABA na via visual (agonistas do GABA, como o midazolam, podem diminuir alguns efeitos da intoxicação por LSD). O dano pode ser o resultado de uma resposta excitotóxica de interneurônios 5HT 2 . [Nota: a grande maioria dos usuários de LSD não experimenta HPPD. Sua manifestação pode ser igualmente dependente da química cerebral individual e do próprio uso de drogas.] Quanto ao MDMA , além das perdas persistentes de 5HT e SERT , a redução duradoura dos axônios e terminais serotonérgicos é encontrada com o uso de curto prazo e rebrota pode ter função comprometida.
Circuitos neurais
Não é uma descoberta tão recente que muitas funções do cérebro estejam um tanto localizadas em áreas associadas, como habilidades motoras e de fala. As associações funcionais da anatomia do cérebro estão agora sendo complementadas com correlatos clínicos, comportamentais e genéticos da ação do receptor, completando o conhecimento da sinalização neural (ver também: Projeto Cognoma Humano ) . As vias de sinal dos neurônios são hiperorganizadas além da escala celular em vias de circuitos neurais frequentemente complexos. O conhecimento dessas vias é talvez o mais fácil de interpretar, sendo mais reconhecível do ponto de vista da análise de sistemas, como pode ser visto nos resumos a seguir.
Quase todas as drogas com potencial conhecido de abuso modulam a atividade (direta ou indiretamente) no sistema dopaminérgico mesolímbico, que inclui e conecta a área tegmental ventral no mesencéfalo ao hipocampo, córtex pré-frontal medial e amígdala no prosencéfalo ; bem como o núcleo accumbens no estriado ventral dos gânglios da base. Em particular, o nucleus accumbens (NAc) desempenha um papel importante na integração da memória experiencial do hipocampo, emoção da amígdala e informação contextual do PFC para ajudar a associar estímulos ou comportamentos específicos com sentimentos de prazer e recompensa; a ativação contínua desse sistema indicador de recompensa por uma droga aditiva também pode fazer com que estímulos anteriormente neutros sejam codificados como pistas de que o cérebro está prestes a receber uma recompensa. Isso acontece por meio da liberação seletiva de dopamina, um neurotransmissor responsável por sensações de euforia e prazer. O uso de drogas dopaminérgicas altera a quantidade de dopamina liberada por todo o sistema mesolímbico, e o uso regular ou excessivo da droga pode resultar em uma regulação negativa de longo prazo da sinalização da dopamina, mesmo após o indivíduo parar de ingerir a droga. Isso pode levar o indivíduo a se envolver em comportamentos de busca de drogas leves a extremos, pois o cérebro começa a esperar regularmente o aumento da presença de dopamina e os sentimentos de euforia que os acompanham, mas o quão problemático isso é depende muito da droga e da situação.
Progresso significativo foi feito nos mecanismos centrais de certas drogas alucinógenas . A essa altura, sabe-se com relativa certeza que os efeitos compartilhados primários de um amplo grupo farmacológico de alucinógenos, às vezes chamados de "psicodélicos clássicos", podem ser atribuídos em grande parte ao agonismo dos receptores de serotonina. O receptor 5HT 2A , que parece ser o receptor mais crítico para a atividade psicodélica, e o receptor 5HT 2C , que é um alvo significativo da maioria dos psicodélicos, mas que não tem um papel claro na alucinogênese, estão envolvidos na liberação de glutamato no córtex frontal , enquanto, simultaneamente, no locus coeruleus, a informação sensorial é promovida e a atividade espontânea diminui. A atividade 5HT 2A tem um efeito pró-dopaminérgico líquido, enquanto o agonismo do receptor 5HT 2C tem um efeito inibitório na atividade dopaminérgica, particularmente no córtex pré-frontal. Uma hipótese sugere que, no córtex frontal, o 5HT 2A promove potenciais pós-sinápticos excitatórios assíncronos tardios , um processo antagonizado pela própria serotonina por meio dos receptores 5HT 1 , o que pode explicar por que os ISRSs e outras drogas que afetam a serotonina normalmente não causam alucinações no paciente. No entanto, o fato de muitos psicodélicos clássicos de fato terem afinidade significativa para os receptores 5HT 1 coloca essa afirmação em questão. A resposta de contração muscular da cabeça, um teste usado para avaliar a atividade psicodélica clássica em roedores, é produzida pela própria serotonina apenas na presença de beta-arrestinas, mas é desencadeada por psicodélicos clássicos independentes do recrutamento de beta-arrestinas. Isso pode explicar melhor a diferença entre a farmacologia da neurotransmissão serotonérgica (mesmo se promovida por drogas como os ISRSs) e a dos psicodélicos clássicos. No entanto, descobertas mais recentes indicam que a ligação ao heterodímero 5HT 2A - mGlu2 também é necessária para a atividade psicodélica clássica. Isso também pode ser relevante para as diferenças farmacológicas entre os dois. Embora no início da história da pesquisa de drogas psicodélicas se presumisse que essas alucinações eram comparáveis às produzidas pela psicose e, portanto, que os psicodélicos clássicos poderiam servir como um modelo de psicose, é importante notar que o conhecimento neuropsicofarmacológico moderno da psicose progrediu significativamente desde então, e agora sabemos que a psicose mostra pouca semelhança com os efeitos dos psicodélicos clássicos no mecanismo, na experiência relatada ou na maioria dos outros aspectos além da semelhança superficial de "alucinação".
O ritmo circadiano , ou ciclo sono / vigília, está centrado no núcleo supraquiasmático (SCN) dentro do hipotálamo e é marcado por níveis de melatonina 2.000 a 4.000% mais elevados durante o sono do que durante o dia. Um circuito é conhecido por começar com células de melanopsina no olho que estimulam o SCN por meio de neurônios glutamato do trato hipotalâmico . Os neurônios gabaérgicos do SCN inibem o núcleo paraventricular , que sinaliza o gânglio cervical superior (SCG) por meio de fibras simpáticas . A saída do SCG, estimula os receptores NE ( β ) na glândula pineal que produz N-acetiltransferase, causando a produção de melatonina a partir da serotonina. Os receptores de melatonina inibitórios no SCN fornecem uma via de feedback positivo . Portanto, a luz inibe a produção de melatonina, que " arrasta " o ciclo de 24 horas da atividade do SCN. O SCN também recebe sinais de outras partes do cérebro, e seu ciclo (aproximadamente) de 24 horas não depende apenas de padrões de luz. Na verdade, o tecido seccionado do SCN exibirá um ciclo diário in vitro por muitos dias. Além disso, (não mostrado no diagrama), o núcleo basal fornece entrada inibitória GABA-ergic para o hipotálamo anterior pré-óptico (PAH). Quando a adenosina se acumula a partir do metabolismo do ATP ao longo do dia, ela se liga aos receptores de adenosina, inibindo o núcleo basal. O PAH é então ativado, gerando atividade de sono de ondas lentas. A cafeína é conhecida por bloquear os receptores de adenosina, inibindo assim o sono, entre outras coisas.
Pesquisar
A pesquisa no campo da neuropsicofarmacologia abrange uma ampla gama de objetivos. Isso pode incluir o estudo de um novo composto químico para efeitos cognitivos ou comportamentais potencialmente benéficos, ou o estudo de um composto químico antigo para compreender melhor seu mecanismo de ação nos níveis da célula e do circuito neural. Por exemplo, há muito se sabe que a droga estimulante viciante cocaína age sobre o sistema de recompensa no cérebro, aumentando os níveis de dopamina e norepinefrina e induzindo euforia por um curto período de tempo. Estudos publicados mais recentemente, no entanto, foram além do nível do circuito e descobriram que um complexo receptor acoplado à proteína G particular, denominado A2AR-D2R-Sigma1R, é formado no NAc após o uso de cocaína; este complexo reduz a sinalização D2R na via mesolímbica e pode ser um fator contribuinte para o vício em cocaína. Outros estudos de ponta se concentraram na genética para identificar biomarcadores específicos que podem prever as reações específicas de um indivíduo ou o grau de resposta a uma droga ou sua tendência de desenvolver vícios no futuro. Essas descobertas são importantes porque fornecem uma visão detalhada dos circuitos neurais envolvidos no uso de drogas e ajudam a refinar antigos, bem como desenvolver novos métodos de tratamento para distúrbios ou vícios. Diferentes estudos relacionados ao tratamento estão investigando o papel potencial dos ácidos nucleicos peptídicos no tratamento da doença de Parkinson e esquizofrenia, enquanto outros ainda estão tentando estabelecer correlações neurais anteriormente desconhecidas subjacentes a certos fenômenos.
A pesquisa em neuropsicofarmacologia vem de uma ampla gama de atividades em neurociência e pesquisa clínica. Isso motivou organizações como o American College of Neuropsychopharmacology (ACNP) , o European College of Neuropsychopharmacology (ECNP) e o Collegium Internationale Neuro-psychopharmacologicum (CINP) a serem estabelecidas como uma medida de enfoque. O ECNP publica Neuropsicofarmacologia Europeia e, como parte do Reed Elsevier Group , o ACNP publica o jornal Neuropsychopharmacology e o CINP publica o jornal International Journal of Neuropsychopharmacology com Cambridge University Press . Em 2002, foi compilado um trabalho abrangente recente do ACNP, "Neuropsicofarmacologia: A Quinta Geração do Progresso". É uma medida do estado do conhecimento em 2002 e pode-se dizer que representa um marco na meta de um século de estabelecer os princípios neurobiológicos básicos que governam as ações do cérebro.
Existem muitos outros periódicos que contêm informações relevantes, como Neurociências . Alguns deles estão listados na Biblioteca da Brown University .
Veja também
Notas
Referências
- ("4ª Geração" e "5ª Geração" referem-se a ACNP, consulte os links)
- ^ "The history of HCNP: Exchange information and catalysing progress",ECNP Newsletter, N7 (2004)
- ^ Fujita, M. e Innis, RB, "In vivoMolecular Imaging: Ligand Development And Research Applications", (5th Gen. Prog.)
- ^ Tallman, JF,"Neuropsychopharmacology at the New Millennium: New Industry Directions",Neuropsychopharmacology20 (1999)
- ^ Bloom, FE, "Introdução à Neuropsicofarmacologia Pré-clínica", (4º Geração Prog.)
- ^ Watson, SJ e Cullinan, WE, "Cytology and Circuitry", (4ª Geração Prog.)
- ^ Physicians 'Desk Reference, 1990, 2005
- ^ Erowid,"The Neuropharmacology of γ-hydroxybutyrate (GHB)"(2004)
- ^ Tallman, JF, Cassella, J., Kehne, J., "Mechanism Of Action Of Anxiolytics", (5th Gen. Prog.)
- ^ Depoortère, R.,e outros. , "Neurochemical, Electrophysiological and Pharmacological Profiles of the Selective Inhibitor of the Glycine Transporter-1 SSR504734, a Potential New Type of Antipsychotic",Neuropsychopharmacology30, pp1963-1985, (2005)
- ^ Abraham, HD, Mccann, UD, Ricaurte, GA, "Psychedelic Drugs", (5th Gen. Prog.)
- ^ Colwell, CS, "Circadian Rhythms", (4º Geração Prog.)
- ^ Lewy, AJ, "Circadian Phase Sleep And Mood Disorders", (5º Geração Prog.)
links externos
- Recursos ACNP
- Organizações
- Collegium Internationale Neuro-psychopharmacologicum Uma organização global dedicada à neuropsicofarmacologia
- Colégio Europeu de Neuropsicofarmacologia
- Diários
- Neuropsychopharmacology Journal - Publicação oficial do American College of Neuropsychopharmacology
- European Neuropsychopharmacology - An Elsevier journal
- The International Journal of Neuropsychopharmacology - Uma publicação da Cambridge University Press
- Neuropsychopharmacology and Therapeutics por Ivor Ebenezer (2015), John Wiley & Sons, Chichester, Reino Unido, ISBN 978-1-118-38565-4

