Proteína básica de mielina - Myelin basic protein
| Myelin_MBP | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Myelin_MBP | ||||||||
| Pfam | PF01669 | ||||||||
| InterPro | IPR000548 | ||||||||
| PRÓSITO | PDOC00492 | ||||||||
| SCOP2 | 1bx2 / SCOPe / SUPFAM | ||||||||
| Superfamília OPM | 274 | ||||||||
| Proteína OPM | 2lug | ||||||||
| |||||||||
A proteína básica da mielina ( MBP ) é uma proteína considerada importante no processo de mielinização dos nervos do sistema nervoso . A bainha de mielina é uma membrana multicamadas, exclusiva do sistema nervoso, que funciona como um isolante para aumentar muito a velocidade de condução do impulso axonal . A MBP mantém a estrutura correta da mielina, interagindo com os lipídios da membrana da mielina.
A MBP foi sequenciada inicialmente em 1971 após o isolamento das membranas de mielina bovina . Camundongos knockout para MBP , chamados de ratos shiverer, foram posteriormente desenvolvidos e caracterizados no início dos anos 1980. Camundongos Shiverer exibem quantidades diminuídas de mielinização do SNC e um distúrbio progressivo caracterizado por tremores , convulsões e morte prematura. O gene humano para MBP está no cromossomo 18 ; a proteína se localiza no SNC e em várias células da linhagem hematopoiética .
O pool de MBP no sistema nervoso central é muito diverso, com várias variantes de splice sendo expressas e um grande número de modificações pós-tradução na proteína, que incluem fosforilação , metilação , desamidação e citrulinação . Estas formas diferem pela presença ou ausência de péptidos curtos (10 a 20 resíduos) em várias localizações internas na sequência . Em geral, a forma principal de MBP é uma proteína de cerca de 18,5 Kd (170 resíduos).
Em tipos de células melanocíticas, a expressão do gene MBP pode ser regulada por MITF .
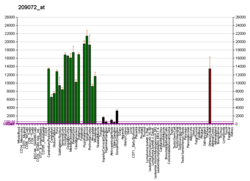
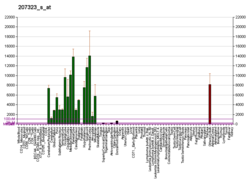
Expressão genetica
A proteína codificada pelo gene MBP clássico é o principal constituinte da bainha de mielina dos oligodendrócitos e das células de Schwann no sistema nervoso. No entanto, os transcritos relacionados com MBP também estão presentes na medula óssea e no sistema imunológico. Esses mRNAs surgem do gene MBP longo (também denominado "Golli-MBP") que contém 3 exons adicionais localizados a montante dos exons MBP clássicos. O splicing alternativo dos locais de início da transcrição de Golli e MBP dá origem a 2 conjuntos de transcritos relacionados com MBP e produtos gênicos. Os mRNAs de Golli contêm 3 exons exclusivos de Golli-MBP, emendados in-frame para 1 ou mais exons de MBP. Eles codificam proteínas híbridas que possuem a sequência Golli aa do terminal N ligada à sequência MBP aa. A segunda família de transcritos contém apenas exons MBP e produzem as proteínas básicas da mielina bem caracterizadas. Essa complexa estrutura gênica é conservada entre as espécies, sugerindo que a unidade de transcrição MBP é parte integrante da unidade de transcrição de Golli e que esse arranjo é importante para a função e / ou regulação desses genes.
Estrutura
A proteína básica da mielina foi classificada como uma proteína intrinsecamente desordenada que não possui estrutura secundária estável em solução. Como a maioria dos IDPs, ele tem uma carga líquida alta e uma hidrofobicidade média baixa, minimizando o efeito hidrofóbico que impulsiona o dobramento tradicional de proteínas. Ele contém algumas exceções ao conteúdo normal de aminoácidos do IDP. Por exemplo, MBP tem mais arginina e menos ácido glutâmico do que a maioria dos IDPs. No entanto, isso é provável porque essas alterações são necessárias para que a MBP seja suficientemente básica e carregada positivamente para interagir corretamente com a membrana. Notavelmente, MBP demonstrou adotar uma estrutura secundária mais estável na interação com lipídios. Experimentos de NMR e de marcação por spin específicos de Cys previram que essa estrutura continha folha beta e regiões de hélice anfipática .
Como implícito em seu nome, a proteína básica da mielina é significativamente básica, com um ponto isoelétrico de 10. Acredita-se que ela se associe à membrana celular por meio de interações eletrostáticas entre suas cargas positivas e as cabeças fosfolipídicas negativamente carregadas da membrana plasmática. Ele pode sofrer uma grande variedade de modificações pós-tradução, criando vários isômeros de carga conhecidos como C1-C6 ou C8. Essas modificações incluem fosforilação , metilação , desamidação , citrulinação , ADP-ribosilação e acilação N-terminal . C1 é o menos modificado, enquanto C8 é o mais distinto, contendo 6-11 citrulinações adicionais. Uma vez que cada um deles diminui sua carga positiva, C8 tem a menor carga positiva líquida dos isômeros. As alternâncias nessas modificações pós-traducionais têm sido associadas a doenças desmielinizantes . Notavelmente, o MBP isolado de indivíduos com esclerose múltipla apresentou maior grau de citrulinação e menor carga positiva. Em um caso raro e grave de EM conhecido como síndrome de Marburg, a citrulinação foi ainda mais extensa.
Papel na doença
O interesse pela MBP tem se centrado em seu papel nas doenças desmielinizantes , em particular na esclerose múltipla (EM). O antígeno alvo da resposta autoimune na EM ainda não foi identificado. No entanto, vários estudos têm mostrado um papel dos anticorpos contra MBP na patogênese da EM. Alguns estudos ligaram uma predisposição genética à MS ao gene MBP, embora a maioria não o tenha feito.
Foi sugerida uma hipótese de "mimetismo molecular" de esclerose múltipla, em que as células T estão, em essência, confundindo MBP com herpesvírus-6 humano . Pesquisadores nos Estados Unidos criaram um peptídeo sintético com uma sequência idêntica à de um peptídeo HHV-6. Níveis elevados de MBP foram encontrados no líquido cefalorraquidiano de pacientes com infecções por HIV e sinais de encefalopatia e, embora MBP não pareça ser um marcador diagnóstico sensível de encefalopatia por HIV, foi sugerido que pode servir como um prognóstico indicador de progressão da doença. É capaz de mostrar que as células T foram ativadas por esse peptídeo. Essas células T ativadas também reconheceram e iniciaram uma resposta imune contra uma sequência de peptídeo criada sinteticamente que é idêntica a parte da MBP humana. Durante a pesquisa, eles descobriram que os níveis dessas células T de reação cruzada são significativamente elevados em pacientes com esclerose múltipla.
Algumas pesquisas mostraram que inocular um animal com MBP para gerar uma resposta imune específica de MBP contra ela aumenta a permeabilidade da barreira hematoencefálica . A permeabilidade é aumentada quando o animal é inoculado contra proteínas não específicas.
Uma resposta imune direcionada ao MBP foi implicada na infecção letal por raiva . A inoculação de MBP gera aumenta a permeabilidade da barreira hematoencefálica (BBB), permitindo que as células imunes entrem no cérebro, o principal local de replicação do vírus da raiva. Em um estudo de camundongos infectados com o vírus da raiva do morcego de cabelo prateado (SHBRV), a taxa de mortalidade dos camundongos tratados com MBP melhorou 20% -30% em relação ao grupo de controle não tratado. É significativo notar que camundongos saudáveis não infectados tratados com MBP mostraram um aumento na taxa de mortalidade entre 0% e 40%.
Interações
Demonstrou-se que a proteína básica da mielina interage in vivo com a proteína proteolipídica 1 e in vitro com calmodulina , actina , tropomiosina , tubulina , clatrina , 2 ', 3'-nucleotídeo cíclico 3'-fosfodiesterase e várias moléculas do sistema imunológico .
Referências
Leitura adicional
- Boylan KB, Ayres TM, Popko B, Takahashi N, Hood LE, Prusiner SB (janeiro de 1990). "DNA repetitivo (TGGA) n 5 'para o gene da proteína básica da mielina humana: uma nova forma de sequência repetitiva de oligonucleotídeo mostrando polimorfismo de comprimento". Genômica . 6 (1): 16–22. doi : 10.1016 / 0888-7543 (90) 90443-X . PMID 1689270 .
- Kishimoto A, Nishiyama K, Nakanishi H, Uratsuji Y, Nomura H, Takeyama Y, Nishizuka Y (outubro de 1985). "Estudos sobre a fosforilação da proteína básica da mielina pela proteína quinase C e proteína quinase dependente de adenosina 3 ': 5'-monofosfato" . The Journal of Biological Chemistry . 260 (23): 12492–9. doi : 10.1016 / S0021-9258 (17) 38898-1 . PMID 2413024 .
- Saxe DF, Takahashi N., Hood L., Simon MI (1985). "Localização do gene da proteína básica da mielina humana (MBP) para a região 18q22 ---- qter por hibridização in situ". Citogenética e genética celular . 39 (4): 246–9. doi : 10.1159 / 000132152 . PMID 2414074 .
- Kamholz J, de Ferra F, Puckett C, Lazzarini R (julho de 1986). "Identificação de três formas de proteína básica de mielina humana por clonagem de cDNA" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 83 (13): 4962–6. Bibcode : 1986PNAS ... 83.4962K . doi : 10.1073 / pnas.83.13.4962 . PMC 323864 . PMID 2425357 .
- Scoble HA, Whitaker JN, Biemann K (agosto de 1986). "Análise da sequência primária de peptídeos de proteína básica de mielina humana 1-44 e 90-170 por espectrometria de massa de bombardeamento de átomo rápido". Journal of Neurochemistry . 47 (2): 614–6. doi : 10.1111 / j.1471-4159.1986.tb04544.x . PMID 2426402 . S2CID 22531833 .
- Roth HJ, Kronquist K., Pretorius PJ, Crandall BF, Campagnoni AT (1986). "Isolamento e caracterização de um cDNA que codifica para uma nova variante da proteína básica de mielina humana 17.3K (MBP)". Journal of Neuroscience Research . 16 (1): 227–38. doi : 10.1002 / jnr.490160120 . PMID 2427738 . S2CID 38277667 .
- Popko B, Puckett C, Lai E, Shine HD, Readhead C, Takahashi N, et al. (Fevereiro de 1987). "Camundongos deficientes de mielina: expressão da proteína básica de mielina e geração de camundongos com níveis variados de mielina". Cell . 48 (4): 713–21. doi : 10.1016 / 0092-8674 (87) 90249-2 . PMID 2434243 . S2CID 25224473 .
- Kamholz J, Spielman R, Gogolin K., Modi W, O'Brien S, Lazzarini R (abril de 1987). "O gene da proteína básica da mielina humana: localização cromossômica e análise de RFLP" . American Journal of Human Genetics . 40 (4): 365–73. PMC 1684086 . PMID 2437795 .
- Roth HJ, Kronquist KE, Kerlero de Rosbo N., Crandall BF, Campagnoni AT (1987). "Evidência para a expressão de quatro variantes da proteína básica da mielina no desenvolvimento da medula espinhal humana através da clonagem de cDNA". Journal of Neuroscience Research . 17 (4): 321–8. doi : 10.1002 / jnr.490170402 . PMID 2442403 . S2CID 37138877 .
- Shoji S, Ohnishi J, Funakoshi T, Fukunaga K, Miyamoto E, Ueki H, Kubota Y (novembro de 1987). "Locais de fosforilação de proteína básica de mielina de cérebro bovino fosforilada com proteína quinase dependente de Ca2 + -calmodulina de cérebro de rato" . Journal of Biochemistry . 102 (5): 1113–20. doi : 10.1093 / oxfordjournals.jbchem.a122149 . PMID 2449425 .
- Wood DD, Moscarello MA (março de 1989). "O isolamento, caracterização e propriedades de agregação de lipídios de uma proteína básica de mielina contendo citrulina" . The Journal of Biological Chemistry . 264 (9): 5121–7. doi : 10.1016 / S0021-9258 (18) 83707-3 . PMID 2466844 .
- Edwards AM, Ross NW, Ulmer JB, Braun PE (janeiro de 1989). "Interação da proteína básica da mielina e proteína proteolipídica". Journal of Neuroscience Research . 22 (1): 97–102. doi : 10.1002 / jnr.490220113 . PMID 2467009 . S2CID 33666906 .
- Streicher R, Stoffel W (maio de 1989). "A organização do gene da proteína básica da mielina humana. Comparação com o gene do camundongo". Biological Chemistry Hoppe-Seyler . 370 (5): 503–10. doi : 10.1515 / bchm3.1989.370.1.503 . PMID 2472816 .
- Lennon VA, Wilks AV, Carnegie PR (novembro de 1970). "Propriedades imunológicas do principal peptídeo encefalitogênico da proteína básica da mielina humana". Journal of Immunology . 105 (5): 1223–30. PMID 4099924 .
- Carnegie PR (junho de 1971). "Sequência de aminoácidos da proteína básica encefalitogênica da mielina humana" . The Biochemical Journal . 123 (1): 57–67. doi : 10.1042 / bj1230057 . PMC 1176899 . PMID 4108501 .
- Baldwin GS, Carnegie PR (fevereiro de 1971). "Metilação enzimática específica de uma arginina na proteína experimental da encefalomielite alérgica da mielina humana". Ciência . 171 (3971): 579–81. Bibcode : 1971Sci ... 171..579B . doi : 10.1126 / science.171.3971.579 . PMID 4924231 . S2CID 36959912 .
- Baldwin GS, Carnegie PR (junho de 1971). "Isolamento e caracterização parcial de argininas metiladas da proteína básica encefalitogênica da mielina" . The Biochemical Journal . 123 (1): 69–74. doi : 10.1042 / bj1230069 . PMC 1176900 . PMID 5128665 .
- Wood DD, Vella GJ, Moscarello MA (outubro de 1984). "Interação entre a proteína básica da mielina humana e a lipofilina". Neurochemical Research . 9 (10): 1523–31. doi : 10.1007 / BF00964678 . PMID 6083474 . S2CID 9751765 .
- Gibson BW, Gilliom RD, Whitaker JN, Biemann K (abril de 1984). "Sequência de aminoácidos do peptídeo 45-89 da proteína básica da mielina humana conforme determinado por espectrometria de massa" . The Journal of Biological Chemistry . 259 (8): 5028–31. doi : 10.1016 / S0021-9258 (17) 42950-4 . PMID 6201481 .
- Pribyl TM, Campagnoni CW, Kampf K, Kashima T, Handley VW, McMahon J, Campagnoni AT (novembro de 1993). "O gene da proteína básica da mielina humana está incluído em uma unidade de transcrição de 179 quilobases: expressão nos sistemas imunológico e nervoso central" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 90 (22): 10695–9. Bibcode : 1993PNAS ... 9010695P . doi : 10.1073 / pnas.90.22.10695 . PMC 47844 . PMID 7504278 .
- Shanshiashvili L, Mikeladze D (2003). "Alguns aspectos da proteína básica da mielina". J. Biol. Phys. Chem . 3 (3): 96–9. doi : 10.4024 / 18SH03R.jbpc.03.03 .
links externos
-
 Mídia relacionada às proteínas básicas de mielina no Wikimedia Commons
Mídia relacionada às proteínas básicas de mielina no Wikimedia Commons - Visão geral de todas as informações estruturais disponíveis no PDB para UniProt : P02686 (proteína básica de mielina) no PDBe-KB .
Este artigo incorpora texto da Biblioteca Nacional de Medicina dos Estados Unidos , que é de domínio público .