Mentol - Menthol
|
|
|||

|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
5-Metil-2- (propan-2-il) ciclohexan-1-ol |
|||
| Outros nomes
2-Isopropil-5-metilciclohexan-1-ol
2-Isopropil-5-metilciclohexanol 3- p- Mentanol Hexahidrotimol Menthomentol Cânfora de hortelã-pimenta |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.016.992 |
||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 10 H 20 O | |||
| Massa molar | 156,269 g · mol −1 | ||
| Aparência | Sólido cristalino branco ou incolor | ||
| Densidade | 0,890 g · cm −3 , sólido (racêmico ou (-) - isômero) |
||
| Ponto de fusão | 36-38 ° C (97-100 ° F; 309-311 K) racêmico 42-45 ° C, (-) - isômero, forma cristalina α |
||
| Ponto de ebulição | 214,6 ° C (418,3 ° F; 487,8 K) | ||
| Ligeiramente solúvel, (-) - isômero | |||
| Perigos | |||
| Riscos principais | Irritante, inflamável | ||
| Ficha de dados de segurança |
Veja: página de dados FISPQ Externa |
||
| Frases R (desatualizado) | R37 / 38 , R41 | ||
| Frases S (desatualizado) | S26 , S36 | ||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 93 ° C (199 ° F; 366 K) | ||
| Compostos relacionados | |||
|
Álcoois relacionados
|
Ciclohexanol , Pulegol , Dihydrocarveol , piperitol |
||
|
Compostos relacionados
|
Menthone , menteno , timol , p - cimeno , Citronelal |
||
| Página de dados suplementares | |||
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|||
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
||
| UV , IR , NMR , MS | |||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O mentol é um composto orgânico feito sinteticamente ou obtido a partir dos óleos de menta de milho , hortelã- pimenta ou outras balas . É uma substância cerosa, cristalina , límpida ou de cor branca, que é sólida à temperatura ambiente e derrete ligeiramente acima.
A principal forma de mentol que ocorre na natureza é (-) - mentol , ao qual é atribuída a configuração ( 1R , 2S , 5R ) . O mentol tem qualidades de anestésico local e anti- irritante , e é amplamente usado para aliviar irritações menores na garganta . O mentol também atua como um fraco agonista do receptor κ-opióide .
Em 2017, era o 193º medicamento mais prescrito nos Estados Unidos, com mais de dois milhões de prescrições.
Estrutura
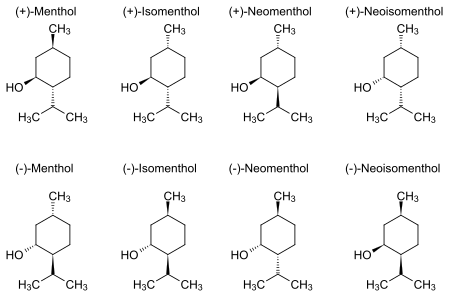
O mentol natural existe como um estereoisômero puro , quase sempre na forma (1 R , 2 S , 5 R ) (canto inferior esquerdo do diagrama abaixo). Os oito estereoisômeros possíveis são:
No composto natural, o grupo isopropil está na orientação trans para os grupos metil e hidroxil . Assim, ele pode ser desenhado de qualquer uma das maneiras mostradas:
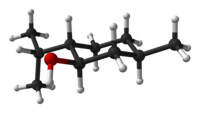
Os (+) - e (-) - enantiômeros do mentol são os mais estáveis entre eles com base em suas conformações de ciclohexano . Com o próprio anel em conformação de cadeira, todos os três grupos volumosos podem se orientar em posições equatoriais.
As duas formas de cristal para mentol racêmico têm pontos de fusão de 28 ° C e 38 ° C. O (-) - mentol puro tem quatro formas de cristal, das quais a mais estável é a forma α, as conhecidas agulhas largas.
Propriedades biológicas

A capacidade do mentol de acionar quimicamente os receptores TRPM8 sensíveis ao frio na pele é responsável pela conhecida sensação de resfriamento que provoca quando inalado, comido ou aplicado na pele. Nesse sentido, é semelhante à capsaicina , o químico responsável pelo apimentado da pimenta malagueta (que estimula os sensores de calor , também sem provocar uma mudança real de temperatura).
As propriedades analgésicas do mentol são mediadas por uma ativação seletiva dos receptores κ- opioides . O mentol bloqueia os canais de cálcio e os canais de sódio sensíveis à voltagem , reduzindo a atividade neural que pode estimular os músculos.
Alguns estudos mostram que o mentol atua como modulador alostérico positivo do receptor GABA A e aumenta a transmissão gabaérgica nos neurônios PAG. Mentol também partilha anestésicos propriedades semelhantes ao propofol , por modulação dos mesmos locais do GABA A receptor .
O mentol é amplamente utilizado na área odontológica como agente antibacteriano tópico, eficaz contra diversos tipos de estreptococos e lactobacilos .
Ocorrência
Mentha arvensis (hortelã selvagem) é a principal espécie de hortelã usada para fazer cristais de mentol naturais e flocos de mentol naturais. Esta espécie é cultivada principalmente na região de Uttar Pradesh , na Índia .
O mentol ocorre naturalmente no óleo de hortelã-pimenta (junto com um pouco de mentona , o éster de acetato de mentila e outros compostos), obtido da Mentha × piperita (hortelã-pimenta). O mentol japonês também contém uma pequena porcentagem do 1- epímero , neomentol.
Biossíntese
A biossíntese de mentol foi investigada em Mentha × piperita e as enzimas envolvidas foram identificadas e caracterizadas. Ela começa com a síntese do terpeno limoneno , seguida pela hidroxilação e, em seguida, várias etapas de redução e isomerização .
Mais especificamente, a biossíntese de (-) - mentol ocorre nas células da glândula secretora da planta de hortelã-pimenta. Geranil difosfato sintase (GPPS), primeiro catalisa a reação de IPP e DMAPP em geranil difosfato . Em seguida, a (-) - limoneno sintase (LS) catalisa a ciclização do difosfato de geranila em (-) - limoneno . (-) - Limoneno-3-hidroxilase (L3OH), usando O 2 e NADPH , então catalisa a hidroxilação alílica de (-) - limoneno na posição 3 para (-) - trans-isopiperitenol. (-) - trans- isopiperitenol desidrogenase (iPD) oxida ainda mais o grupo hidroxila na posição 3 usando NAD + para formar (-) - isopiperitenona. A (-) - isopiperitenona redutase (iPR) reduz então a ligação dupla entre os carbonos 1 e 2 usando NADPH para formar (+) - cis- isopulegona. A (+) - cis- isopulegona isomerase (iPI) então isomeriza a ligação dupla restante para formar (+) - pulegona. (+) - Pulegone redutase (PR) então reduz esta ligação dupla usando NADPH para formar (-) - mentona. (-) - Mentona redutase (MR) então reduz o grupo carbonila usando NADPH para formar (-) - mentol.
Produção
O mentol natural é obtido pelo congelamento do óleo de hortelã-pimenta . Os cristais de mentol resultantes são então separados por filtração .
A produção mundial total de mentol em 1998 foi de 12.000 toneladas, das quais 2.500 toneladas foram sintéticas. Em 2005, a produção anual de mentol sintético quase dobrou. Os preços estão na faixa de US $ 10-20 / kg, com picos na região de US $ 40 / kg, mas chegaram a US $ 100 / kg. Em 1985, estimava-se que a China produzia a maior parte do suprimento mundial de mentol natural, embora pareça que a Índia empurrou a China para o segundo lugar.
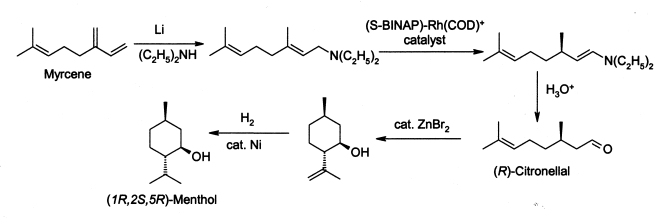
O mentol é fabricado como um único enantiômero (94% ee ) na escala de 3.000 toneladas por ano pela Takasago International Corporation . O processo envolve uma síntese assimétrica desenvolvida por uma equipe liderada por Ryōji Noyori , que ganhou o Prêmio Nobel de Química de 2001 em reconhecimento ao seu trabalho neste processo:
O processo começa com a formação de uma amina alílica de mirceno , que sofre isomerização assimétrica na presença de um complexo de ródio BINAP para dar (após hidrólise ) R - citronelal enantiomericamente puro . Este é ciclizado por uma reação de carbonil-eno iniciada por brometo de zinco em isopulegol , que é então hidrogenado para dar ( 1R , 2S , 5R ) -mentol puro .
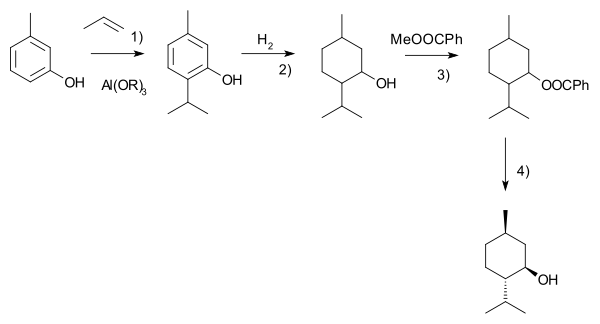
Outro processo comercial é o processo Haarmann-Reimer (após a empresa Haarmann & Reimer, agora parte da Symrise ). Esse processo começa a partir do m- cresol que é alquilado com propeno em timol . Este composto é hidrogenado na próxima etapa. O mentol racêmico é isolado por destilação fracionada . Os enantiômeros são separados por resolução quiral em reação com benzoato de metila , cristalização seletiva seguida de hidrólise.
O mentol racêmico também pode ser formado por hidrogenação de timol , mentona ou pulegona . Em ambos os casos, com processamento posterior (resolução de arrastamento cristalizador do conglomerado de benzoato de mentila) é possível concentrar o enantiômero L , no entanto, este tende a ser menos eficiente, embora os custos de processamento mais elevados possam ser compensados por menores custos de matéria-prima. Uma outra vantagem deste processo é que o D- mentol se torna acessível para uso como um auxiliar quiral, junto com o antípodo L mais usual .
Formulários
O mentol está incluído em muitos produtos e por vários motivos. Esses incluem:
- Em produtos sem receita para o alívio de curto prazo de pequenas dores de garganta e pequenas irritações na boca ou na garganta.
- Exemplos: protetores labiais e remédios para tosse .
- Como antipruriginoso para reduzir a coceira.
- Como analgésico tópico , é usado para aliviar dores menores, como cãibras musculares, entorses, dores de cabeça e condições semelhantes, sozinho ou combinado com produtos químicos como cânfora , óleo de eucalipto ou capsaicina . Na Europa, tende a aparecer como um gel ou um creme, enquanto nos Estados Unidos os adesivos e mangas corporais são muito usados.
- Exemplos: tigre bálsamo , ou IcyHot manchas ou joelho / cotovelo mangas .
- Como um intensificador de penetração na administração transdérmica de drogas .
- Em descongestionantes para o tórax e seios da face (creme, adesivo ou inalador nasal).
- Exemplos: Vicks VapoRub , Mentholatum , VapoRem, Mentisan.
- Em certos medicamentos usados para tratar queimaduras solares , uma vez que proporciona uma sensação de resfriamento (então frequentemente associada ao babosa ).
- Em produtos pós-barba para aliviar a queimadura de navalha .
- Como aditivo para fumar em algumas marcas de cigarros , para dar sabor e para reduzir a irritação da garganta e dos seios nasais causada pelo fumo. O mentol também aumenta a densidade do receptor de nicotina, aumentando o potencial de dependência dos produtos do tabaco.
- Comumente usado em produtos de higiene oral e remédios para o mau hálito, como enxaguatórios bucais , pasta de dente , sprays para a boca e a língua e, mais geralmente, como um agente aromatizante de alimentos; como em chicletes e doces .
- Como pesticida contra os ácaros traqueais das abelhas .
- Na perfumaria , o mentol é usado para preparar ésteres mentílicos para enfatizar as notas florais (especialmente rosa).
- Em produtos de primeiros socorros como "gelo mineral" para produzir um efeito refrescante como substituto do gelo real na ausência de água ou eletricidade (bolsa, adesivo corporal / manga ou creme).
- Em vários remendos, desde remendos para redução da febre aplicados na testa de crianças a "remendos nos pés" para aliviar inúmeras doenças (o último sendo muito mais frequente e elaborado na Ásia , especialmente no Japão : algumas variedades usam "protuberâncias funcionais" ou pequenos inchaços para massagear os pés, além de acalmá-los e resfriá-los).
- Em alguns produtos de beleza, como condicionadores de cabelo, à base de ingredientes naturais (por exemplo, St. Ives).
- Como um relaxante antiespasmódico e de músculo liso em endoscopia digestiva alta .
Na química orgânica , o mentol é usado como um auxiliar quiral na síntese assimétrica . Por exemplo, ésteres de sulfinato feitos de cloretos de sulfinila e mentol podem ser usados para fazer sulfóxidos enantiomericamente puros por reação com reagentes de organolítio ou reagentes de Grignard . O mentol reage com os ácidos carboxílicos quirais para dar ésteres mentílicos diastereômicos, que são úteis para a resolução quiral .
- Ele pode ser usado como um catalisador para a produção de sódio para o químico amador por meio do processo de redução de magnésio catalisado por álcool.
- mentol é potencialmente ergogênico (melhora o desempenho) para o desempenho atlético em ambientes quentes
Reações
O mentol reage de várias maneiras como um álcool secundário normal. É oxidado a mentona por agentes oxidantes, como ácido crômico ou dicromato , embora sob algumas condições a oxidação possa ir mais longe e quebrar o anel. O mentol é facilmente desidratado para dar principalmente 3-menteno, pela ação do ácido sulfúrico a 2% . Pentacloreto de fósforo (PCl 5 ) dá cloreto de mentilo.
História
No Ocidente , o mentol foi isolado pela primeira vez em 1771, pelo alemão Hieronymus David Gaubius . As primeiras caracterizações foram feitas por Oppenheim, Beckett, Moriya e Atkinson. Foi nomeado por FL Alphons Oppenheim (1833-1877) em 1861.
Status de compêndio
Segurança
A dose letal estimada para mentol (e óleo de hortelã-pimenta ) em humanos pode ser tão baixa quanto 50–500 mg / kg, (DL50 Aguda: 3300 mg / kg [Rato]. 3400 mg / kg [Rato]. 800 mg / kg [ Gato]).
A sobrevivência após doses de 8 a 9 g foi relatada. Os efeitos da overdose são dor abdominal, ataxia, fibrilação atrial, bradicardia, coma, tontura, letargia, náusea, erupção cutânea, tremor, vômito, vertigem.
Veja também
Referências
Leitura adicional
- Turner, EE; Harris, MM (1952). Química Orgânica . Londres: Longmans, Green & Co.
- Handbook of Chemistry and Physics (71ª ed.). Ann Arbor, MI: CRC Press. 1990.
- The Merck Index (7ª ed.). Rahway, NJ: Merck & Co. 1960.
- "Perfil químico de aroma: mentol". Perfumista e aromatizante . 32 (12): 38–47. Dezembro de 2007.
- Colacot, TJ (1 de abril de 2002). "Prêmio Nobel de Química de 2001: Reconhecimento oportuno para reações quirais catalisadas por ródio, rutênio e ósmio" . Platinum Metals Rev . 46 (2): 82–83.
links externos
- "Mentol" . Portal de informações sobre medicamentos . Biblioteca Nacional de Medicina dos EUA.
- Palestra Ryoji Noyori Nobel (2001)
- Uma análise de mentol do Science Creative Quarterly