Hidrazina - Hydrazine
|
|
|||
|
|
|||
 Hidrato de hidrazina
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC sistemático
Hidrazina |
|||
| Outros nomes
Diamina; Diazane; Tetrahidridodinitrogênio ( N - N ); diamidogênio
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 3DMet | |||
| 878137 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,005,560 |
||
| Número EC | |||
| 190 | |||
| KEGG | |||
| Malha | Hidrazina | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 2029 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
|
N 2H 4 |
|||
| Massa molar | 32,0452 g · mol −1 | ||
| Aparência | Líquido incolor, fumegante, oleoso | ||
| Odor | Semelhante a amônia | ||
| Densidade | 1,021 g · cm -3 | ||
| Ponto de fusão | 2 ° C; 35 ° F; 275 K | ||
| Ponto de ebulição | 114 ° C; 237 ° F; 387 K | ||
| Miscível | |||
| log P | 0,67 | ||
| Pressão de vapor | 1 kPa (a 30,7 ° C) | ||
| Acidez (p K a ) | 8,10 (N 2 H 5 + ) | ||
| Basicidade (p K b ) | 5,90 | ||
| Ácido conjugado | Hidrazínio | ||
|
Índice de refração ( n D )
|
1,46044 (a 22 ° C) | ||
| Viscosidade | 0,876 cP | ||
| Estrutura | |||
| Piramidal triangular em N | |||
| 1,85 D | |||
| Termoquímica | |||
|
Entropia molar padrão ( S |
121,52 J · K −1 · mol −1 | ||
| 50,63 kJ · mol −1 | |||
| Perigos | |||
| Ficha de dados de segurança | ICSC 0281 | ||
| Pictogramas GHS |
    
|
||
| Palavra-sinal GHS | Perigo | ||
| H226 , H301 , H311 , H314 , H317 , H331 , H350 , H410 | |||
| P201 , P261 , P273 , P280 , P301 + 310 , P305 + 351 + 338 | |||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 52 ° C (126 ° F; 325 K) | ||
| 24 a 270 ° C (75 a 518 ° F; 297 a 543 K) | |||
| Limites explosivos | 1,8–99,99% | ||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
59-60 mg / kg (oral em ratos, camundongos) | ||
|
LC 50 ( concentração média )
|
260 ppm (rato, 4 horas) 630 ppm (rato, 1 hora) 570 ppm (rato, 4 horas) 252 ppm (rato, 4 horas) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 1 ppm (1,3 mg / m 3 ) [pele] | ||
|
REL (recomendado)
|
Ca C 0,03 ppm (0,04 mg / m 3 ) [2 horas] | ||
|
IDLH (perigo imediato)
|
Ca [50 ppm] | ||
| Compostos relacionados | |||
|
Outros ânions
|
Tetrafluorohidrazina Peróxido de hidrogênio Difosfano Tetraiodeto de difósforo |
||
|
Outros cátions
|
Hidrazinas orgânicas | ||
|
Azanos binários relacionados
|
Ammonia Triazane |
||
|
Compostos relacionados
|
Diazeno triazeno Tetrazene Diphosphene |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
A hidrazina é um composto inorgânico com a fórmula química N
2H
4. É um hidreto de pnictogênio simples e é um líquido inflamável incolor com um odor semelhante ao da amônia .
A hidrazina é altamente tóxica, a menos que tratada em solução como, por exemplo, hidrato de hidrazina ( NH
2NH
2 · XH
2O ). Em 2015, o mercado mundial de hidrato de hidrazina somava US $ 350 milhões. A hidrazina é usada principalmente como um agente espumante na preparação de espumas de polímero , mas as aplicações também incluem seu uso como um precursor de catalisadores de polimerização , produtos farmacêuticos e agroquímicos, bem como um propelente armazenável de longo prazo para a propulsão de espaçonaves no espaço .
Cerca de dois milhões de toneladas de hidrato de hidrazina foram usados em agentes de expansão de espuma em 2015. Além disso, a hidrazina é usada em vários combustíveis para foguetes e para preparar os precursores de gás usados em airbags . A hidrazina é usada em ciclos de vapor de usinas de energia elétrica nuclear e convencional como um eliminador de oxigênio para controlar as concentrações de oxigênio dissolvido em um esforço para reduzir a corrosão.
Hidrazinas referem-se a uma classe de substâncias orgânicas derivadas da substituição de um ou mais átomos de hidrogênio na hidrazina por um grupo orgânico.
Usos
Produtores de gás e propelentes
A maior parte do uso da hidrazina é como um precursor de agentes de expansão . Compostos específicos incluem azodicarbonamida e azobisisobutironitrila , que produzem 100–200 mL de gás por grama de precursor. Em uma aplicação relacionada, a azida de sódio , o agente formador de gás nos airbags , é produzida a partir da hidrazina por reação com nitrito de sódio .
A hidrazina também é usada como propelente armazenável a longo prazo a bordo de veículos espaciais , como a missão Dawn para Ceres e Vesta, e para reduzir a concentração de oxigênio dissolvido e controlar o pH da água usada em grandes caldeiras industriais. O jato de combate F-16 , o Eurofighter Typhoon , o ônibus espacial e o avião espião U-2 usam hidrazina para abastecer suas unidades de energia auxiliares .
Precursor de pesticidas e produtos farmacêuticos
A hidrazina é um precursor de vários produtos farmacêuticos e pesticidas. Freqüentemente, essas aplicações envolvem a conversão de hidrazina em anéis heterocíclicos , como pirazóis e piridazinas . Exemplos de derivados de hidrazina bioativos comercializados incluem cefazolina , rizatriptano , anastrozol , fluconazol , metazacloro , metamitron , metribuzina , paclobutrazol , diclobutrazol , propiconazol , sulfato de hidrazina , diimida , triadimefon e dibenzoil- hidrazina .
Os compostos de hidrazina podem ser eficazes como ingredientes ativos em mistura com ou em combinação com outros produtos químicos agrícolas, como inseticidas, miticidas, nematicidas, fungicidas, agentes antivirais, atrativos, herbicidas ou reguladores de crescimento de plantas.
Pequena escala, nicho e pesquisa
A fabricante italiana de catalisadores Acta (empresa química) propôs o uso da hidrazina como alternativa ao hidrogênio nas células a combustível . O principal benefício do uso da hidrazina é que ela pode produzir mais de 200 m W / cm 2 a mais do que uma célula de hidrogênio semelhante, sem a necessidade de usar catalisadores de platina caros . Como o combustível é líquido à temperatura ambiente, ele pode ser manuseado e armazenado com mais facilidade do que o hidrogênio. Ao armazenar a hidrazina em um tanque cheio de carbono de ligação dupla - carbonila de oxigênio , o combustível reage e forma um sólido seguro chamado hidrazona . Ao lavar o tanque com água morna, o hidrato de hidrazina líquido é liberado. A hidrazina tem uma força eletromotriz superior de 1,56 V em comparação com 1,23 V para o hidrogênio. A hidrazina se decompõe na célula para formar nitrogênio e hidrogênio, que se ligam ao oxigênio, liberando água. A hidrazina foi usada em células de combustível fabricadas pela Allis-Chalmers Corp. , incluindo algumas que forneceram energia elétrica em satélites espaciais na década de 1960.
Uma mistura de 63% de hidrazina, 32% de nitrato de hidrazina e 5% de água é um propelente padrão para artilharia de propelente líquido experimental carregada a granel . A mistura propelente acima é uma das mais previsíveis e estáveis, com um perfil de pressão plano durante o disparo. As falhas de ignição geralmente são causadas por ignição inadequada. O movimento da carcaça após uma ignição incorreta causa uma grande bolha com uma área de superfície de ignição maior, e a maior taxa de produção de gás causa pressão muito alta, às vezes incluindo falhas catastróficas do tubo (ou seja, explosões). De janeiro a junho de 1991, o Laboratório de Pesquisa do Exército dos EUA conduziu uma revisão dos primeiros programas de armas de propelente líquido carregadas a granel para possível relevância para o programa de propulsão química eletrotérmica.
A Força Aérea dos Estados Unidos (USAF) usa regularmente H-70, uma mistura de 70% de hidrazina e 30% de água, em operações que empregam a aeronave de combate General Dynamics F-16 “Fighting Falcon” e a aeronave de reconhecimento Lockheed U-2 “Dragon Lady” . O motor a jato único F-16 utiliza hidrazina para alimentar sua Unidade de Energia de Emergência (EPU), que fornece energia elétrica e hidráulica de emergência no caso de uma falha do motor. A EPU é ativada automaticamente, ou manualmente pelo controle do piloto, em caso de perda de pressão hidráulica ou energia elétrica para fornecer controles de voo de emergência. O motor a jato único U-2 utiliza hidrazina para alimentar seu Sistema de Partida de Emergência (ESS), que fornece um método altamente confiável para reiniciar o motor em vôo em caso de estol.
Combustível de foguete
A hidrazina foi usada pela primeira vez como componente de combustíveis para foguetes durante a Segunda Guerra Mundial . Uma mistura de 30% em peso com 57% de metanol (denominada M-Stoff na Luftwaffe alemã ) e 13% de água foi denominada C-Stoff pelos alemães. A mistura foi usada para fornecer energia ao avião de combate movido a foguete Messerschmitt Me 163B , no qual o peróxido de alto teste alemão T-Stoff foi usado como oxidante. A hidrazina não misturada foi referida como B-Stoff pelos alemães, uma designação também usada mais tarde para o combustível etanol / água para o míssil V-2 .
A hidrazina é usada como um monopropelente de baixa potência para os propulsores de manobras de espaçonaves e foi usada para alimentar as unidades de energia auxiliares (APUs) do ônibus espacial . Além disso, motores de foguete monopropelentes movidos a hidrazina são freqüentemente usados na descida terminal de espaçonaves. Esses motores foram usados nos módulos de pouso do programa Viking na década de 1970, bem como nos módulos de pouso da Mars, Phoenix (maio de 2008), Curiosity (agosto de 2012) e Perseverança (fevereiro de 2021).
Em todos os motores monopropelentes de hidrazina, a hidrazina é passada sobre um catalisador , como irídio metálico suportado por alumina de alta área superficial (óxido de alumínio), o que faz com que se decomponha em amônia , nitrogênio gasoso e hidrogênio gasoso de acordo com o seguinte reações:
As duas primeiras reações são extremamente exotérmicas (a câmara do catalisador pode atingir 800 ° C em questão de milissegundos) e produzem grandes volumes de gás quente a partir de um pequeno volume de líquido, tornando a hidrazina um propelente propulsor bastante eficiente com um impulso específico de vácuo de cerca de 220 segundos. A reação 2 é a mais exotérmica, mas produz um número menor de moléculas do que a reação 1. A reação 3 é endotérmica e reverte o efeito da reação 2 de volta ao mesmo efeito da reação 1 sozinha (temperatura mais baixa, maior número de moléculas). A estrutura do catalisador afeta a proporção do NH 3 que é dissociado na reação 3; uma temperatura mais alta é desejável para propulsores de foguetes, enquanto mais moléculas são desejáveis quando as reações se destinam a produzir maiores quantidades de gás.
Como a hidrazina é um sólido abaixo de 2 ° C, ela não é adequada como propelente de foguete de uso geral para aplicações militares. Outras variantes de hidrazina que são usadas como combustível de foguete são monometilhidrazina , (CH 3 ) NH (NH 2 ), também conhecido como MMH (mp: -52 ° C), e dimetilhidrazina assimétrica , (CH 3 ) 2 N (NH 2 ) , também conhecido como UDMH (pf: -57 ° C). Esses derivados são usados em combustíveis de foguete de dois componentes, geralmente junto com o tetróxido de dinitrogênio , N 2 O 4 . Uma mistura 50:50 em peso de hidrazina e UDMA foi usada nos ICBMs Titan II e é conhecida como Aerozine 50 . Essas reações são extremamente exotérmicas e a queima também é hipergólica (começa a queimar sem qualquer ignição externa).
Existem esforços contínuos na indústria aeroespacial para substituir a hidrazina e outras substâncias altamente tóxicas. Alternativas promissoras incluem nitrato de hidroxilamônio , 2-dimetilaminoetilazida (DMAZ) e líquidos iônicos energéticos.
Riscos ocupacionais
Efeitos na saúde
As rotas potenciais de exposição à hidrazina incluem cutânea, ocular, inalação e ingestão.
A exposição à hidrazina pode causar irritação na pele / dermatite de contato e queimação, irritação nos olhos / nariz / garganta, náuseas / vômitos, falta de ar, edema pulmonar, dor de cabeça, tontura, depressão do sistema nervoso central, letargia, cegueira temporária, convulsões e coma. A exposição também pode causar danos a órgãos do fígado, rins e sistema nervoso central. A hidrazina é documentada como um forte sensibilizador da pele com potencial de sensibilização cruzada aos derivados da hidrazina após a exposição inicial. Além dos usos ocupacionais revisados acima, a exposição à hidrazina também é possível em pequenas quantidades pela fumaça do tabaco.
A orientação oficial dos EUA sobre a hidrazina como carcinógeno é mista, mas geralmente há reconhecimento de potenciais efeitos cancerígenos. O Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH) o lista como um “potencial cancerígeno ocupacional”. O Programa Nacional de Toxicologia (NTP) considera que é "razoavelmente antecipado para ser um carcinógeno humano". A Conferência Americana de Higienistas Industriais Governamentais (ACGIH) classifica a hidrazina como "A3 - cancerígeno animal confirmado com relevância desconhecida para os humanos". A Agência de Proteção Ambiental dos Estados Unidos (EPA) o classifica como "B2 - um provável cancerígeno humano com base em evidências de estudos em animais".
A Agência Internacional de Pesquisa sobre o Câncer (IARC) classifica a hidrazina como "2A - provavelmente cancerígena para humanos", com uma associação positiva observada entre a exposição à hidrazina e o câncer de pulmão. Com base em estudos de coorte e corte transversal de exposição ocupacional à hidrazina, um comitê das Academias Nacionais de Ciências , Engenharia e Medicina concluiu que há evidências sugestivas de associação entre exposição à hidrazina e câncer de pulmão, com evidência insuficiente de associação com câncer em outros sites. A Comissão Europeia ‘s Comité Científico em matéria de Limites de Exposição Ocupacional (SCOEL) coloca hidrazina em carcinógeno‘grupo B-uma substância cancerígena genotóxica’. O mecanismo genotóxico que o comitê citou faz referência à reação da hidrazina com o formaldeído endógeno e à formação de um agente de metilação do DNA.
No caso de uma emergência relacionada à exposição à hidrazina, o NIOSH recomenda remover as roupas contaminadas imediatamente, lavar a pele com água e sabão e, para exposição aos olhos, remover as lentes de contato e enxaguar os olhos com água por pelo menos 15 minutos. O NIOSH também recomenda que qualquer pessoa com potencial exposição à hidrazina busque atendimento médico o mais rápido possível. Não há recomendações específicas de laboratório pós-exposição ou de imagens médicas, e a investigação médica pode depender do tipo e da gravidade dos sintomas. A Organização Mundial da Saúde (OMS) recomenda que as exposições potenciais sejam tratadas sintomaticamente, com atenção especial aos danos potenciais aos pulmões e ao fígado. Casos anteriores de exposição à hidrazina documentaram sucesso com o tratamento com Piridoxina (Vitamina B6) .
Limites de exposição ocupacional
- Limite de exposição recomendado pelo NIOSH (REL): 0,03 ppm (0,04 mg / m 3 ) teto de 2 horas
- Limite de exposição permissível OSHA (PEL): 1 ppm (1,3 mg / m 3 ) Média ponderada do tempo de 8 horas
- Valor Limite do Limiar ACGIH (TLV): 0,01 ppm (0,013 mg / m 3 ) Média Ponderada de Tempo de 8 horas
O limite de odor para hidrazina é 3,7 ppm, portanto, se um trabalhador for capaz de cheirar um odor de amônia, é provável que ele esteja acima do limite de exposição. No entanto, esse limite de odor varia muito e não deve ser usado para determinar exposições potencialmente perigosas.
Para o pessoal aeroespacial, a USAF usa uma diretriz de exposição de emergência, desenvolvida pelo National Academy of Science Committee on Toxicology, que é utilizada para exposições não rotineiras do público em geral e é chamada de Short-Term Public Emergency Exposure Guideline (SPEGL). O SPEGL, que não se aplica a exposições ocupacionais, é definido como o pico de concentração aceitável para exposições de emergência imprevistas, únicas e de curto prazo do público em geral e representa exposições raras na vida de um trabalhador. Para a hidrazina, o SPEGL de 1 hora é 2 ppm, com um SPEGL de 24 horas de 0,08 ppm.
Manuseio e vigilância médica
Um programa completo de vigilância para hidrazina deve incluir análise sistemática de monitoramento biológico, triagem médica e informações de morbidade / mortalidade. O CDC recomenda que resumos de vigilância e educação sejam fornecidos para supervisores e trabalhadores. A pré-colocação e a triagem médica periódica devem ser conduzidas com foco específico nos efeitos potenciais da hidrazina sobre o funcionamento dos olhos, pele, fígado, rins, sistema hematopoiético, nervoso e respiratório.
Os controles comuns usados para a hidrazina incluem processo fechado, ventilação de exaustão local e equipamento de proteção individual (PPE). Diretrizes para hidrazina PPE incluem luvas e roupas não permeáveis, óculos resistentes a respingos de ventilação indireta, proteção facial e, em alguns casos, um respirador. O uso de respiradores para o manuseio da hidrazina deve ser o último recurso como método de controle da exposição do trabalhador. Nos casos em que respiradores são necessários, a seleção adequada do respirador e um programa completo de proteção respiratória consistente com as diretrizes da OSHA devem ser implementados.
Para o pessoal da USAF , o Padrão 48-8 de Segurança e Saúde Ocupacional da Força Aérea (AFOSH), Anexo 8, analisa as considerações para a exposição ocupacional à hidrazina em sistemas de mísseis, aeronaves e espaçonaves. A orientação específica para a resposta à exposição inclui chuveiros de emergência e lavatórios para os olhos obrigatórios e um processo para descontaminar as roupas de proteção. A orientação também atribui responsabilidades e requisitos para EPIs adequados, treinamento de funcionários, vigilância médica e resposta a emergências. As bases da USAF que exigem o uso de hidrazina geralmente têm regulamentos básicos específicos que regem os requisitos locais para o uso seguro de hidrazina e resposta a emergências.
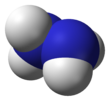
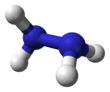
Estrutura molecular
Cada subunidade H 2 N − N é piramidal. A distância de ligação simples N − N é 1,45 Å (145 pm ), e a molécula adota uma conformação gauche . A barreira rotacional é o dobro do etano . Essas propriedades estruturais se assemelham às do peróxido de hidrogênio gasoso , que adota uma conformação anticlinal "enviesada" e também experimenta uma forte barreira rotacional.
Síntese e produção
Diversas rotas foram desenvolvidas. A etapa principal é a criação da ligação simples nitrogênio-nitrogênio. As várias rotas podem ser divididas entre aquelas que usam oxidantes de cloro (e geram sal) e aquelas que não usam.
Oxidação de amônia via oxaziridinas de peróxido
A hidrazina pode ser sintetizada a partir da amônia e do peróxido de hidrogênio com um catalisador de cetona, em um procedimento denominado processo de peróxido (às vezes denominado processo Pechiney-Ugine-Kuhlmann, ciclo Atofina-PCUK ou processo cetazina). A reação líquida segue:
Nessa rota, a cetona e a amônia primeiro se condensam para dar a imina , que é oxidada pelo peróxido de hidrogênio à oxaziridina , um anel de três membros contendo carbono, oxigênio e nitrogênio. Em seguida, a oxaziridina dá a hidrazona por tratamento com amônia , cujo processo cria a ligação simples nitrogênio-nitrogênio. Esta hidrazona se condensa com mais um equivalente de cetona.
A azina resultante é hidrolisada para dar hidrazina e regenerar a cetona, metil etil cetona :
Ao contrário da maioria dos outros processos, esta abordagem não produz um sal como subproduto.
Oxidações à base de cloro
O processo Olin Raschig , anunciado pela primeira vez em 1907, produz hidrazina a partir de hipoclorito de sódio (o ingrediente ativo em muitos alvejantes ) e amônia sem o uso de um catalisador de cetona. Este método se baseia na reação de monocloramina com amônia para criar a ligação única nitrogênio-nitrogênio, bem como um subproduto de cloreto de hidrogênio :
Relacionado ao processo Raschig, a ureia pode ser oxidada em vez da amônia. Novamente, o hipoclorito de sódio atua como oxidante. A reação líquida é mostrada:
O processo gera subprodutos significativos e é praticado principalmente na Ásia.
O processo Bayer Ketazine é o predecessor do processo de peróxido. Ele emprega hipoclorito de sódio como oxidante em vez de peróxido de hidrogênio. Como todas as rotas baseadas em hipoclorito, este método produz um equivalente de sal para cada equivalente de hidrazina.
Reações
Comportamento ácido-base
A hidrazina forma um monohidrato mais denso (1,032 g / cm 3 ) do que o material anidro . A hidrazina tem propriedades químicas básicas ( alcalinas ) comparáveis às da amônia :
(para amônia )
É difícil diprotonato:
Reações redox
O calor de combustão da hidrazina no oxigênio (ar) é 1,941 × 10 7 J / kg (8345 BTU / lb).
A hidrazina é um redutor conveniente porque os subprodutos são tipicamente nitrogênio gasoso e água. Assim, é usado como um antioxidante , um eliminador de oxigênio e um inibidor de corrosão em caldeiras de água e sistemas de aquecimento. É também usado para reduzir os sais de metais e óxidos de metais puros em electrolítico de níquel chapeamento e plutónio extracção a partir de resíduos do reactor nuclear . Alguns processos fotográficos coloridos também usam uma solução fraca de hidrazina como lavagem estabilizadora, uma vez que elimina o acoplador de tinta e haletos de prata não reagidos. A hidrazina é o agente redutor mais comum e eficaz usado para converter o óxido de grafeno (GO) em óxido de grafeno reduzido (rGO) por meio de tratamento hidrotérmico.
Sais de hidrazínio
A hidrazina pode ser monoprotonada para formar vários sais sólidos do cátion hidrazínio (N 2 H 5 + ) por tratamento com ácidos minerais. Um sal comum é o sulfato de hidrazínio , [N 2 H 5 ] HSO 4 , também chamado de sulfato de hidrazina. O sulfato de hidrazina foi investigado como tratamento da caquexia induzida pelo câncer , mas se mostrou ineficaz.
A protonação dupla dá a dicação de hidrazínio (H 3 NNH 3 2+ ), da qual vários sais são conhecidos.
Química orgânica
As hidrazinas são parte de muitas sínteses orgânicas , frequentemente aquelas de significado prático em produtos farmacêuticos (consulte a seção de aplicações), bem como em tinturas têxteis e em fotografia.
A hidrazina é usada na redução de Wolff-Kishner , uma reação que transforma o grupo carbonil de uma cetona em uma ponte de metileno (ou um aldeído em um grupo metil ) por meio de um intermediário de hidrazona . A produção do dinitrogênio altamente estável a partir do derivado da hidrazina ajuda a impulsionar a reação.
Sendo bifuncional, com duas aminas, a hidrazina é um bloco de construção chave para a preparação de muitos compostos heterocíclicos por condensação com uma variedade de eletrófilos difuncionais . Com 2,4-pentanodiona , ele se condensa para dar o 3,5-dimetilpirazol . Na reação de Einhorn-Brunner, as hidrazinas reagem com as imidas para dar triazóis .
Por ser um bom nucleófilo, o N 2 H 4 pode atacar haletos de sulfonila e haletos de acila. A tosilhidrazina também forma hidrazonas após tratamento com carbonilas.
A hidrazina é usada para clivar derivados de ftalimida N- alquilados. Esta reação de cisão permite que o ânion ftalimida seja usado como precursor da amina na síntese de Gabriel .
Formação de hidrazona
Ilustrativo da condensação de hidrazina com um carbonil simples é sua reação com propanona para dar a diisopropilideno hidrazina (acetona azina). Este último reage ainda mais com a hidrazina para produzir a hidrazona:
A propanona azina é um intermediário no processo Atofina-PCUK . A alquilação direta de hidrazinas com halogenetos de alquila na presença de base produz hidrazinas substituídas com alquil, mas a reação é tipicamente ineficiente devido ao controle deficiente do nível de substituição (o mesmo que nas aminas comuns ). A redução de hidrazonas a hidrazinas apresenta uma maneira limpa de produzir hidrazinas 1,1-dialquiladas.
Em uma reação relacionada, 2-cianopiridinas reagem com hidrazina para formar hidrazidas de amida, que podem ser convertidas usando 1,2-dicetonas em triazinas .
Bioquímica
A hidrazina é o intermediário no processo de oxidação anaeróbia da amônia ( anammox ). É produzido por algumas leveduras e pela bactéria anammox de oceano aberto ( Brocadia anammoxidans ). O falso morel produz o veneno giromitrina, um derivado orgânico da hidrazina, que é convertido em monometilhidrazina por processos metabólicos. Até mesmo o cogumelo "botão" comestível mais popular, Agaricus bisporus, produz derivados orgânicos de hidrazina, incluindo agaritina , um derivado de hidrazina de um aminoácido, e giromitrina .
História
O nome "hidrazina" foi cunhado por Emil Fischer em 1875; ele estava tentando produzir compostos orgânicos que consistiam em hidrazina monossubstituída. Em 1887, Theodor Curtius havia produzido sulfato de hidrazina tratando diazidas orgânicas com ácido sulfúrico diluído; no entanto, ele não conseguiu obter hidrazina pura, apesar dos esforços repetidos. A hidrazina anidra pura foi preparada pela primeira vez pelo químico holandês Lobry de Bruyn em 1895.
Veja também
- Diazene
- Sulfato de hidrazina
- Lista de Stoffs
- Mistura de combustível de óxido nitroso - Classe de propelentes de foguete líquidos
- EUA 193













![{\ displaystyle {\ ce {N2H4 + H2O -> [N2H5] ^ + + OH-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ef02d7cc8519ded31bae36408d7f1461c64195b7)


![{\ displaystyle {\ ce {[N2H5] + + H2O -> [N2H6] ^ 2 + + OH-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/58d05df88d00c82f17bb6b59cf2a7d07696dc980)

![{\ displaystyle {\ ce {2 (CH3) 2CO + N2H4 -> 2 H2O + [(CH3) 2C = N] 2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8036d601adcf4a13ee6b912eb05bc55994ab952a)
![{\ displaystyle {\ ce {[(CH3) 2C = N] 2 + N2H4 -> 2 (CH3) 2C = NNH2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/183b956f5ae1e22d5ada6e751b42ace50f85e25d)