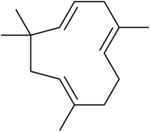
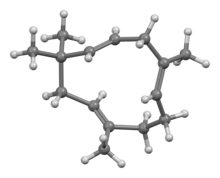
Humulene - Humulene
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
(1 E , 4 E , 8 E ) -2,6,6,9-Tetrametilcicloundeca-1,4-8-trieno |
|
| Outros nomes
alfa-cariofileno; 3,7,10-Humulatriene
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.027.106 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 15 H 24 | |
| Massa molar | 204,357 g · mol −1 |
| Aparência | Líquido claro verde amarelado pálido |
| Densidade | 0,886 g / cm 3 |
| Ponto de fusão | <25 ° C (77 ° F; 298 K) |
| Ponto de ebulição | 106 a 107 ° C (223 a 225 ° F; 379 a 380 K) a 5 mmHg |
| Perigos | |
| Ficha de dados de segurança | MSDS |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
> 48 mg / kg |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Humulene , também conhecido como α-humuleno ou α-cariofileno , é um sesquiterpeno monocíclico de ocorrência natural (C 15 H 24 ), contendo um anel de 11 membros e consistindo em 3 unidades de isopreno contendo três ligações duplas C = C não conjugadas, duas delas sendo triplamente substituído e um sendo duplamente substituído. Foi encontrado pela primeira vez nos óleos essenciais de Humulus lupulus ( lúpulo ), de onde deriva o seu nome. Humulene é um isômero de β-cariofileno , e os dois são freqüentemente encontrados juntos como uma mistura em muitas plantas aromáticas.
Ocorrência
Humulene é um dos componentes do óleo essencial da pinha do lúpulo, Humulus lupulus , da qual deriva o seu nome. A concentração de humulene varia entre as diferentes variedades da planta, mas pode chegar a 40% do óleo essencial. O Humulene e seus produtos de reação no processo de fabricação da cerveja conferem a muitas cervejas seu aroma “lúpulo”. Descobriu-se que as variedades de lúpulo nobre apresentam níveis mais elevados de humuleno, enquanto outras variedades de lúpulo amargo contêm níveis baixos. Vários epóxidos de humuleno são produzidos no processo de fermentação. Em um estudo científico envolvendo análise de cromatografia gasosa-espectrometria de massa de amostras e um painel sensorial treinado, descobriu-se que os produtos da hidrólise do epóxido de humuleno II produzem especificamente um aroma de “lúpulo” na cerveja.
O α-Humulene foi encontrado em muitas plantas aromáticas em todos os continentes, frequentemente junto com seu isômero β-cariofileno. Os emissores de α-humuleno comprovados na atmosfera são pinheiros, pomares de laranja, anciãos de pântano , tabaco e campos de girassol. α-Humulene está contido nos óleos essenciais de plantas aromáticas, como Salvia officinalis (sálvia comum, sálvia culinária), Lindera strychnifolia Uyaku ou erva-doce japonesa, espécie de ginseng , até 29,9% dos óleos essenciais de Mentha spicata , a família do gengibre ( Zingiberaceae), 10% do óleo da folha de Litsea mushaensis , loureiro chinês, 4% do extrato da folha de Cordia verbenacea , um arbusto da costa tropical da América do Sul (erva baleeira), mas com 25% de trans- cariofileno e é um dos compostos químicos que contribuem para o sabor da especiaria Persicaria odorata ou coentro vietnamita e o aroma característico da Cannabis .
Preparação e síntese
Humulene é um dos muitos sesquiterpenóides derivados do difosfato de farnesil (FPP). A formação de humuleno a partir de FPP é catalisada por enzimas de síntese de sesquiterpeno.
Esta biossíntese pode ser imitada em laboratório pela preparação de estanano alílico a partir do farnesol, denominado síntese de Corey. Existem diversas maneiras de sintetizar humuleno em laboratório, envolvendo diferentes fechamentos da ligação CC no macrociclo. A síntese de McMurry usa uma reação de acoplamento de carbonila catalisada por titânio; a síntese de Takahashi usa alquilação intramolecular de um haleto de alila por um ânion cianoidrina protegido; a síntese de Suginome utiliza um fragmento de geranil; e a síntese de Groot sintetiza humuleno a partir de um destilado bruto de óleo de eucalipto. Humulene também pode ser sintetizado usando uma combinação de montagem de quatro componentes e ciclização mediada por paládio, descrita abaixo. Esta síntese é notável pela simplicidade das construções da ligação C − C e etapas de ciclização, que se acredita serão vantajosas na síntese de politerpenóides relacionados.
Para entender a regiosseletividade do humulene, o fato de que uma das duas ligações duplas C═C triplamente substituídas é significativamente mais reativa, seu espaço conformacional foi explorado computacionalmente e quatro conformações diferentes foram identificadas.
Pesquisar
Em estudos de laboratório, o humulene está sendo estudado para potenciais efeitos antiinflamatórios .
Em 2015, pesquisadores no Brasil identificaram o α-Humulene como um contribuinte ativo para as propriedades repelentes de insetos do óleo da folha de commiphora leptophloeos , especificamente contra “o mosquito da febre amarela”, Aedes aegypti .
Química atmosférica
α-Humulene é um composto orgânico volátil biogênico , emitido por numerosas plantas (ver ocorrência) com um potencial relativamente alto para formação de aerossol orgânico secundário na atmosfera. Ele reage rapidamente com o ozônio na luz solar (fotooxidação) para formar produtos oxigenados. α-Humulene tem um coeficiente de taxa de reação muito alto (1,17 × 10 −14 cm 3 molécula −1 s −1 ) em comparação com a maioria dos monoterpenos. Uma vez que contém três ligações duplas, são possíveis produtos de primeira, segunda e terceira geração, que podem se condensar para formar um aerossol orgânico secundário. Em proporções de mistura de ozônio troposférico típicas de 30 ppb, o tempo de vida do α-humuleno é de cerca de 2 minutos, enquanto os produtos de primeira e segunda geração têm tempos de vida médios de 1 he 12,5 h, respectivamente.


