Vírus linfotrópico T humano - Human T-lymphotropic virus
| Vírus linfotrópico T humano | |
|---|---|

|
|
| uma micrografia mostrando o vírus T-linfotrópico humano 1 e HIV | |
|
Classificação científica |
|
| (não classificado): | Vírus |
| Reino : | Riboviria |
| Reino: | Pararnavirae |
| Filo: | Artverviricota |
| Classe: | Revtraviricetes |
| Pedido: | Ortervirales |
| Família: | Retroviridae |
| Subfamília: | Orthoretrovirinae |
| Gênero: | Deltaretrovirus |
| Grupos incluídos | |
| Táxons cladisticamente incluídos, mas tradicionalmente excluídos | |
O vírus linfotrópico T humano , o vírus linfotrópico de células T humanas ou a família de vírus do vírus da leucemia-linfoma de células T humanas ( HTLV ) são um grupo de retrovírus humanos que são conhecidos por causar um tipo de câncer chamado leucemia de células T adultas / linfoma e uma doença desmielinizante chamada mielopatia associada ao HTLV-1 / paraparesia espástica tropical ( HAM / TSP ). Os HTLVs pertencem a um grupo maior de vírus linfotrópicos T de primatas ( PTLVs ). Os membros dessa família que infectam humanos são chamados de HTLVs, e os que infectam macacos do Velho Mundo são chamados de vírus linfotrópicos T dos símios (STLVs). Até o momento, quatro tipos de HTLVs ( HTLV-1 , HTLV-2 , HTLV-3 e HTLV-4) e quatro tipos de STLVs (STLV-1, STLV-2, STLV-3 e STLV-5) foram identificado. Os vírus HTLV tipos HTLV-1 e HTLV-2 são os primeiros retrovírus descobertos. Ambos pertencem à subfamília dos retrovírus oncovírus e podem transformar linfócitos humanos de modo que sejam autossustentáveis in vitro. Acredita-se que os HTLVs se originem da transmissão entre espécies de STLVs. O genoma do HTLV-1 é diplóide, composto por duas cópias de um vírus de RNA de fita simples cujo genoma é copiado em uma forma de DNA de fita dupla que se integra ao genoma da célula hospedeira , ponto em que o vírus é referido como um provírus . Um vírus intimamente relacionado é o vírus da leucemia bovina BLV . O nome original do HIV , o vírus que causa a AIDS , era HTLV-3.
HTLV-1
HTLV-1 é uma abreviatura para vírus linfotrópico de células T humanas tipo 1 , também chamado de leucemia de células T humanas tipo 1, um vírus que tem sido implicado em vários tipos de doenças, incluindo paraparesia espástica tropical , e como uma ligação do câncer de vírus para leucemia (ver leucemia / linfoma de células T do adulto ). O HTLV-1 tem sete subtipos relatados (subtipos A a G). A grande maioria das infecções é causada pelo cosmopolita subtipo A. O HTLV foi descoberto por Robert Gallo e colegas em 1980. Acredita-se que entre 1 em 20 e 1 em 25 pessoas infectadas desenvolvam câncer como resultado do vírus. Acredita-se que a infecção por HTLV-1 se espalhe apenas por células em divisão, uma vez que a transcriptase reversa gera DNA proviral a partir do RNA viral genômico, e o provírus é integrado ao genoma do hospedeiro pela integrase viral após a transmissão. Portanto, a quantificação do provírus reflete o número de células infectadas pelo HTLV-1. Assim, um aumento no número de células infectadas pelo HTLV-1 usando a divisão celular, por ações de genes virais acessórios, especialmente Tax, pode fornecer um aumento da infectividade. A expressão de tax induz proliferação, inibe a apoptose de células infectadas com HTLV-1 e, inversamente, evoca a resposta imune do hospedeiro, incluindo células T citotóxicas, para matar células infectadas por vírus.

HTLV-2
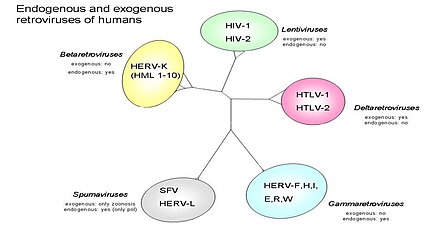
Um vírus intimamente relacionado ao HTLV-1, também descoberto por Robert Gallo e colegas. A família do vírus linfotrópico T humano (Figura 2) pode ser ainda categorizada em quatro subtipos. A figura também divide os retrovírus em exógenos e endógenos. Os retrovírus podem existir em duas formas diferentes: endógenos, que consistem em componentes genéticos normais, e exógenos, que são componentes genéticos transferidos horizontalmente, que geralmente são agentes infecciosos que causam doenças, por exemplo, HIV . Na (Figura 3) quadros de leitura aberta (ORF) são mostrados que podem, se traduzidos, prever quais genes estarão presentes e isso pode ajudar a entender melhor os retrovírus humanos. Dos quatro subtipos, o HTLV-2 pode estar ligado ao linfoma cutâneo de células T (CTCL). Em um estudo envolvendo cultura de linfócitos de pacientes com micose fungóide (Figura 1), a amplificação por PCR mostrou sequências gênicas de HTLV-II. Esse achado pode sugerir uma possível correlação com HTLV-2 e CTCL. Mais pesquisas e estudos devem ser realizados para mostrar uma relação positiva.
HTLV-3 e HTLV-4
HTLV-3 e HTLV-4 têm sido usados para descrever vírus recentemente caracterizados. Esses vírus foram descobertos em 2005 na zona rural dos Camarões e, presume-se, foram transmitidos de macacos para caçadores de macacos por meio de mordidas e arranhões.
- O HTLV-3 é semelhante ao STLV-3 ( vírus Simian T-lympotropic 3 ). Várias cepas foram identificadas. Ele expressa gag , pol e env , entre outras proteínas.
- O HTLV-4 é aparentemente substancialmente idêntico ao STLV-4 hospedado em gorilas.
Ainda não se sabe quantas outras transmissões ocorreram entre humanos, ou se os vírus podem causar doenças.
O uso desses nomes pode causar alguma confusão, porque o nome HTLV-3 era um dos nomes para HIV na literatura sobre a AIDS , mas desde então caiu em desuso. O nome HTLV-4 também foi usado para descrever o HIV-2 . Um grande estudo canadense documentou essa confusão entre os profissionais de saúde, onde> 90% dos testes de HTLV solicitados por médicos tinham a intenção de ser testes de HIV.

Transmissão
O HTLV-1 e o HTLV-2 podem ser transmitidos sexualmente , por contato de sangue com sangue (por exemplo, por transfusão de sangue ou compartilhamento de agulhas ao usar drogas) e por meio da amamentação .
Epidemiologia
Dois HTLVs estão bem estabelecidos. O HTLV-1 e o HTLV-2 estão envolvidos na propagação ativa de epidemias, afetando de 15 a 20 milhões de pessoas em todo o mundo.
O HTLV-1 é o mais clinicamente significativo dos dois: pelo menos 500.000 dos indivíduos infectados com HTLV-1 eventualmente desenvolvem uma leucemia frequentemente fatal , enquanto outros desenvolverão uma mielopatia debilitativa , e outros ainda sofrerão uveíte , dermatite infecciosa ou outro distúrbio inflamatório. O HTLV-2 está associado a distúrbios neurológicos mais brandos e infecções pulmonares crônicas . Nos Estados Unidos, as taxas de soroprevalência do HTLV-1/2 entre doadores de sangue voluntários são em média 0,016%.
Nenhuma doença específica foi ainda associada ao HTLV-3 e ao HTLV-4 .
Vacinação e tratamentos
Embora não haja uma vacina licenciada no momento, há muitos fatores que tornam viável uma vacina contra o HTLV-1. O vírus exibe uma variabilidade antigênica relativamente baixa, a imunidade natural ocorre em humanos e a vacinação experimental usando antígenos de envelope mostrou ser bem-sucedida em modelos animais. As vacinas de DNA de plasmídeo provocam respostas imunes potentes e protetoras em vários modelos de pequenos animais de doenças infecciosas. No entanto, sua imunogenicidade em primatas parece menos potente. Nas últimas duas décadas, uma grande iniciativa foi lançada para entender as propriedades biológicas e patogênicas do vírus linfotrópico de células T humanas tipo 1 (HTLV-1); em última análise, isso levou ao desenvolvimento de várias vacinas experimentais e estratégias terapêuticas para combater a infecção pelo HTLV-1. Essas estratégias incluem o desenvolvimento de epítopos de células B derivados da glicoproteína do envelope para a indução de anticorpos neutralizantes, bem como uma estratégia para gerar uma resposta de linfócitos T citotóxicos multivalentes (CTL) contra o antígeno Tax do HTLV-1. Uma vacina candidata que pode induzir ou aumentar a resposta do anticorpo neutralizante anti-gp46 pode ter potencial para prevenção e terapia contra a infecção por HTLV-1.
Os tratamentos potenciais incluem prosultiamina , um derivado da vitamina B-1, que demonstrou reduzir a carga viral e os sintomas; azacitidina , um antimetabólito, que foi creditado com a cura de um paciente na Grécia; tenofovir disoproxil (TDF), um inibidor da transcriptase reversa usado para o HIV; cefarantina , um alcalóide de stephania cepharantha hayata; e nucleósidos 2'-oxa-3'aza carbocíclicos fosfonados (PCOANs). Uma formulação mais recente de TDF, chamada tenofovir alafenamida (TAF), também é promissora como um tratamento com menos toxicidade.
Referências
links externos
- vírus linfotrófico de células T humanas na eMedicine
- Associação Internacional de Retrovirologia
- Humano + T-linfotrópico + vírus + 1 na Biblioteca Nacional de Medicina dos EUA Medical Subject Headings (MeSH)
- Humano + T-linfotrópico + vírus + 2 na Biblioteca Nacional de Medicina dos EUA Medical Subject Headings (MeSH)
- " Vírus linfotrópico T humano 1 " . Navegador de taxonomia NCBI . 11908.
- " Vírus linfotrópico T humano 2 " . Navegador de taxonomia NCBI . 11909.
- " Vírus linfotrópico T humano 3 " . Navegador de taxonomia NCBI . 28332.
- " Vírus linfotrópico T humano 4 " . Navegador de taxonomia NCBI . 318279.
- " Vírus linfotrópico T humano não tipado " . Navegador de taxonomia NCBI . 318275.