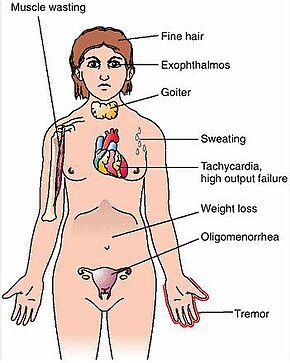
Doença de Graves - Graves' disease
| Doença de Graves | |
|---|---|
| Outros nomes | Bócio difuso tóxico, doença de Flajani – Basedow – Graves |
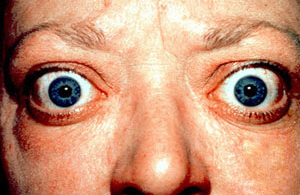 | |
| O achado clássico de exoftalmia e retração da pálpebra na doença de Graves | |
| Especialidade | Endocrinologia |
| Sintomas | Tireóide aumentada , irritabilidade, fraqueza muscular, problemas de sono, batimento cardíaco acelerado , perda de peso, baixa tolerância ao calor |
| Complicações | Oftalmopatia de Graves |
| Causas | Desconhecido |
| Fatores de risco | História familiar, outras doenças autoimunes |
| Método de diagnóstico | Exames de sangue, captação de radioiodo |
| Tratamento | Terapia de radioiodo , medicamentos, cirurgia da tireoide |
| Frequência | 0,5% (homens), 3% (mulheres) |
A doença de Graves , também conhecida como bócio difuso tóxico , é uma doença auto - imune que afeta a tireóide . Freqüentemente resulta e é a causa mais comum de hipertireoidismo . Freqüentemente, também resulta em aumento da tireoide . Os sinais e sintomas de hipertireoidismo podem incluir irritabilidade, fraqueza muscular , problemas de sono , batimento cardíaco acelerado , baixa tolerância ao calor, diarréia e perda de peso não intencional. Outros sintomas podem incluir espessamento da pele nas canelas, conhecido como mixedema pré-tibial , e olhos esbugalhados , uma condição causada pela oftalmopatia de Graves . Cerca de 25 a 80% das pessoas com a doença desenvolvem problemas nos olhos.
A causa exata da doença não é clara; no entanto, acredita-se que envolva uma combinação de fatores genéticos e ambientais. Uma pessoa tem maior probabilidade de ser afetada se tiver um membro da família com a doença. Se um dos gêmeos for afetado, existe uma chance de 30% de que o outro gêmeo também tenha a doença. O início da doença pode ser desencadeado por estresse físico ou emocional, infecção ou parto . Pessoas com outras doenças autoimunes, como diabetes tipo 1 e artrite reumatóide, têm maior probabilidade de serem afetadas. Fumar aumenta o risco de doenças e pode piorar os problemas oculares. O distúrbio resulta de um anticorpo , denominado imunoglobulina estimuladora da tireoide (TSI), que tem um efeito semelhante ao do hormônio estimulador da tireoide (TSH). Esses anticorpos TSI fazem com que a glândula tireóide produza hormônios tireoidianos em excesso . O diagnóstico pode ser suspeitado com base nos sintomas e confirmado com exames de sangue e captação de radioiodo . Normalmente, os exames de sangue mostram T 3 e T 4 elevados , TSH baixo, captação aumentada de radioiodo em todas as áreas da tireoide e anticorpos TSI.
As três opções de tratamento são radioiodoterapia , medicamentos e cirurgia da tireoide . A terapia com radioiodo envolve a ingestão de iodo-131 por via oral, que é então concentrada na tireoide e a destrói ao longo de semanas a meses. O hipotireoidismo resultante é tratado com hormônios tireoidianos sintéticos . Medicamentos como betabloqueadores podem controlar alguns dos sintomas, e medicamentos antitireoidianos , como metimazol, podem ajudar temporariamente as pessoas enquanto outros tratamentos fazem efeito. A cirurgia para remover a tireoide é outra opção. Problemas oculares podem exigir tratamentos adicionais.
A doença de Graves se desenvolverá em cerca de 0,5% dos homens e 3% das mulheres. Ocorre cerca de 7,5 vezes mais frequentemente em mulheres do que em homens. Freqüentemente, começa entre as idades de 40 e 60, mas pode começar em qualquer idade. É a causa mais comum de hipertireoidismo nos Estados Unidos (cerca de 50 a 80% dos casos). A condição tem o nome do cirurgião irlandês Robert Graves , que a descreveu em 1835. Também existem várias descrições anteriores.
sinais e sintomas
Os sinais e sintomas da doença de Graves resultam virtualmente dos efeitos diretos e indiretos do hipertireoidismo, com as principais exceções sendo a oftalmopatia de Graves , bócio e mixedema pré - tibial (que são causados pelos processos autoimunes da doença). Os sintomas do hipertireoidismo resultante são principalmente insônia , tremor das mãos , hiperatividade , queda de cabelo, sudorese excessiva , oligomenorréia , coceira, intolerância ao calor, perda de peso apesar do aumento do apetite , diarreia , defecação frequente , palpitações , fraqueza muscular parcial periódica ou paralisia naqueles especialmente de Descendência asiática e calor e umidade da pele. Outros sinais que podem ser vistos no exame físico são mais comumente um difusamente alargada (geralmente simétrica), nontender tiróide, atraso tampa , excessiva lacrimação devido a oftalmopatia de Graves, arritmias do coração, tal como taquicardia sinusal , fibrilação atrial , e ventricular prematura contrações e hipertensão . Pessoas com hipertireoidismo podem apresentar mudanças comportamentais e de personalidade, incluindo psicose , mania , ansiedade , agitação e depressão .
Causa
A causa exata não é clara; no entanto, acredita-se que envolva uma combinação de fatores genéticos e ambientais. Embora ocorra um mecanismo teórico pelo qual a exposição a estressores graves e altos níveis de sofrimento subsequente, como PTSD (transtorno de estresse pós-traumático), pode aumentar o risco de doença autoimune e causar um agravamento da resposta autoimune que leva à doença de Graves, mais robusto dados clínicos são necessários para uma conclusão firme.
Genética
Uma predisposição genética para a doença de Graves é observada, com algumas pessoas mais propensas a desenvolver anticorpos ativadores do receptor de TSH devido a uma causa genética. O antígeno leucocitário humano DR (especialmente DR3) parece desempenhar um papel. Até o momento, nenhum defeito genético claro foi encontrado para apontar para uma causa de um único gene .
Os genes que se acredita estar envolvida incluem aqueles para tiroglobulina , receptor de tirotrofina , proteína tirosina fosfatase nonreceptor tipo 22 , e citotóxicas antigénio do linfócito T-4 associada , entre outros.
Gatilho infeccioso
Uma vez que a doença de Graves é uma doença autoimune que surge repentinamente, freqüentemente mais tarde na vida, uma infecção viral ou bacteriana pode desencadear anticorpos que apresentam reação cruzada com o receptor humano de TSH, um fenômeno conhecido como mimetismo antigênico .
A bactéria Yersinia enterocolitica apresenta semelhança estrutural com o receptor de tireotropina humano e foi considerada como contribuindo para o desenvolvimento da autoimunidade tireoidiana por outras razões em indivíduos geneticamente suscetíveis. Na década de 1990, foi sugerido que Y. enterocolitica pode estar associada à doença de Graves. Mais recentemente, o papel de Y. enterocolitica foi disputado.
O vírus Epstein-Barr (EBV) é outro gatilho potencial.
Mecanismo
As imunoglobulinas estimuladoras da tireoide reconhecem e se ligam ao receptor de tireotropina ( receptor de TSH), que estimula a secreção de tiroxina (T4) e triiodotironina (T3). Os receptores de tiroxina na glândula pituitária são ativados pelo hormônio excedente, suprimindo a liberação adicional de TSH em um ciclo de feedback negativo. O resultado são níveis muito altos de hormônios tireoidianos circulantes e um nível baixo de TSH.
Fisiopatologia
A doença de Graves é uma doença auto - imune , na qual o corpo produz anticorpos que são específicos para uma auto-proteína : o receptor do hormônio estimulador da tireoide. (Anticorpos para a tireoglobulina e para os hormônios tireoidianos T3 e T4 também podem ser produzidos.)
Esses anticorpos causam hipertireoidismo porque se ligam ao TSHr e o estimulam cronicamente . O TSHr é expresso nas células foliculares da tireoide da glândula tireoide (as células que produzem o hormônio tireoidiano) e o resultado da estimulação crônica é uma produção anormalmente alta de T3 e T4. Isso, por sua vez, causa os sintomas clínicos de hipertireoidismo e o aumento da glândula tireoide visível como bócio.
A exoftalmia infiltrativa freqüentemente encontrada foi explicada pela postulação de que a glândula tireóide e os músculos extraoculares compartilham um antígeno comum que é reconhecido pelos anticorpos. Os anticorpos que se ligam aos músculos extraoculares podem causar inchaço atrás do globo ocular.
A "casca de laranja" da pele tem sido explicada pela infiltração de anticorpos sob a pele, causando uma reação inflamatória e subsequentes placas fibrosas.
Os três tipos de autoanticorpos para o receptor de TSH atualmente reconhecidos são:
- Imunoglobulinas estimuladoras da tireoide: esses anticorpos (principalmente IgG) atuam como estimulantes da tireoide de ação prolongada , ativando as células por meio de um processo mais lento e prolongado em comparação com o TSH, levando a uma produção elevada de hormônio da tireoide.
- Imunoglobulinas de crescimento da tireoide: esses anticorpos se ligam diretamente ao receptor de TSH e têm sido implicados no crescimento dos folículos da tireoide.
-
Imunoglobulinas inibidoras da ligação da tireotrofina: esses anticorpos inibem a união normal do TSH com seu receptor.
- Alguns realmente agem como se o próprio TSH estivesse se ligando ao seu receptor, induzindo assim a função da tireoide.
- Outros tipos podem não estimular a glândula tireóide, mas impedem que o TSI e o TSH se liguem e estimulem o receptor.
Outro efeito do hipertireoidismo é a perda óssea decorrente da osteoporose, causada por um aumento da excreção de cálcio e fósforo na urina e nas fezes. Os efeitos podem ser minimizados se o hipertireoidismo for tratado precocemente. A tireotoxicose também pode aumentar os níveis de cálcio no sangue em até 25%. Isso pode causar dores de estômago, micção excessiva e função renal prejudicada.
Diagnóstico
A doença de Graves pode se manifestar clinicamente com um ou mais destes sinais característicos:
- Batimento cardíaco rápido (80%)
- Bócio difuso palpável com sopro audível (70%)
- Tremor (40%)
- Exoftalmia (protuberância de um ou ambos os olhos), edema periorbital (25%)
- Fadiga (70%), perda de peso (60%) com aumento do apetite em jovens e falta de apetite em idosos e outros sintomas de hipertireoidismo / tireotoxicose
- Intolerância ao calor (55%)
- Tremores (55%)
- Palpitações (50%)
Dois sinais são verdadeiramente "diagnósticos" da doença de Graves (ou seja, não vistos em outras condições hipertireoidianas): exoftalmia e edema sem depressões ( mixedema pré-tibial ). Bócio é uma glândula tireoide aumentada e é do tipo difuso (ou seja, espalhado por toda a glândula). O bócio difuso pode ser observado com outras causas de hipertireoidismo, embora a doença de Graves seja a causa mais comum de bócio difuso. Um bócio grande será visível a olho nu, mas um pequeno (aumento moderado da glândula) pode ser detectado apenas pelo exame físico. Ocasionalmente, o bócio não é clinicamente detectável, mas pode ser observado apenas com tomografia computadorizada ou exame de ultrassom da tireoide.
Outro sinal da doença de Graves é hipertireoidismo; ou seja, superprodução dos hormônios tireoidianos T3 e T4. Também são observados níveis normais de tireoide e, ocasionalmente , hipotireoidismo , que pode ajudar a causar bócio (embora não seja a causa da doença de Graves). O hipertireoidismo na doença de Graves é confirmado, como em qualquer outra causa de hipertireoidismo, pela medição dos níveis sanguíneos elevados de T3 e T4 livres (não ligados).
Outras medições laboratoriais úteis na doença de Graves incluem o hormônio estimulador da tireoide (TSH, geralmente indetectável na doença de Graves devido ao feedback negativo de T3 e T4 elevados) e iodo ligado à proteína (elevado). Anticorpos estimuladores da tireoide detectados sorologicamente , captação de iodo radioativo (RAI) ou ultrassonografia da tireoide com Doppler, todos podem confirmar independentemente um diagnóstico de doença de Graves.
A biópsia para obter o teste histiológico normalmente não é necessária, mas pode ser obtida se a tireoidectomia for realizada.
O bócio na doença de Graves geralmente não é nodular, mas os nódulos da tireoide também são comuns. Diferenciar formas comuns de hipertireoidismo, como doença de Graves, adenoma único da tireoide e bócio multinodular tóxico, é importante para determinar o tratamento adequado. A diferenciação entre essas entidades tem avançado , à medida que os exames de imagem e bioquímicos melhoram. Medir os anticorpos do receptor de TSH com o ensaio h-TBII provou ser eficiente e foi a abordagem mais prática encontrada em um estudo.
Doença ocular
A oftalmopatia associada à tireoide (TAO), ou doença ocular da tireoide (TED), é a manifestação extratireoidiana mais comum da doença de Graves. É uma forma de inflamação linfocítica orbital idiopática e, embora sua patogênese não seja completamente compreendida, acredita-se que a ativação autoimune de fibroblastos orbitais , que no TAO expressam o receptor de TSH , desempenhe um papel central.
A hipertrofia dos músculos extraoculares, adipogênese e deposição de glicoaminoglicanos não sulfatados e hialuronato, causa expansão da gordura orbital e dos compartimentos musculares, que dentro dos limites da órbita óssea podem levar a neuropatia óptica distireoidiana , aumento das pressões intraoculares , proptose, congestão venosa levando a quemose e edema periorbital e remodelação progressiva das paredes orbitárias. Outras características distintivas do TAO incluem retração da pálpebra, miopatia restritiva, ceratoconjuntivite límbica superior e ceratopatia de exposição .
A gravidade da doença ocular pode ser classificada pelo mnemônico: "SEM ESPECIFICAÇÕES":
- Classe 0: Sem sinais ou sintomas
- Classe 1: Apenas sinais (limitado a retração da pálpebra superior e olhar fixo, com ou sem retardo de pálpebra)
- Classe 2: envolvimento de tecidos moles ( edema de conjuntiva e pálpebras, injeção conjuntival, etc.)
- Classe 3: Proptose
- Classe 4: envolvimento do músculo extraocular (geralmente com diplopia )
- Classe 5: envolvimento da córnea (principalmente devido ao lagoftalmo )
- Classe 6: perda de visão (devido ao envolvimento do nervo óptico)
Normalmente, a história natural do TAO segue a curva de Rundle, que descreve uma rápida piora durante uma fase inicial, até um pico de gravidade máxima e, em seguida, melhora para um platô estático sem, no entanto, retornar à condição normal.
Gestão
O tratamento da doença de Graves inclui medicamentos antitireoidianos que reduzem a produção do hormônio tireoidiano; radioiodo (iodo radioativo I-131 ); e tireoidectomia (excisão cirúrgica da glândula). Como operar um paciente com hipertireoidismo é perigoso, antes da tireoidectomia, o tratamento pré-operatório com medicamentos antitireoidianos é administrado para tornar o paciente "eutireoidiano" (isto é, normotireoidiano). Cada um desses tratamentos tem vantagens e desvantagens. Nenhuma abordagem de tratamento é considerada a melhor para todos.
O tratamento com medicamentos antitireoidianos deve ser administrado por seis meses a dois anos para ser eficaz. Mesmo assim, após a interrupção dos medicamentos, o estado de hipertireoidismo pode reaparecer. O risco de recorrência é de cerca de 40–50%, e o tratamento vitalício com medicamentos antitireoidianos traz alguns efeitos colaterais, como agranulocitose e doença hepática. Os efeitos colaterais dos medicamentos antitireoidianos incluem uma redução potencialmente fatal no nível de glóbulos brancos. A terapia com radioiodo é o tratamento mais comum nos Estados Unidos, enquanto os medicamentos antitireoidianos e / ou tireoidectomia são usados com mais frequência na Europa, no Japão e na maior parte do resto do mundo.
Os β-bloqueadores (como o propranolol ) podem ser usados para inibir os sintomas do sistema nervoso simpático de taquicardia e náusea até o momento em que os tratamentos antitireoidianos comecem a fazer efeito. Os β-bloqueadores puros não inibem a retração da pálpebra nos olhos, que é mediada por receptores alfa adrenérgicos.
Drogas antitireoidianas
Os principais medicamentos antitireoidianos são o carbimazol (no Reino Unido), o metimazol (nos EUA) e o propiltiouracil / PTU. Essas drogas bloqueiam a ligação do iodo e o acoplamento das iodotirosinas. O efeito colateral mais perigoso é a agranulocitose (1/250, mais no PTU). Outros incluem granulocitopenia (dependente da dose, que melhora com a cessação do medicamento) e anemia aplástica . Os pacientes que tomam esses medicamentos devem consultar um médico se desenvolverem dor de garganta ou febre. Os efeitos colaterais mais comuns são erupção cutânea e neurite periférica. Essas drogas também atravessam a placenta e são secretadas no leite materno. O iodo de Lugol pode ser usado para bloquear a síntese hormonal antes da cirurgia.
Um ensaio clínico randomizado testando o tratamento de dose única para Graves descobriu que o metimazol atingiu o estado eutireoidiano de forma mais eficaz após 12 semanas do que o propiltyouracil (77,1% com metimazol 15 mg vs 19,4% nos grupos de propiltiouracil 150 mg).
Nenhuma diferença no resultado foi mostrada para adicionar tiroxina à medicação antitireoidiana e continuar a tiroxina versus placebo após a retirada da medicação antitireoidiana. No entanto, foram encontrados dois marcadores que podem ajudar a prever o risco de recorrência. Estes dois marcadores são um positivo TSHR anticorpo (TSHR-Ab) e de fumar. Um TSHR-Ab positivo no final do tratamento com drogas antitireoidianas aumenta o risco de recorrência em 90% ( sensibilidade 39%, especificidade 98%), um TSHR-Ab negativo no final do tratamento com drogas antitireoidianas está associado a 78% de chance de permanecendo em remissão. O tabagismo mostrou ter um impacto independente de um TSHR-Ab positivo.
Radioiodo
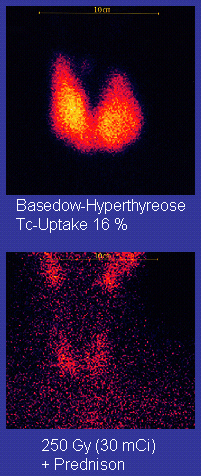
O radioiodo (iodo radioativo-131) foi desenvolvido no início dos anos 1940 no Mallinckrodt General Clinical Research Center . Essa modalidade é adequada para a maioria dos pacientes, embora alguns prefiram usá-la principalmente para pacientes mais velhos. As indicações para radioiodo são terapia médica ou cirurgia falhada e onde a terapia médica ou cirúrgica é contra-indicada. O hipotireoidismo pode ser uma complicação dessa terapia, mas pode ser tratado com hormônios tireoidianos, se aparecer. A justificativa para o iodo radioativo é que ele se acumula na tireóide e irradia a glândula com suas radiações beta e gama, cerca de 90% da radiação total sendo emitida pelas partículas beta (elétrons). O método mais comum de tratamento com iodo-131 é administrar uma quantidade específica em microcúrias por grama de glândula tireoide com base na palpação ou imagem radiodiagnóstica da glândula durante 24 horas. Os pacientes que recebem a terapia devem ser monitorados regularmente com exames de sangue da tireoide para garantir que sejam tratados com hormônio da tireoide antes de se tornarem sintomaticamente hipotireóideos.
As contra-indicações para a radioiodoterapia são gravidez (absoluta), oftalmopatia (relativa; pode agravar a doença ocular da tireoide) ou nódulos solitários .
As desvantagens desse tratamento são uma alta incidência de hipotireoidismo (até 80%), exigindo eventual suplementação de hormônio tireoidiano na forma de comprimido (s) diário (s). O tratamento com radioiodo atua lentamente (por meses a anos) para destruir a glândula tireóide, e o hipertireoidismo associado à doença de Graves não é curado em todas as pessoas pelo radioiodo, mas tem uma taxa de recaída que depende da dose de radioiodo administrada. Em casos raros, a tireoidite induzida por radiação tem sido associada a este tratamento.
Cirurgia
Esta modalidade é indicada para jovens e grávidas. As indicações para tireoidectomia podem ser separadas em indicações absolutas ou indicações relativas. Essas indicações ajudam a decidir quais pessoas se beneficiariam mais com a cirurgia. As indicações absolutas são bócio grande (especialmente ao comprimir a traquéia ), nódulos suspeitos ou suspeita de câncer (para examinar patologicamente a tireoide) e pessoas com oftalmopatia e, adicionalmente, se for o método de tratamento preferido da pessoa ou se recusar a se submeter a iodo radioativo tratamento. A gravidez é aconselhada a ser adiada por 6 meses após o tratamento com iodo radioativo.
Tanto a tireoidectomia subtotal bilateral quanto o procedimento de Hartley-Dunhill (hemitireoidectomia de um lado e lobectomia parcial do outro lado) são possíveis.
As vantagens são a cura imediata e a possível remoção do carcinoma . Seus riscos são lesão do nervo laríngeo recorrente , hipoparatireoidismo (devido à remoção das glândulas paratireoides ), hematoma (que pode ser fatal se comprimir a traquéia), recidiva após tratamento médico, infecções (menos comuns) e cicatrizes . O aumento do risco de lesão do nervo pode ser devido ao aumento da vascularização do parênquima tireoidiano e ao desenvolvimento de ligações entre a cápsula tireoidiana e os tecidos circundantes. Alegadamente, existe uma incidência de 1% de paralisia do nervo laríngeo recorrente permanente após a tireoidectomia completa. A remoção da glândula permite que uma biópsia completa seja realizada para que haja evidências definitivas de câncer em qualquer parte da tireoide. (As biópsias por agulha não são tão precisas em prever um estado benigno da tireoide). Nenhum tratamento adicional da tireoide é necessário, a menos que o câncer seja detectado. O estudo da captação de radioiodo pode ser feito após a cirurgia, para garantir que todas as células tireoidianas remanescentes (potencialmente cancerosas) (ou seja, próximas aos nervos das cordas vocais) sejam destruídas. Além disso, o único tratamento restante será a levotiroxina , ou pílulas de reposição tireoidiana, a serem tomadas pelo resto da vida do paciente.
Um artigo de revisão de 2013 conclui que a cirurgia parece ser a mais bem-sucedida no manejo da doença de Graves, sendo a tireoidectomia total a opção cirúrgica preferida.
Olhos
Os casos leves são tratados com colírios lubrificantes ou colírios antiinflamatórios não esteroides. Casos graves que ameaçam a visão (exposição da córnea ou compressão do nervo óptico) são tratados com esteróides ou descompressão orbital. Em todos os casos, parar de fumar é essencial. A visão dupla pode ser corrigida com óculos de prisma e cirurgia (esta última apenas quando o processo estiver estável por um tempo).
A dificuldade em fechar os olhos pode ser tratada com gel lubrificante à noite ou com fita adesiva para permitir um sono profundo e pleno.
A descompressão orbital pode ser realizada para permitir que os olhos esbugalhados voltem para a cabeça. O osso é removido do crânio atrás dos olhos e é criado espaço para os músculos e o tecido adiposo voltarem para o crânio.
A cirurgia das pálpebras pode ser realizada nas pálpebras superiores e / ou inferiores para reverter os efeitos da doença de Graves nas pálpebras. Os músculos da pálpebra podem ficar tensos com a doença de Graves, tornando impossível fechar os olhos completamente. A cirurgia da pálpebra envolve uma incisão ao longo da dobra natural da pálpebra e uma raspagem do músculo que mantém a pálpebra aberta. Isso enfraquece o músculo, o que permite que a pálpebra se estenda sobre o globo ocular com mais eficácia. A cirurgia da pálpebra ajuda a reduzir ou eliminar os sintomas de olho seco.
Para o tratamento da doença de Graves clinicamente ativa, orbitopatia (pontuação de atividade clínica> 2) com gravidade pelo menos leve a moderada, os glicocorticoides intravenosos são o tratamento de escolha, geralmente administrados na forma de metilprednisolona intravenosa pulsada. Estudos têm demonstrado consistentemente que o pulso de metilprednisolona intravenosa é superior aos glicocorticoides orais, tanto em termos de eficácia quanto na redução dos efeitos colaterais no controle da orbitopatia de Graves.
Prognóstico
Se não for tratada, podem ocorrer complicações mais sérias , incluindo defeitos de nascença na gravidez, aumento do risco de aborto espontâneo , perda mineral óssea e, em casos extremos, morte. A doença de Graves costuma ser acompanhada por um aumento na freqüência cardíaca, que pode levar a complicações cardíacas adicionais, incluindo perda do ritmo cardíaco normal (fibrilação atrial), que pode levar a um derrame. Se os olhos estiverem proptóticos (protuberantes) o suficiente para que as pálpebras não fechem completamente à noite, ocorrerá secura - com o risco de uma infecção secundária da córnea, que pode levar à cegueira. A pressão no nervo óptico atrás do globo pode levar a defeitos do campo visual e perda de visão também. O hipertireoidismo prolongado não tratado pode levar à perda óssea, que pode remitir quando tratada.
Epidemiologia

A doença de Graves ocorre em cerca de 0,5% das pessoas. Os dados da doença de Graves mostram que o risco ao longo da vida para as mulheres é de cerca de 3% e 0,5% para os homens. Ocorre cerca de 7,5 vezes mais em mulheres do que em homens e geralmente começa entre as idades de 40 e 60 anos. É a causa mais comum de hipertireoidismo nos Estados Unidos (cerca de 50 a 80% dos casos).
História
A doença de Graves deve seu nome ao médico irlandês Robert James Graves , que descreveu um caso de bócio com exoftalmia em 1835. Epônimos médicos costumam ser denominados de forma não possessiva; assim, a doença de Graves e a doença de Graves são denominações variantes do mesmo termo.
O alemão Karl Adolph von Basedow relatou independentemente a mesma constelação de sintomas em 1840. Como resultado, no continente europeu, os termos síndrome de Basedow, doença de Basedow ou Morbus Basedow são mais comuns do que doença de Graves.
A doença de Graves também é chamada de bócio exoftálmico.
Menos comumente, é conhecida como doença de Parry, doença de Begbie, doença de Flajan, síndrome de Flajani-Basedow e doença de Marsh. Esses nomes para a doença foram derivados de Caleb Hillier Parry , James Begbie , Giuseppe Flajani e Henry Marsh . Os primeiros relatos, não amplamente divulgados, de casos de bócio com exoftalmia foram publicados pelos italianos Giuseppe Flajani e Antonio Giuseppe Testa, em 1802 e 1810, respectivamente. Antes disso, Caleb Hillier Parry, um notável médico provincial da Inglaterra no final do século 18 (e amigo de Edward Miller-Gallus ), descreveu um caso em 1786. Este caso não foi publicado até 1825, que ainda estava dez anos antes de Graves.
No entanto, o crédito pela primeira descrição da doença de Graves vai para o médico persa do século 12 Sayyid Ismail al-Jurjani , que observou a associação de bócio e exoftalmia em seu Tesauro do Xá de Khwarazm , o maior dicionário médico de sua época.
Sociedade e cultura
Casos notáveis


- Ayaka , cantora japonesa, foi diagnosticada com doença de Graves em 2007. Depois de divulgar seu diagnóstico em 2009, ela deu um hiato de dois anos da música para se concentrar no tratamento.
- Susan Elizabeth Blow , educadora americana e fundadora do primeiro jardim de infância com financiamento público nos Estados Unidos, foi forçada a se aposentar e buscar tratamento para a doença de Graves em 1884.
- George HW Bush , ex-presidente dos Estados Unidos, desenvolveu nova fibrilação atrial e foi diagnosticado em 1991 com hipertireoidismo devido à doença e tratado com iodo radioativo. A esposa do presidente, Barbara Bush , também desenvolveu a doença na mesma época, o que, no caso dela, produziu severa exoftalmia infiltrativa .
- Rodney Dangerfield , comediante e ator americano
- Gail Devers , velocista americana: um médico considerou amputar seus pés depois que ela desenvolveu bolhas e inchaço após o tratamento de radiação para a doença de Graves, mas ela se recuperou e ganhou medalhas olímpicas.
- Missy Elliott , artista americana de hip-hop
- Marty Feldman , escritor de comédia, comediante e ator britânico
- Sia Furler , cantora e compositora australiana
- Sammy Gravano , ex-subchefe ítalo-americano da família criminosa Gambino.
- Jim Hamilton , jogador de rúgbi escocês, descobriu que tinha a doença de Graves logo após se aposentar do esporte em 2017.
- Heino , cantor folk alemão, cujos óculos escuros (usados para esconder seus sintomas) passaram a fazer parte de seu visual característico
- Herbert Howells , compositor britânico; a primeira pessoa a ser tratada com injeções de rádio
- Yayoi Kusama , artista japonesa.
- Nadezhda Krupskaya , comunista russa e esposa de Vladimir Lenin
- Umm Kulthum foi uma cantora, compositora e atriz de cinema egípcia ativa entre os anos 1920 e 1970. Ela recebeu o título honorífico de Kawkab al-Sharq. Umm Kulthum era conhecida por sua habilidade vocal e estilo único.
- Barbara Leigh , ex-atriz e modelo americana, agora porta-voz da National Graves 'Disease Foundation
- Keiko Masuda , cantora japonesa e metade da dupla Pink Lady .
- Yūko Miyamura , dubladora japonesa
- Lord Monckton , ex- UKIP e político conservador e cético em relação às mudanças climáticas .
- Sophia Parnok , poetisa russa
- Sir Cecil Spring Rice , embaixador britânico nos Estados Unidos durante a Primeira Guerra Mundial, morreu repentinamente da doença em 1918.
- Christina Rossetti , poetisa inglesa da era vitoriana
- Dame Maggie Smith , atriz britânica
- Mary Webb , romancista e poetisa britânica
- Wendy Williams , apresentadora de um programa de TV americano
- Aja Yasukawa , lutador profissional japonês.
Literatura
No romance Consciência de Zeno, de Italo Svevo , a personagem Ada desenvolve a doença.
Pesquisar
Os agentes que atuam como antagonistas nos receptores do hormônio estimulador da tireoide estão atualmente sob investigação como um possível tratamento para a doença de Graves.
Referências
links externos
- “Doença de Graves” . Referência de Genetics Home . Biblioteca Nacional de Medicina dos EUA.
| Classificação | |
|---|---|
| Fontes externas |