Extração (química) - Extraction (chemistry)

Extração em química é um processo de separação que consiste na separação de uma substância de uma matriz . Exemplos comuns incluem extração líquido-líquido e extração em fase sólida . A distribuição de um soluto entre duas fases é uma condição de equilíbrio descrita pela teoria da partição. Isso se baseia exatamente em como o analito se move do solvente inicial para o solvente de extração. O termo lavagem também pode ser usado para se referir a uma extração na qual as impurezas são extraídas do solvente contendo o composto desejado .
Tipos de extração
- Extração líquido-líquido
- Extração de fase sólida
- Extração ácido-base
- Extração de fluido supercrítico
- Extração assistida por ultrassom
- Extração de refluxo de calor
- Extração assistida por mecanoquímico
- Maceração
- Extração assistida por microondas
- Extração de queda de pressão controlada instantânea (DIC, do francês, Détente instantanée contrôlée)
- Perstraction
Aplicações e exemplos de laboratório
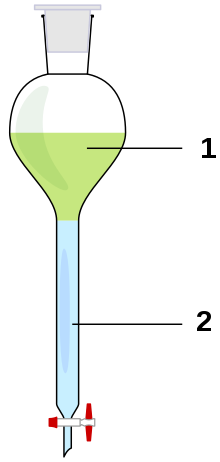
As extrações líquido-líquido no laboratório costumam fazer uso de funil separador , onde duas fases imiscíveis são combinadas para separar um soluto de uma fase para a outra, de acordo com a solubilidade relativa em cada uma das fases. Normalmente, isso será para extrair compostos orgânicos de uma fase aquosa para uma fase orgânica, mas também pode incluir a extração de impurezas solúveis em água de uma fase orgânica para uma fase aquosa.
Extratantes comuns podem ser dispostos em ordem crescente de polaridade de acordo com o parâmetro de solubilidade de Hildebrand :
acetato de etila < acetona < etanol < metanol <acetona: água (7: 3) <etanol: água (8: 2) <metanol: água (8: 2) < água
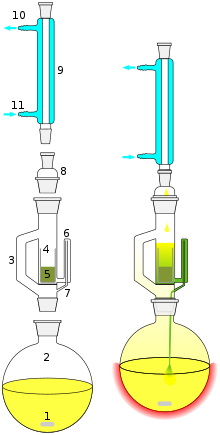
Extrações sólido-líquido em escala de laboratório podem usar extratores Soxhlet . Uma amostra sólida contendo o composto desejado junto com as impurezas é colocada no dedal. É escolhido um solvente de extração em que as impurezas são insolúveis e o composto desejado tem pelo menos uma solubilidade limitada. O solvente é refluxado e o solvente condensado cai no dedal e dissolve o composto desejado, que então passa de volta através do filtro para o frasco. Após a extração estar completa, o solvente pode ser removido e o produto desejado coletado.
Aplicações e exemplos do dia a dia
As folhas de chá fervidas na água extraem os taninos, a teobromina e a cafeína das folhas e a colocam na água, como um exemplo de extração sólido-líquido.
A descafeinação de chá e café também é um exemplo de extração, em que as moléculas de cafeína são removidas das folhas de chá ou dos grãos de café, geralmente utilizando extração de fluido supercrítico com CO 2 ou técnicas de extração sólido-líquido padrão.
Leitura adicional
- Gunt Hamburg, 2014, Thermal Process Engineering: Extração líquido-líquido e extração sólido-líquido, ver [1] , acessado em 12 de maio de 2014.
- GW Stevens, TC, Lo, & MHI Baird, 2007, "Extraction, Liquid-Liquid", em Kirk-Othmer Encyclopedia of Chemical Technology, doi : 10.1002 / 0471238961.120917211215.a01.pub2 , acessado em 12 de maio de 2014.
- T. Voeste, K. Weber, B. Hiskey & G. Brunner, 2006, "Liquid – Solid Extraction", em Ullmann's Encyclopedia of Industrial Chemistry, doi : 10.1002 / 14356007.b03_07.pub2 , acessado em 12 de maio de 2014.
- RJ Wakeman, 2000, "Extraction, Liquid-Solid", em Kirk-Othmer Encyclopedia of Chemical Technology, doi : 10.1002 / 0471238961.1209172123011105.a01 , acessado em 12 de maio de 2014.
- MJM Wells, 2000, "Essential guias to method development in solid-phase extract," in Encyclopedia of Separation Science , Vol. 10 (ID Wilson, ER Adlard, M. Cooke e CF Poole, eds.), London: Academic Press, London, 2000, pp. 4636-4643.
- Colin Poole & Michael Cooke, 2000, Extraction, em Encyclopedia of Separation Science, 10 Vols., ISBN 9780122267703 , acessado em 12 de maio de 2014.
Veja também
- Preparação da amostra (química analítica)
- Solvente
- Resinas impregnadas com solvente
- Extração de camada fina
- Lixiviação (Química)
Referências
Leitura adicional
- Fundamentals of Analytical Chemistry (8ª ed.).
links externos
-
 Mídia relacionada à Extração (química) no Wikimedia Commons
Mídia relacionada à Extração (química) no Wikimedia Commons