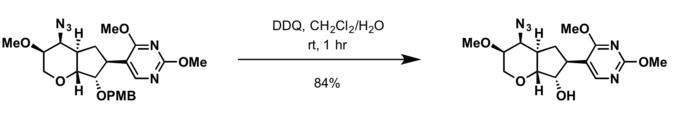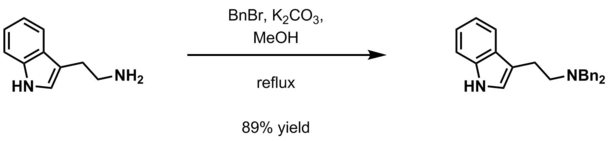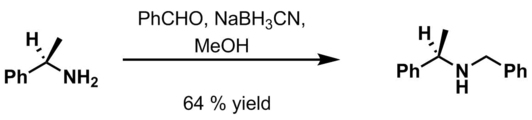Grupo benzil - Benzyl group
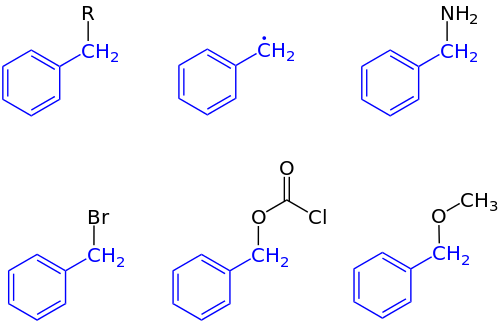
Em química orgânica , benzil é o substituinte ou fragmento molecular possuindo a estrutura C 6 H 5 CH 2 -. Benzil apresenta um anel de benzeno ligado a um grupo CH 2 .
Nomenclatura
Na nomenclatura IUPAC o prefixo benzilo refere-se a um grupo C 6 H 5 CH 2 substituinte, por exemplo, cloreto de benzilo ou benzoato de benzilo . Benzil não deve ser confundido com fenil com a fórmula C 6 H 5 . O termo benzílico é usado para descrever a posição do primeiro carbono ligado a um benzeno ou outro anel aromático . Por exemplo, (C 6 H 5 ) (CH 3 ) 2 C + é referido como um carbocátion "benzílico". O radical livre benzil tem a fórmula C
6 H
5 CH •
2 . O cátion benzil ou íon fenilcarbênio é o carbocátion com a fórmula C
6 H
5 CH +
2 ; o ânion benzila ou íon fenilmetaneto é o carbânion com a fórmula C
6 H
5 CH -
2 . Nenhuma dessas espécies pode ser formada em quantidades significativas na fase de solução sob condições normais, mas são referências úteis para a discussão dos mecanismos de reação e podem existir como intermediários reativos.
Abreviações
A abreviatura "Bn" denota benzilo. Por exemplo, o álcool benzílico pode ser representado como BnOH. Esta abreviatura não deve ser confundida com "Bz", que é a abreviatura para o grupo benzoílo C 6 H 5 C (O) -, ou o grupo fenilo C 6 H 5 , abreviado "Ph". Surpreendentemente, na literatura antiga, "Bz" também era usado para benzil.
Reatividade de centros benzílicos
A reatividade aumentada das posições benzílicas é atribuída à baixa energia de dissociação das ligações para as ligações C-H benzílicas. Especificamente, a ligação C 6 H 5 CH 2 −H é cerca de 10-15% mais fraca do que outros tipos de ligações C − H. O anel aromático vizinho estabiliza os radicais benzila. Os dados tabulados abaixo comparam a ligação C − H benzílica com as forças de ligação C − H relacionadas.
| Vinculo | Vinculo | Energia de dissociação de ligação | Comente | |
|---|---|---|---|---|
| (kcal / mol) | (kJ / mol) | |||
| C 6 H 5 CH 2 −H | ligação C − H benzílica | 90 | 377 | semelhantes às ligações C-H alílicas, tais ligações mostram reatividade aprimorada |
| H 3 C − H | ligação metil C − H | 105 | 439 | uma das ligações C − H alifáticas mais fortes |
| C 2 H 5 −H | ligação etil C − H | 101 | 423 | ligeiramente mais fraco do que H 3 C − H |
| C 6 H 5 −H | ligação fenil C − H | 113 | 473 | comparável ao radical de vinil, raro |
| CH 2 = CHCH 2 −H | ligação C – H alílica | 89 | 372 | semelhante ao CH benzílico |
| (C 6 H 4 ) 2 CH − H | ligação fluorenil C – H | 80 | mais ativado vs difenilmetilo ( pKa = 22,6) | |
| (C 6 H 5 ) 2 CH − H | ligação difenilmetil C – H | 82 | "duplamente benzílico" ( pKa = 32,2) | |
| (C 6 H 5 ) 3 C − H | ligação tritil C – H | 81 | 339 | "triplamente benzílico" |
A fraqueza da ligação C − H reflete a estabilidade do radical benzílico. Por razões relacionadas, os substituintes benzílicos exibem reatividade aumentada, como na oxidação , halogenação de radical livre ou hidrogenólise . Como um exemplo prático, na presença de catalisadores adequados, o p - xileno oxida exclusivamente nas posições benzílicas para dar ácido tereftálico :
- CH 3 C 6 H 4 CH 3 + 3 O 2 → HO 2 CC 6 H 4 CO 2 H + 2 H 2 O.
Milhões de toneladas de ácido tereftálico são produzidos anualmente por esse método.
Funcionalização na posição benzílica
Em alguns casos, essas transformações benzílicas ocorrem em condições adequadas para síntese em laboratório. A reação de Wohl-Ziegler irá bromar uma ligação C – H benzílica: (ArCHR 2 → ArCBrR 2 ). Qualquer grupo alquil benzílico não terciário será oxidado a um grupo carboxila por permanganato de potássio aquoso (KMnO 4 ) ou ácido nítrico concentrado (HNO 3 ): (ArCHR 2 → ArCOOH). Finalmente, o complexo de trióxido de cromo e 3,5-dimetilpirazol (CrO 3 –dmpyz) oxidará seletivamente um grupo metileno benzílico a um carbonil: (ArCH 2 R → ArC (O) R). O ácido 2-iodoxibenzoico em DMSO tem um desempenho semelhante.
Como um grupo protetor
Os grupos benzila são ocasionalmente empregados como grupos de proteção em síntese orgânica. Sua instalação e especialmente sua remoção requerem condições relativamente adversas, portanto, o benzil normalmente não é preferido para proteção.
Proteção contra álcool
Benzil é comumente usado em síntese orgânica como um grupo protetor robusto para álcoois e ácidos carboxílicos .
- Tratamento do álcool com uma base forte tal como o pó de hidróxido de potássio ou hidreto de sódio e haleto de benzilo ( BNCL ou BnBr )
- A monobenzilação de dióis pode ser alcançada usando Ag 2 O em dimetilformamida (DMF) em temperaturas ambiente a elevadas
- Os álcoois primários podem ser benzilados seletivamente na presença de grupos funcionais fenólicos usando Cu (acac) 2
Métodos de desprotecção
Os éteres benzílicos podem ser removidos sob condições redutoras , condições oxidativas e o uso de ácidos de Lewis .
- Removido por hidrogenólise
- Processo de elétron único com Na / NH 3 ou Li / NH 3
- Os grupos de proteção de benzila podem ser removidos usando uma ampla gama de agentes oxidantes, incluindo:
- CrO 3 / ácido acético à temperatura ambiente
- Ozônio
- N- bromossuccinimida (NBS)
- N- Iodosuccinimida (NIS)
- Iodeto de trimetilsilil (Me 3 SiI) em diclorometano à temperatura ambiente (a seletividade pode ser alcançada sob condições específicas)
O grupo de proteção p- metoxibenzil
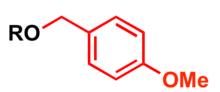
O p -metoxibenzil ( PMB ) é usado como um grupo de proteção para álcoois em síntese orgânica ( 4-metoxibenziltiol é usado para proteger tióis).
- Base forte, como hidróxido de potássio em pó ou hidreto de sódio e haleto de p- metoxibenzil (cloreto ou brometo)
- O 4-metoxibenzil-2,2,2-tricloroacetimidato pode ser usado para instalar o grupo PMB na presença de:
- Triflato de escândio (III) (Sc (OTf) 3 ) em tolueno a 0 ° C
-
Ácido trifluorometanossulfônico (TfOH) em diclorometano a 0 ° C
Métodos de desprotecção
- 2,3-Dicloro-5,6-diciano- p- benzoquinona (DDQ)
- As condições para a desproteção do grupo benzil são aplicáveis para a clivagem do grupo protetor de PMB
Proteção amina
O grupo benzila é ocasionalmente usado como um grupo protetor para aminas em síntese orgânica . Existem outros métodos.
- Aquosa de carbonato de potássio e haleto de benzilo ( BNCL , BnBr ) em metanol
-
Benzaldeído , HCl 6 M e NaBH 3 CN em metanol
Métodos de desprotecção
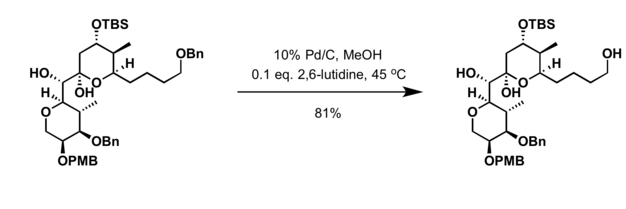
- Hidrogenação na presença do catalisador de paládio
Veja também
Referências
links externos
-
 Portal de química
Portal de química
-
 Citações relacionadas ao grupo Benzyl no Wikiquote
Citações relacionadas ao grupo Benzyl no Wikiquote