Astrocitoma - Astrocytoma
| Astrocitoma | |
|---|---|
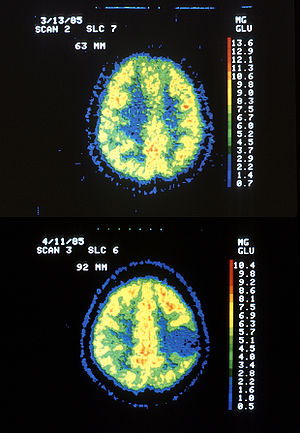 | |
| Duas imagens PET - a superior mostra um cérebro normal e a inferior mostra um astrocitoma. | |
| Especialidade | Neuro-oncologia , neurocirurgia |
Astrocitomas são um tipo de tumor cerebral . Eles se originam em um tipo específico de células da glia , células cerebrais em forma de estrela no cérebro chamadas astrócitos . Esse tipo de tumor geralmente não se espalha para fora do cérebro e da medula espinhal e geralmente não afeta outros órgãos. Astrocitomas são os gliomas mais comuns e podem ocorrer na maior parte do cérebro e, ocasionalmente, na medula espinhal.
Dentro dos astrocitomas, duas grandes classes são reconhecidas na literatura, aquelas com:
- Zonas estreitas de infiltração (principalmente tumores não invasivos; por exemplo, astrocitoma pilocítico, astrocitoma de células gigantes subependimárias, xantoastrocitoma pleomórfico), que muitas vezes são claramente delineados em imagens de diagnóstico
- Zonas difusas de infiltração (por exemplo, astrocitoma de alto grau, astrocitoma anaplásico, glioblastoma), que compartilham várias características, incluindo a capacidade de surgir em qualquer local do sistema nervoso central, mas com preferência pelos hemisférios cerebrais; eles ocorrem geralmente em adultos e têm uma tendência intrínseca de progredir para graus mais avançados.
As pessoas podem desenvolver astrocitomas em qualquer idade. O tipo de baixo grau é mais freqüentemente encontrado em crianças ou adultos jovens, enquanto o tipo de alto grau é mais prevalente em adultos. Astrocitomas na base do cérebro são mais comuns em pessoas jovens e representam cerca de 75% dos tumores neuroepiteliais.
Fisiopatologia
Astrocitoma causa efeitos regionais por compressão, invasão e destruição do parênquima cerebral , hipóxia arterial e venosa, competição por nutrientes, liberação de produtos finais metabólicos (por exemplo, radicais livres, eletrólitos alterados, neurotransmissores) e liberação e recrutamento de mediadores celulares (por exemplo , citocinas) que interrompem a função normal do parênquima. As sequelas clínicas secundárias podem ser causadas por pressão intracraniana elevada atribuível ao efeito direto de massa, aumento do volume sanguíneo ou aumento do volume do líquido cefalorraquidiano.
Alterações moleculares
Foi descoberto um padrão genômico de alterações do número de cópias (CNAs) do DNA, que está correlacionado com a sobrevivência do paciente e a resposta ao tratamento. Este padrão identifica entre os glioblastomas, bem como os pacientes com astrocitoma de baixo grau, um subtipo, onde o genótipo CNA está correlacionado com um fenótipo de sobrevida de aproximadamente um ano.
Diagnóstico
Uma tomografia computadorizada de raios-X (TC) ou ressonância magnética (MRI) é necessária para caracterizar a extensão desses tumores (tamanho, localização, consistência). A TC geralmente mostra distorção dos ventrículos terceiros e laterais com deslocamento das artérias cerebrais anterior e média. A análise histológica é necessária para classificar o diagnóstico.
No primeiro estágio do diagnóstico, o médico fará um histórico dos sintomas e realizará um exame neurológico básico, incluindo um exame oftalmológico e testes de visão, equilíbrio, coordenação e estado mental. O médico então exigirá uma tomografia computadorizada e ressonância magnética do cérebro do paciente. Durante uma tomografia computadorizada, raios-X do cérebro do paciente são tirados de muitas direções diferentes. Em seguida, eles são combinados por um computador, produzindo uma imagem transversal do cérebro. Para uma ressonância magnética, o paciente relaxa em um instrumento parecido com um túnel enquanto o cérebro é submetido a mudanças no campo magnético. Uma imagem é produzida com base no comportamento das moléculas de água do cérebro em resposta aos campos magnéticos. Um corante especial pode ser injetado em uma veia antes desses exames para fornecer contraste e tornar os tumores mais fáceis de identificar.
Se um tumor for encontrado, um neurocirurgião deve realizar uma biópsia. Isso envolve simplesmente a remoção de uma pequena quantidade de tecido tumoral, que é então enviada a um neuropatologista para exame e classificação. A biópsia pode ocorrer antes da remoção cirúrgica do tumor ou a amostra pode ser coletada durante a cirurgia. A classificação da amostra do tumor é um método de classificação que ajuda o médico a determinar a gravidade do astrocitoma e a decidir sobre as melhores opções de tratamento. O neuropatologista classifica o tumor procurando células atípicas, o crescimento de novos vasos sanguíneos e indicadores de divisão celular denominados figuras mitóticas.
Imagens de ressonância magnética de um paciente com astrocitoma, mostrando progressão do tumor ao longo de sete anos
Classificação
Dos vários sistemas de classificação em uso para a classificação de tumor do sistema nervoso central, o sistema de classificação da Organização Mundial da Saúde (OMS) é comumente usado para astrocitoma. Estabelecido em 1993 em um esforço para eliminar a confusão em relação aos diagnósticos, o sistema da OMS estabeleceu uma diretriz de classificação histológica de quatro camadas para astrocitomas que atribui um grau de 1 a 4, sendo 1 o menos agressivo e 4 o mais agressivo.
O esquema de classificação da OMS é baseado no aparecimento de certas características: atipia , mitose , proliferação endotelial e necrose . Essas características refletem o potencial maligno do tumor em termos de invasão e taxa de crescimento. Vários tipos de astrocitomas recebem estes graus da OMS:
| Grau OMS | Astrocitomas | Descrição |
|---|---|---|
| eu | Consistem em astrocitomas de crescimento lento, benignos e associados à sobrevivência a longo prazo. Indivíduos com tumores de crescimento muito lento, onde a remoção cirúrgica completa por cirurgia estereotáxica é possível, podem apresentar remissão total. Mesmo que o cirurgião não consiga remover todo o tumor, ele pode permanecer inativo ou ser tratado com sucesso com radiação. | |
| II |
|
Consistem em astrocitomas de crescimento relativamente lento, geralmente considerados benignos, que às vezes evoluem para tumores mais malignos ou de alto grau. Eles são prevalentes em pessoas mais jovens que freqüentemente apresentam convulsões. A sobrevida média varia com o tipo de célula do tumor. Os astrocitomas de grau 2 são definidos como gliomas invasivos, o que significa que as células tumorais penetram no cérebro normal circundante, tornando a cura cirúrgica mais difícil. Pessoas com oligodendrogliomas (que podem compartilhar células de origem comuns) têm melhores prognósticos do que aqueles com oligoastrocitomas mistos, que por sua vez têm melhores prognósticos do que pacientes com astrocitomas (puros) de baixo grau. Outros fatores que influenciam a sobrevivência incluem a idade (quanto mais jovem, melhor) e o status de desempenho (capacidade de realizar tarefas da vida diária). Devido à natureza infiltrativa desses tumores, as recorrências são relativamente comuns. Dependendo do paciente, a radioterapia ou quimioterapia após a cirurgia é uma opção. Indivíduos com astrocitoma de grau 2 têm uma taxa de sobrevivência de 5 anos de cerca de 34% sem tratamento e cerca de 70% com radioterapia. O tempo médio de sobrevivência é de 4 anos. |
| III | Astrocitoma anaplásico | Consistem em astrocitomas anaplásicos. Freqüentemente, está relacionado a convulsões, déficits neurológicos, dores de cabeça ou mudanças no estado mental. O tratamento inicial padrão é remover o máximo possível do tumor sem agravar os déficits neurológicos. A radioterapia demonstrou prolongar a sobrevida e é um componente padrão do tratamento. Indivíduos com astrocitoma de grau 3 têm uma sobrevida média de 18 meses sem tratamento (radiação e quimioterapia). Não há benefício comprovado da quimioterapia adjuvante ou suplementação de outros tratamentos para esse tipo de tumor. Embora a temozolomida seja eficaz no tratamento de astrocitoma anaplásico recorrente, seu papel como adjuvante à radioterapia não foi totalmente testado. |
| 4 | Glioblastoma multiforme (GBM) | Consiste em Glioblastoma multiforme (GBM), que é o tumor cerebral primário mais comum e maligno. O GBM primário cresce e se espalha para outras partes do cérebro rapidamente; eles podem se tornar muito grandes antes de produzirem sintomas, que geralmente começam abruptamente com convulsões. Menos de 10% se formam mais lentamente após a degeneração do astrocitoma de baixo grau ou astrocitoma anaplásico. Estes são chamados de GBM secundário e são mais comuns em pacientes mais jovens (idade média de 45 versus 62 anos). "A remoção cirúrgica continua sendo a base do tratamento, desde que uma lesão neurológica inaceitável possa ser evitada. A natureza extremamente infiltrativa desse tumor torna a remoção cirúrgica completa impossível. Embora a radioterapia raramente cure o glioblastoma, estudos mostram que ela dobra a sobrevida média dos pacientes, em comparação com cuidados de suporte sozinho. " O prognóstico é pior para esses gliomas de grau 4. Poucos pacientes sobrevivem além de 3 anos. Indivíduos com astrocitoma de grau 4 têm um tempo médio de sobrevida de 17 semanas sem tratamento, 30 semanas com radiação e 37 semanas com remoção cirúrgica da maior parte do tumor seguida por radioterapia. A sobrevida em longo prazo (pelo menos cinco anos) cai bem abaixo de 3%. |
De acordo com os dados da OMS, os astrocitomas de menor grau (grau I) representam apenas 2% dos astrocitomas registrados, grau II 8% e os astrocitomas anaplásicos de grau superior (grau III) 20%. O astrocitoma de grau mais alto (GBM grau IV) é o câncer do sistema nervoso primário mais comum e o segundo tumor cerebral mais frequente depois da metástase cerebral. Apesar da baixa incidência de astrocitomas em comparação com outros cânceres humanos, a mortalidade é significativa, pois os graus mais elevados (III e IV) apresentam altas taxas de mortalidade (principalmente devido à detecção tardia da neoplasia).
Prevenção
Não há diretrizes precisas porque a causa exata do astrocitoma não é conhecida.
Tratamento
Para astrocitomas de baixo grau, a remoção do tumor geralmente permite a sobrevivência funcional por muitos anos. Em alguns relatórios, a sobrevida de 5 anos foi superior a 90% com tumores bem ressecados. Na verdade, a ampla intervenção de condições de baixo grau é uma questão contestada. Em particular, os astrocitomas pilocíticos são comumente corpos indolentes que podem permitir a função neurológica normal. No entanto, quando deixados sem cuidados, esses tumores podem eventualmente sofrer transformação neoplásica. Até o momento, a ressecção completa de astrocitomas de alto grau é impossível devido à infiltração difusa de células tumorais no parênquima normal. Assim, os astrocitomas de alto grau recorrem inevitavelmente após a cirurgia ou terapia inicial e geralmente são tratados de forma semelhante ao tumor inicial. Apesar de décadas de pesquisa terapêutica, a intervenção curativa ainda é inexistente para astrocitomas de alto grau; Em última análise, o atendimento ao paciente concentra-se no gerenciamento paliativo .
Sociedade e cultura
Casos notáveis
Em março de 1990, o prolífico estrategista político do Partido Republicano dos Estados Unidos, Lee Atwater, foi diagnosticado com astrocitoma depois que um tumor foi encontrado em seu lobo parietal direito . Depois de se submeter à radioterapia (incluindo o então novo implante de radioterapia ), Atwater morreu no ano seguinte aos 40 anos.
O senador americano de longa data Ted Kennedy (D-MA) morreu de glioma maligno.
O atirador da Universidade do Texas, Charles Whitman , que matou várias pessoas durante um assassinato em massa em 1966, foi diagnosticado com astrocitoma post-mortem. A Comissão Connally que investigou o tiroteio concluiu que o tumor "possivelmente poderia ter contribuído para sua incapacidade de controlar suas emoções e ações".
Dan Quisenberry (arremessador da Liga Principal) foi diagnosticado com astrocitoma grau IV em janeiro de 1998. Ele morreu em 1998 em Leawood, Kansas.
Richard Burns , vencedor do Campeonato Mundial de Rally de 2001 , foi diagnosticado com astrocitoma em 2003. Quatro anos depois de vencer o Campeonato Mundial de Rally, em 25 de novembro de 2005, Burns morreu em Westminster , Londres, aos 34 anos, após ter participado de um coma por alguns dias como resultado de seu tumor cerebral.
Brittany Maynard , formada pela UC Berkeley e defensora da Death With Dignity, morreu em 19 de novembro de 2014, aos 29 anos, sendo assistida com autopreenchimento, tendo sido diagnosticada e lutado contra glioblastoma.
O lutador profissional Matt Cappotelli foi diagnosticado com astrocitoma de grau 2/3 em dezembro de 2005, fugindo dos planos para promover Cappottelli ao elenco principal da WWE . Cappotelli, que ganhou um contrato com a WWE através da terceira temporada de seu reality show Tough Enough , era o campeão dos pesos pesados da Ohio Valley Wrestling no momento de seu diagnóstico e desocupou o título em fevereiro de 2006 após confirmar que o tumor era cancerígeno. Cappotelli foi submetido a uma cirurgia e quimioterapia bem-sucedidas, mas não conseguiu retornar ao trabalho de luta livre. Ele retornou à OVW como treinador em 2013. Ele morreu em 29 de junho de 2018.
O senador John McCain (R-AZ) anunciou em 20 de julho de 2017 que havia sido diagnosticado com glioblastoma. O senador McCain sucumbiu à doença em 25 de agosto de 2018, 4 dias antes de seu 82º aniversário, em seu rancho perto de Sedona, Arizona.
Referências
Bibliografia
- "Tipos de adolescentes com câncer obtêm". KidsHealth - o site mais visitado da web sobre saúde infantil. Rede. 07 dez. 2009. KidsHealth.org Resultados da pesquisa: types-of-cancer - Nemours KidsHealth .
- "Astrocitoma - opções de diagnóstico e tratamento na Clínica Mayo." Mayo Clinic: Centros de Pesquisa e Tratamento Médico. Rede. 07 dez. 2009. Glioma - Sintomas e causas .
- "Tratamento de Glioblastoma Multiforme na Clínica Mayo." Mayo Clinic: Centros de Pesquisa e Tratamento Médico. Rede. 07 dez. 2009. Glioma - Sintomas e causas .
- "A nova Classificação da OMS de Tumores que afetam o Sistema Nervoso Central" por Stephen B. Tatter, MD, Ph.D.; MGH Arquivado em 30/01/2012 na Wayback Machine
links externos
- Cancer.Net: Astrocitoma, Infância
- Astrocitoma por imagem MR, CT, Patologia
| Classificação | |
|---|---|
| Fontes externas |



