Adenosina desaminase - Adenosine deaminase
| Adenosina / AMP desaminase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
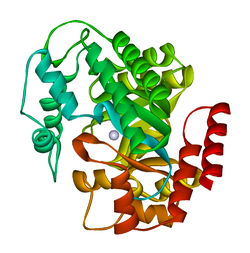
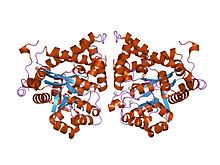 estrutura cristalina da adenosina desaminase plasmódio yoelii (py02076)
| |||||||||
| Identificadores | |||||||||
| Símbolo | A_deaminase | ||||||||
| Pfam | PF00962 | ||||||||
| Clã Pfam | CL0034 | ||||||||
| InterPro | IPR001365 | ||||||||
| PRÓSITO | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| CDD | cd01320 | ||||||||
| |||||||||
| Domínio da adenosina desaminase (editase) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | A_deamin | ||||||||
| Pfam | PF02137 | ||||||||
| InterPro | IPR002466 | ||||||||
| PRÓSITO | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| |||||||||
| Adenosina / AMP desaminase N-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | A_deaminase_N | ||||||||
| Pfam | PF08451 | ||||||||
| InterPro | IPR013659 | ||||||||
| |||||||||
A adenosina desaminase (também conhecida como adenosina amino-hidrolase ou ADA ) é uma enzima ( EC 3.5.4.4 ) envolvida no metabolismo das purinas . É necessário para a decomposição da adenosina dos alimentos e para a renovação dos ácidos nucleicos nos tecidos.
Sua função primária em humanos é o desenvolvimento e manutenção do sistema imunológico. No entanto, o papel fisiológico completo da ADA ainda não está completamente compreendido.
Estrutura
O ADA existe tanto na forma pequena (como um monômero) quanto na forma grande (como um complexo de dímero). Na forma monomérica, a enzima é uma cadeia polipeptídica, dobrada em oito cadeias de barris α / β paralelos, que circundam uma bolsa central profunda que é o sítio ativo. Além dos oito barris β centrais e oito hélices α periféricas , ADA também contém cinco hélices adicionais: resíduos 19-76 vezes em três hélices, localizadas entre as dobras β1 e α1; e duas hélices de terminal carboxi antiparalelas estão localizadas ao longo do terminal amino do cilindro β.
O sítio ativo ADA contém um íon zinco, que está localizado no recesso mais profundo do sítio ativo e coordenado por cinco átomos de His15, His17, His214, Asp295 e o substrato. O zinco é o único cofator necessário para a atividade.
O substrato, a adenosina, é estabilizado e ligado ao sítio ativo por nove pontes de hidrogênio. O grupo carboxila de Glu217, aproximadamente coplanar com o anel de purina do substrato, está em posição de formar uma ligação de hidrogênio com N1 do substrato. O grupo carboxila de Asp296, também coplanar com o anel de purina do substrato, forma ligação de hidrogênio com N7 do substrato. O grupo NH de Gly184 está em posição de formar uma ligação de hidrogênio com N3 do substrato. O Asp296 forma ligações tanto com o íon Zn 2+ quanto com o 6-OH do substrato. His238 também se liga ao substrato 6-OH. O 3'-OH do substrato ribose forma uma ligação de hidrogênio com Asp19, enquanto o 5'-OH forma uma ligação de hidrogênio com His17. Duas outras ligações de hidrogênio são formadas para moléculas de água, na abertura do sítio ativo, pelo 2'-OH e 3'-OH do substrato.
Devido ao recesso do sítio ativo dentro da enzima, o substrato, uma vez ligado, é quase completamente sequestrado do solvente. A exposição da superfície do substrato ao solvente quando ligado é de 0,5% da exposição da superfície do substrato no estado livre.
Reações
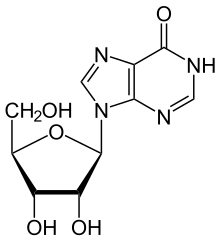
O ADA desamina irreversivelmente a adenosina, convertendo-a no nucleosídeo inosina relacionado pela substituição do grupo amino por um grupo ceto.
A inosina pode então ser deribosilada (removida da ribose ) por outra enzima chamada purina nucleosídeo fosforilase (PNP), convertendo-a em hipoxantina .
Mecanismo de catálise
O mecanismo proposto para a desaminação catalisada por ADA é a adição-eliminação estereoespecífica via intermediário tetraédrico. Por qualquer um dos mecanismos, o Zn 2+ como um eletrófilo forte ativa uma molécula de água, que é desprotonada pelo Asp295 básico para formar o hidróxido de ataque. His238 orienta a molécula de água e estabiliza a carga do hidróxido de ataque. Glu217 é protonado para doar um próton para N1 do substrato.
A reação é estereoespecífica devido à localização dos resíduos de zinco, Asp295 e His238, todos voltados para o lado B do anel de purina do substrato.
A inibição competitiva foi observada para ADA, onde o produto inosina atua no inibidor competitivo da atividade enzimática.
Função
ADA é considerada uma das principais enzimas do metabolismo das purinas. A enzima foi encontrada em bactérias, plantas, invertebrados, vertebrados e mamíferos, com alta conservação da sequência de aminoácidos . O alto grau de conservação da sequência de aminoácidos sugere a natureza crucial do ADA na via de recuperação da purina.
Primeiramente, o ADA em humanos está envolvido no desenvolvimento e manutenção do sistema imunológico. No entanto, a associação de ADA também foi observada com diferenciação de células epiteliais , neurotransmissão e manutenção da gestação . Também foi proposto que o ADA, além da degradação da adenosina, estimula a liberação de aminoácidos excitatórios e é necessário para o acoplamento de receptores de adenosina A1 e proteínas G heterotriméricas . A deficiência de adenosina desaminase leva à fibrose pulmonar, sugerindo que a exposição crônica a altos níveis de adenosina pode exacerbar as respostas inflamatórias em vez de suprimi-las. Também foi reconhecido que a proteína e a atividade da adenosina desaminase são reguladas positivamente em corações de camundongos que superexpressam HIF1α , o que em parte explica os níveis atenuados de adenosina em corações que expressam HIF-1α durante o estresse isquêmico .
Patologia
Algumas mutações no gene da adenosina desaminase fazem com que ela não seja expressa. A deficiência resultante é uma das causas da imunodeficiência combinada grave (SCID), particularmente da herança autossômica recessiva. Níveis deficientes de ADA também foram associados a inflamação pulmonar, morte de células tímicas e sinalização defeituosa do receptor de células T.
Por outro lado, as mutações que causam a superexpressão dessa enzima são uma das causas da anemia hemolítica .
Existem algumas evidências de que um alelo diferente (ADA2) pode levar ao autismo .
Níveis elevados de ADA também foram associados à AIDS .
Isoformas
Existem 2 isoformas de ADA: ADA1 e ADA2.
- O ADA1 é encontrado na maioria das células do corpo, particularmente linfócitos e macrófagos , onde está presente não apenas no citosol e no núcleo, mas também como ecto-forma na membrana celular ligada à dipeptidil peptidase-4 (também conhecida como CD26). O ADA1 está envolvido principalmente na atividade intracelular e existe tanto na forma pequena (monômero) quanto na forma grande (dímero). A interconversão de formas pequenas a grandes é regulada por um "fator de conversão" no pulmão.
- O ADA2 foi identificado pela primeira vez no baço humano. Posteriormente, foi encontrado em outros tecidos, incluindo o macrófago, onde coexiste com ADA1. As duas isoformas regulam a proporção de adenosina para desoxiadenosina, potencializando a morte de parasitas. O ADA2 é encontrado predominantemente no plasma e soro humano e existe apenas como um homodímero.
Significado clínico
ADA2 é a forma predominante presente no plasma sanguíneo humano e está aumentada em muitas doenças, particularmente aquelas associadas ao sistema imunológico: por exemplo, artrite reumatóide , psoríase e sarcoidose . A isoforma plasmática de ADA2 também está aumentada na maioria dos cânceres. ADA2 não é onipresente, mas coexiste com ADA1 apenas em monócitos-macrófagos.
O ADA plasmático total pode ser medido usando cromatografia líquida de alto desempenho ou técnicas enzimáticas ou colorimétricas. Talvez o sistema mais simples seja a medição da amônia liberada pela adenosina quando quebrada em inosina. Após a incubação do plasma com uma solução tamponada de adenosina, a amônia é reagida com um reagente de Berthelot para formar uma cor azul que é proporcional à quantidade de atividade enzimática. Para medir ADA2, eritro-9- (2-hidroxi-3-nonil) adenina (EHNA) é adicionada antes da incubação de modo a inibir a atividade enzimática de ADA1. É a ausência de ADA1 que causa a SCID .
O ADA também pode ser usado na investigação de derrames pleurais linfocíticos ou ascite peritoneal , em que tais amostras com níveis baixos de ADA excluem essencialmente a tuberculose de consideração.
Os derrames pleurais da tuberculose podem agora ser diagnosticados com precisão pelo aumento dos níveis de adenosina desaminase no líquido pleural, acima de 40 U por litro.
A cladribina e a pentostatina são agentes antineoplásicos usados no tratamento da leucemia de células pilosas ; seu mecanismo de ação é a inibição da adenosina desaminase.
Veja também
Referências
Leitura adicional
- da Cunha JG (1992). "[Adenosina desaminase. Uma enzima pluridisciplinar]". Acta Médica Portuguesa . 4 (6): 315–23. PMID 1807098 .
- Franco R, Casadó V, Ciruela F, Saura C, Mallol J, Canela EI, Lluis C (julho de 1997). "Adenosina desaminase de superfície celular: muito mais do que uma ectoenzima". Progress in Neurobiology . 52 (4): 283–94. doi : 10.1016 / S0301-0082 (97) 00013-0 . PMID 9247966 . S2CID 40318396 .
- Valenzuela A, Blanco J, Callebaut C, Jacotot E, Lluis C, Hovanessian AG, Franco R (1997). "O envelope gp120 do HIV-1 e as partículas virais bloqueiam a ligação da adenosina desaminase ao CD26 humano". Advances in Experimental Medicine and Biology . 421 : 185–92. doi : 10.1007 / 978-1-4757-9613-1_24 . ISBN 978-1-4757-9615-5. PMID 9330696 .
- Moriwaki Y, Yamamoto T, Higashino K (outubro de 1999). "Enzimas envolvidas no metabolismo das purinas - uma revisão da localização histoquímica e implicações funcionais". Histologia e histopatologia . 14 (4): 1321–40. PMID 10506947 .
- Hirschhorn R (1993). "Identificação de duas novas mutações missense (R156C e S291L) em dois pacientes ADA-SCID incomum para resposta à terapia com transfusões de troca parcial". Mutação Humana . 1 (2): 166–8. doi : 10.1002 / humu.1380010214 . PMID 1284479 . S2CID 44617309 .
- Berkvens TM, van Ormondt H., Gerritsen EJ, Khan PM, van der Eb AJ (agosto de 1990). "Deleção idêntica de 3250 pb entre duas repetições AluI nos genes ADA de pacientes não relacionados com ADA-SCID". Genômica . 7 (4): 486–90. doi : 10.1016 / 0888-7543 (90) 90190-6 . PMID 1696926 .
- Aran JM, Colomer D, Matutes E, Vives-Corrons JL, Franco R (agosto de 1991). "Presença de adenosina desaminase na superfície das células mononucleares do sangue: localização imunoquímica usando microscopia de luz e eletrônica" . The Journal of Histochemistry and Cytochemistry . 39 (8): 1001–8. doi : 10.1177 / 39.8.1856451 . PMID 1856451 .
- Bielat K, Tritsch GL (abril de 1989). "Ecto-enzima activity of human erythrocyte adenosine deaminase". Molecular and Cellular Biochemistry . 86 (2): 135–42. doi : 10.1007 / BF00222613 . PMID 2770711 . S2CID 20850552 .
- Hirschhorn R, Tzall S, Ellenbogen A, Orkin SH (fevereiro de 1989). "Identificação de uma mutação pontual resultando em uma adenosina desaminase termolábil (ADA) em duas crianças não relacionadas com deficiência parcial de ADA" . The Journal of Clinical Investigation . 83 (2): 497–501. doi : 10.1172 / JCI113909 . PMC 303706 . PMID 2783588 .
- Murray JL, Perez-Soler R, Bywaters D, Hersh EM (janeiro de 1986). "Diminuição da atividade da adenosina desaminase (ADA) e 5'nucleotidase (5NT) em células T do sangue periférico na doença de Hodgkin". American Journal of Hematology . 21 (1): 57–66. doi : 10.1002 / ajh.2830210108 . PMID 3010705 . S2CID 25540139 .
- Wiginton DA, Kaplan DJ, States JC, Akeson AL, Perme CM, Bilyk IJ, Vaughn AJ, Lattier DL, Hutton JJ (dezembro de 1986). "Sequência completa e estrutura do gene para a adenosina desaminase humana". Bioquímica . 25 (25): 8234–44. doi : 10.1021 / bi00373a017 . PMID 3028473 .
- Akeson AL, Wiginton DA, Dusing MR, States JC, Hutton JJ (novembro de 1988). "Alelos de adenosina desaminase humana mutante e sua expressão por transfecção em fibroblastos" . The Journal of Biological Chemistry . 263 (31): 16291–6. doi : 10.1016 / S0021-9258 (18) 37591-4 . PMID 3182793 .
- Glader BE, Backer K (fevereiro de 1988). "Atividade elevada da adenosina desaminase dos glóbulos vermelhos: um marcador de eritropoiese desordenada na anemia Diamond-Blackfan e outras doenças hematológicas". British Journal of Hematology . 68 (2): 165–8. doi : 10.1111 / j.1365-2141.1988.tb06184.x . PMID 3348976 . S2CID 44789636 .
- Petersen MB, Tranebjaerg L, Tommerup N, Nygaard P, Edwards H (fevereiro de 1987). "Nova atribuição do locus do gene da adenosina desaminase ao cromossomo 20q13 X 11 pelo estudo de um paciente com deleção intersticial 20q" . Journal of Medical Genetics . 24 (2): 93–6. doi : 10.1136 / jmg.24.2.93 . PMC 1049896 . PMID 3560174 .
- Orkin SH, Goff SC, Kelley WN, Daddona PE (abril de 1985). "Expressão transitória de cDNAs de adenosina desaminase humana: identificação de um clone não funcional resultante de uma única substituição de aminoácido" . Biologia Molecular e Celular . 5 (4): 762–7. doi : 10.1128 / mcb.5.4.762 . PMC 366780 . PMID 3838797 .
- Valerio D, Duyvesteyn MG, Dekker BM, Weeda G, Berkvens TM, van der Voorn L., van Ormondt H, van der Eb AJ (fevereiro de 1985). "Adenosina desaminase: caracterização e expressão de um gene com um promotor notável" . The EMBO Journal . 4 (2): 437–43. doi : 10.1002 / j.1460-2075.1985.tb03648.x . PMC 554205 . PMID 3839456 .
- Bonthron DT, Markham AF, Ginsburg D, Orkin SH (agosto de 1985). "Identificação de uma mutação pontual no gene da adenosina desaminase responsável pela imunodeficiência" . The Journal of Clinical Investigation . 76 (2): 894–7. doi : 10.1172 / JCI112050 . PMC 423929 . PMID 3839802 .
- Daddona PE, Shewach DS, Kelley WN, Argos P, Markham AF, Orkin SH (outubro de 1984). "Adenosina desaminase humana. CDNA e sequência de aminoácidos primária completa" . The Journal of Biological Chemistry . 259 (19): 12101–6. doi : 10.1016 / S0021-9258 (20) 71325-6 . PMID 6090454 .
- Valerio D, Duyvesteyn MG, Meera Khan P, Geurts van Kessel A, de Waard A, van der Eb AJ (novembro de 1983). "Isolamento de clones de cDNA para adenosina desaminase humana". Gene . 25 (2–3): 231–40. doi : 10.1016 / 0378-1119 (83) 90227-5 . PMID 6198240 .
links externos
- Localização do gene humano ADA no navegador do genoma UCSC .
- Detalhes do gene humano ADA no navegador do genoma UCSC .
- PDBe-KB fornece uma visão geral de todas as informações de estrutura disponíveis no PDB para adenosina desaminase humana
- O PDBe-KB fornece uma visão geral de todas as informações de estrutura disponíveis no PDB para Adenosina desaminase de camundongo